Clear Sky Science · pt
LncRNA FTX promove fibrose miocárdica ao sequestrar miR-335-3p para regular a sinalização TFEC/ILK
Por que a cicatriz no coração importa
A insuficiência cardíaca afeta dezenas de milhões de pessoas em todo o mundo e muitas vezes avança silenciosamente ao longo de anos. Um grande motor desse declínio é a fibrose miocárdica — a cicatrização lenta e progressiva do músculo cardíaco que o torna mais rígido e menos capaz de bombear sangue. Este estudo investiga a “fiação” molecular que ordena às células do coração que depositem tecido cicatricial em excesso e identifica uma nova cadeia de moléculas que pode ser alvo para desacelerar ou mesmo reverter esse processo prejudicial.
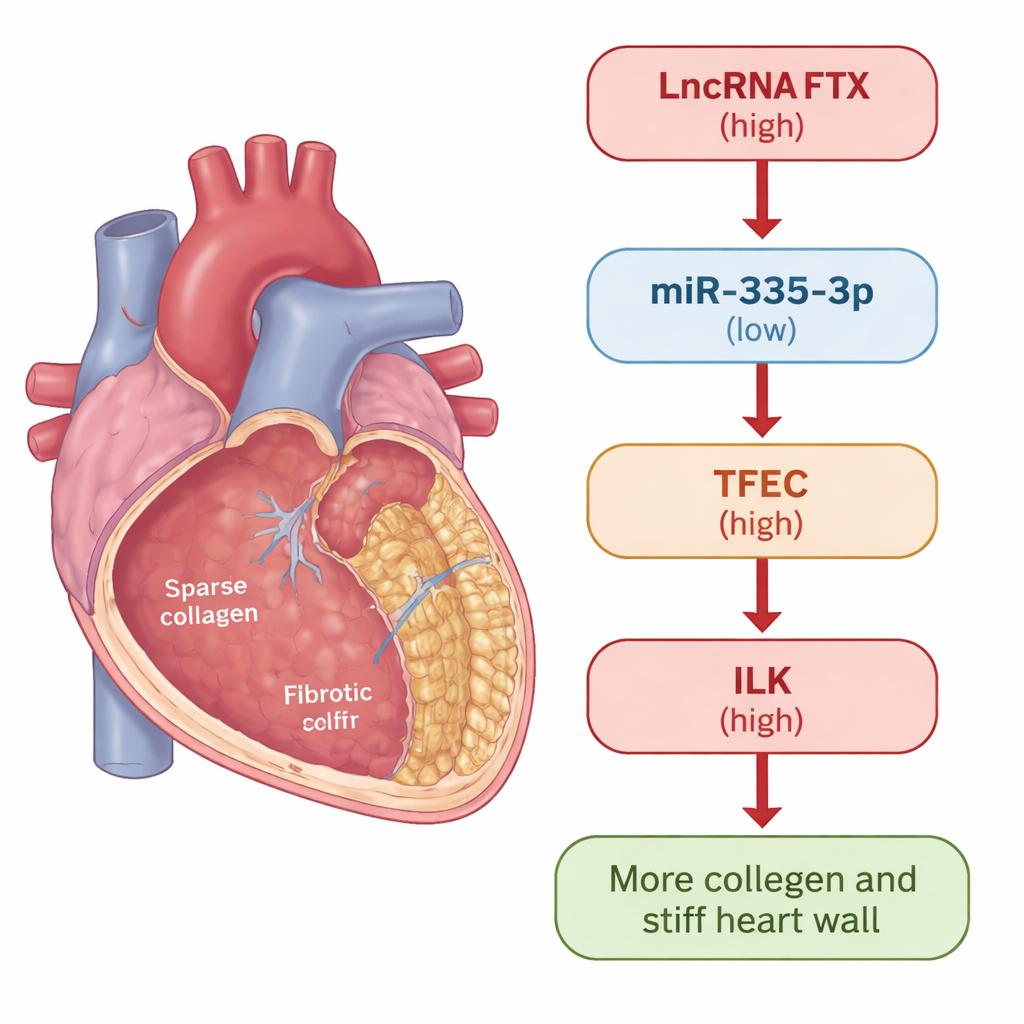
Um olhar mais atento sobre a cicatrização cardíaca
Quando o coração é lesionado ou submetido a estresse, células de suporte chamadas fibroblastos cardíacos entram em ação. Na reparação saudável, eles ajudam a remendar danos. Mas em doenças crônicas eles podem mudar para um estado hiperativo, produzindo excesso de colágeno e outros componentes da matriz extracelular, acabando por tornar a parede cardíaca rígida. Os pesquisadores usaram dois modelos para estudar esse processo: camundongos tratados com o fármaco isoproterenol, que induz de forma confiável fibrose cardíaca, e fibroblastos cardíacos humanos expostos à molécula sinalizadora TGF-β1, um conhecido indutor de cicatrização. Em ambos os cenários, mediram como genes e proteínas específicos mudaram conforme a fibrose se desenvolvia.
Uma reação em cadeia nociva dentro das células
A equipe concentrou-se em um fator de transcrição chamado TFEC, uma proteína que fica no núcleo celular e ativa outros genes. Eles descobriram que TFEC, junto com outra proteína chamada integrin-linked kinase (ILK), aumentava consistentemente quando os fibroblastos eram induzidos a um estado fibrótico formador de cicatriz. Silenciar TFEC ou ILK reduziu fortemente marcadores clássicos de fibrose, como α-actina de músculo liso e colágenos I e III, e também diminuiu uma via de controle de crescimento (sinalização Akt/GSK3β e Hippo) conhecida por promover a cicatrização tecidual. Experimentos de mapeamento de ligação ao DNA mostraram que TFEC se liga diretamente ao promotor do gene ILK e aumenta sua atividade, posicionando TFEC claramente a montante de ILK em uma cascata de sinalização pró-fibrose.
Interruptores de RNA que controlam o regulador mestre
Para entender o que controla o próprio TFEC, os pesquisadores recorreram aos RNAs não codificantes — moléculas de RNA que não produzem proteínas, mas atuam como reguladoras finas da atividade gênica. Identificaram um pequeno RNA, miR-335-3p, que estava reduzido em corações e células fibróticas. Elevar os níveis de miR-335-3p diminuiu TFEC, enquanto bloqueá-lo aumentou TFEC; testes de repórter confirmaram que miR-335-3p se liga diretamente às mensagens de TFEC para mantê-las sob controle. Em seguida, encontraram um RNA longo não codificante, chamado FTX, que estava elevado na fibrose e interagia fisicamente com miR-335-3p. O FTX atuou como uma esponja molecular: absorvia miR-335-3p, impedindo que esse pequeno RNA reprimisse TFEC. Como resultado, TFEC e ILK aumentaram, e os fibroblastos produziram mais colágeno formador de cicatriz.
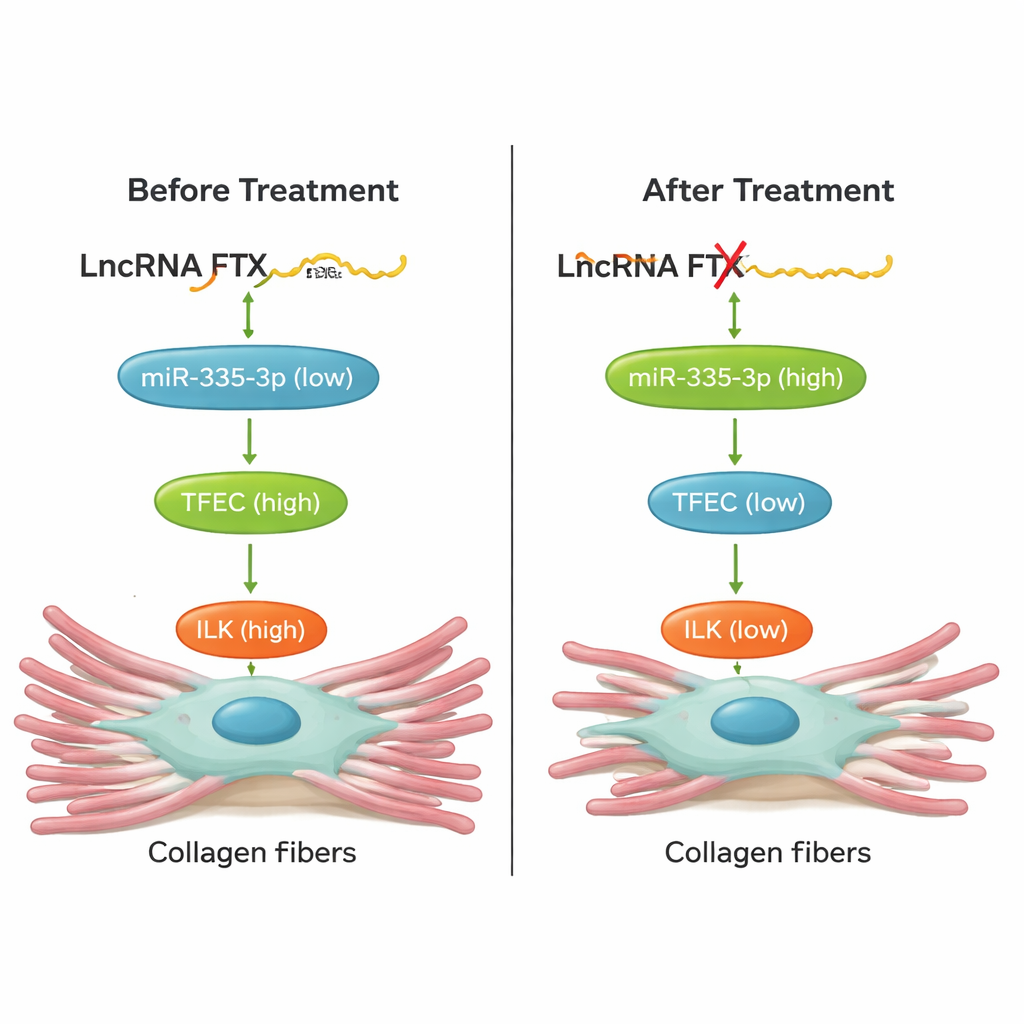
Da cultura celular aos corações vivos
De forma crucial, a equipe testou se interromper essa cadeia poderia realmente proteger corações em animais. Em camundongos expostos ao isoproterenol, reduzir TFEC, diminuir FTX no coração com um vetor de terapia gênica AAV9, ou aumentar miR-335-3p com um “agomir” quimicamente estabilizado levou a menos acúmulo de colágeno e níveis mais baixos de marcadores de fibrose no tecido cardíaco. Essas intervenções também melhoraram a função cardíaca: volume sistólico e fração de ejeção voltaram em direção ao normal, e aumentos prejudiciais da frequência cardíaca foram atenuados. Experimentos de resgate em células mostraram que alterar um componente do eixo FTX/miR-335-3p/TFEC/ILK mudava previsivelmente os outros, confirmando que se trata de uma via intimamente conectada e não de uma correlação frouxa.
O que isso significa para tratamentos futuros
Para um não-especialista, a mensagem principal é que os autores identificaram uma nova “alavanca de controle” para a cicatrização cardíaca. Um RNA longo chamado FTX afrouxa os freios (miR-335-3p) sobre um interruptor mestre (TFEC), que então ativa ILK e sinais pró-cicatrização a jusante, impulsionando a deposição excessiva de colágeno e o enrijecimento do coração. Reduzindo o FTX, restaurando miR-335-3p ou bloqueando diretamente TFEC foi possível, em camundongos, diminuir a cicatriz e melhorar a função de bombeamento. Embora sejam necessários mais estudos para confirmar essa via em pacientes humanos e desenvolver terapias seguras, essa cadeia regulatória baseada em RNA oferece vários pontos promissores para intervir na insuficiência cardíaca impulsionada pela fibrose.
Citação: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
Palavras-chave: fibrose miocárdica, insuficiência cardíaca, RNA não codificante, fibroblastos cardíacos, sinalização da fibrose