Clear Sky Science · pt
Fragmento intravenoso da proteína HMGB1 melhora função cardíaca, fibrose e fluxo coronariano em modelo suíno de cardiomiopatia isquêmica
Por que este estudo cardíaco importa
A insuficiência cardíaca torna-se mais comum à medida que as populações envelhecem, e muitos pacientes com danos severos após infartos acabam ficando sem opções de tratamento. Procedimentos como transplantes cardíacos ou bombas mecânicas podem salvar vidas, mas são altamente invasivos e nem sempre indicados. Este estudo explora uma abordagem menos invasiva: um pequeno fragmento de uma proteína natural, administrado por infusão venosa simples, que parece ajudar o coração a se reparar em um modelo de grande animal que se aproxima da doença cardíaca humana.
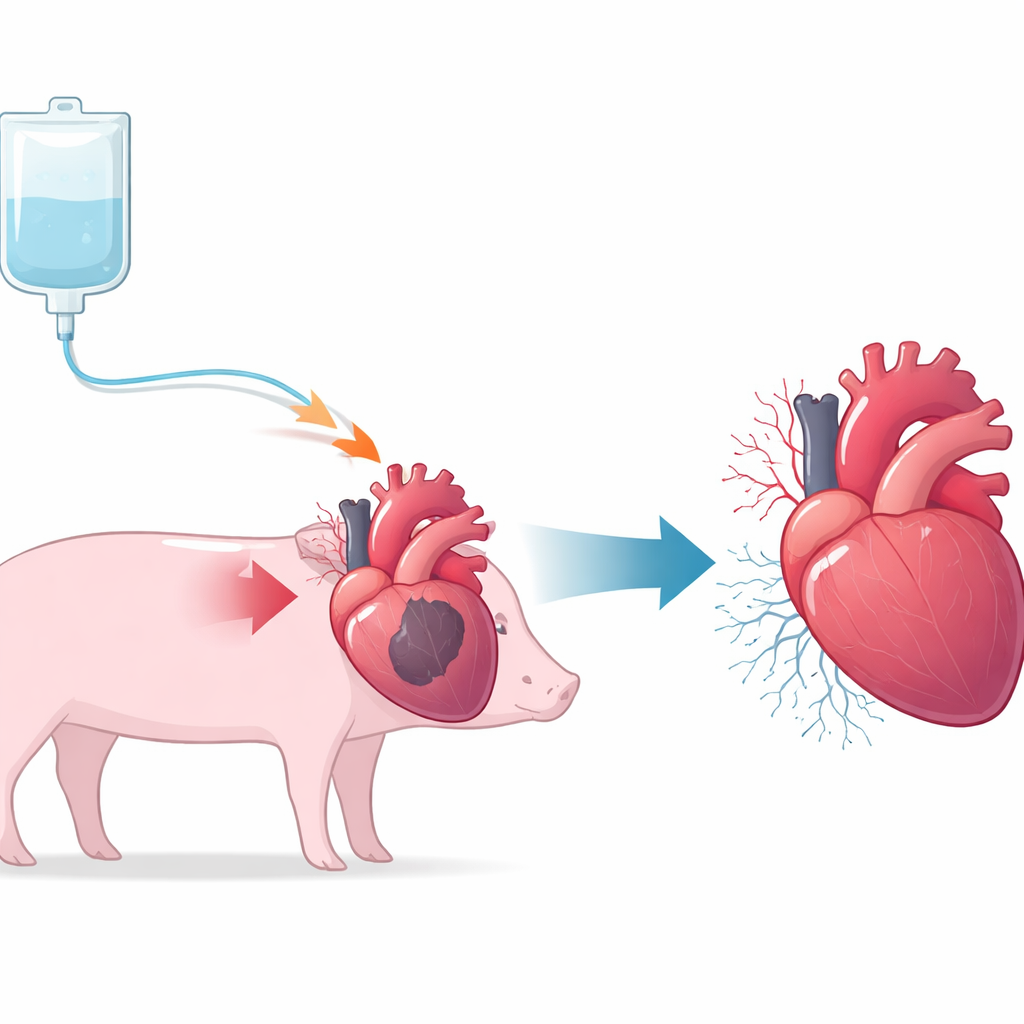
Uma nova forma de mobilizar a equipe de reparo do próprio corpo
Os pesquisadores concentraram-se em uma proteína chamada high mobility group box 1, ou HMGB1. No organismo, a HMGB1 atua no controle de genes, na inflamação e na cicatrização dos tecidos. Trabalhos anteriores mostraram que um fragmento específico da HMGB1 pode atrair células reparadoras provenientes da medula óssea — chamadas células-tronco mesenquimais — para a corrente sanguínea e em direção a tecidos lesionados. A equipe investigou se esse fragmento, administrado por via venosa, poderia melhorar a função cardíaca em porcos com cardiomiopatia isquêmica, condição em que perda prévia de fluxo sanguíneo deixa o coração fraco e cicatrizado, semelhante ao que ocorre em muitos pacientes após infartos.
Construindo um modelo realista de coração danificado
Para imitar a doença arterial coronariana crônica, os cientistas reduziriam parcialmente o calibre de uma artéria cardíaca principal em mini porcos usando um anel que se estreita lentamente, criando fluxo sanguíneo insuficiente de longa duração e formação de cicatrizes. Após quatro semanas, os animais apresentaram função de ejeção reduzida, dilatação cardíaca e áreas danificadas visíveis em exames avançados. Os porcos foram então randomizados em dois grupos: um recebeu cinco doses intravenosas do fragmento HMGB1 ao longo de dez dias, enquanto o outro recebeu apenas solução salina. Os animais foram acompanhados por mais oito semanas com ecocardiografia, ressonância magnética cardíaca, medições de pressão nas artérias coronárias e análise detalhada dos tecidos após eutanásia humanitária.
Batidas mais fortes, menos cicatriz, melhor fluxo sanguíneo
Em vários modos de imagem, os porcos tratados exibiram um padrão claro de recuperação em comparação com os controles. Ultrassom padrão e ressonância magnética revelaram que a eficiência de bombeamento do coração — a fração de sangue ejetada a cada batida — aumentou no grupo HMGB1, mas não nos animais não tratados. O volume de sangue residual após cada contração diminuiu, indicando uma contração mais forte e eficaz. As imagens de ressonância que destacam tecido cicatricial mostraram que as áreas de músculo danificado e inativo encolheram nos animais tratados, enquanto se expandiram nos controles. Medições realizadas com fios finos dentro das artérias coronárias indicaram que a capacidade dos vasos em aumentar o fluxo quando necessário — chamada reserva de fluxo coronariano — melhorou com o tratamento por HMGB1, sugerindo vasos pequenos mais saudáveis que nutrem o músculo cardíaco.
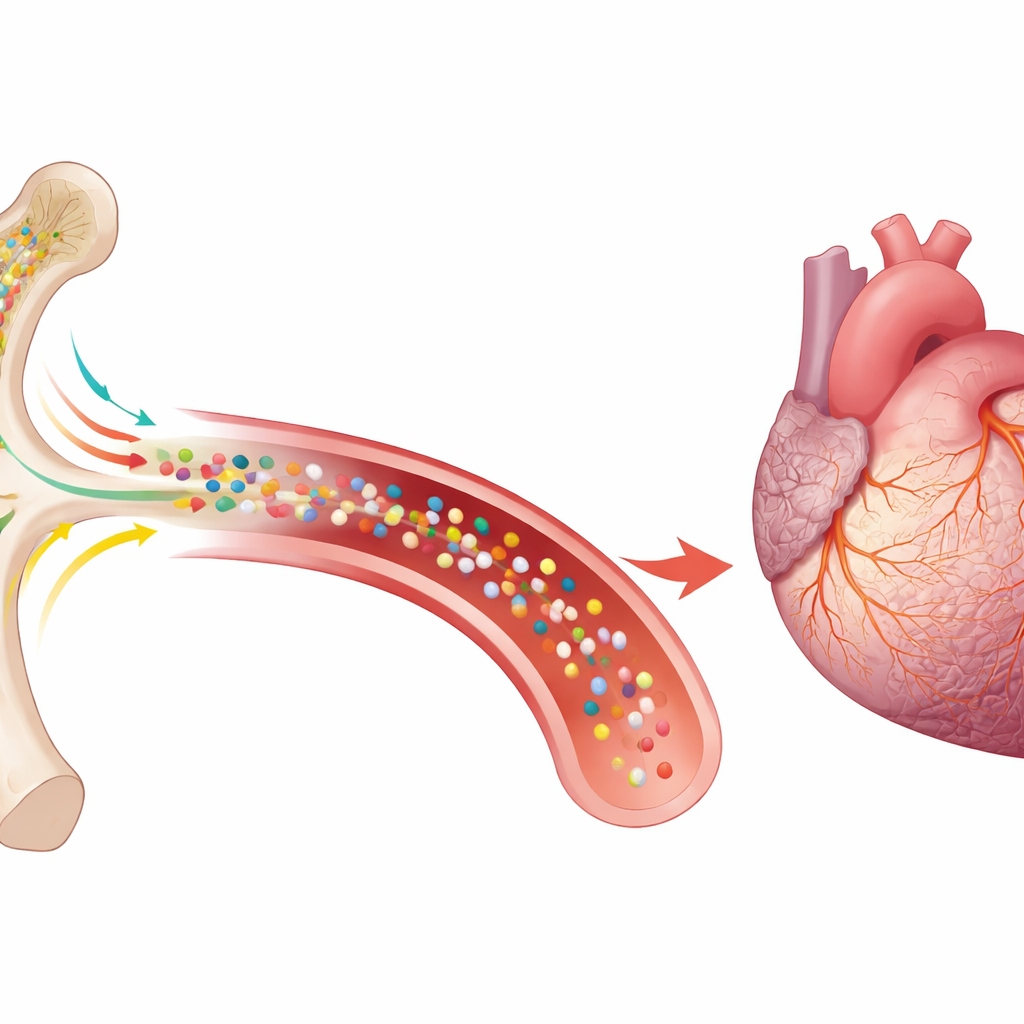
Sinais de reparo ao microscópio
Ao examinar os corações diretamente, as zonas de transição ao redor da lesão antiga pareceram mais saudáveis nos animais tratados. As células musculares eram menores e mais uniformes, em vez de alongadas e inchadas como observado em corações em falha. Houve uma tendência à redução do tecido fibrótico, e muito mais pequenos vasos sanguíneos revestidos por células especializadas, consistente com formação de nova vasculatura. Testes moleculares mostraram níveis mais elevados de vários fatores conhecidos por estimular a formação de vasos, limitar a cicatrização excessiva e moderar a inflamação. Marcadores associados a células reparadoras derivadas da medula óssea também estavam um pouco mais elevados, apoiando a ideia de que o fragmento recrutou o sistema de reparo celular do próprio organismo, em vez de atuar como um fármaco convencional que mira uma única via.
O que isso pode significar para pacientes no futuro
Em conjunto, os achados sugerem que doses intravenosas repetidas de um fragmento da HMGB1 podem desencadear um amplo programa de autorreparo em um modelo de grande animal de dano cardíaco crônico. O tratamento pareceu estimular a formação de novos vasos, reduzir fibrose prejudicial e restaurar a função em músculo cardíaco em hibernação, porém ainda vivo, tudo sem a necessidade de transplante celular ou cirurgia de alto risco. Embora sejam necessários mais estudos para confirmar a segurança, refinar posologia e demonstrar benefício em humanos, essa abordagem aponta para um futuro em que algumas formas de insuficiência cardíaca severa poderiam ser tratadas despertando a capacidade de cura do próprio coração.
Citação: Ito, Y., Kawamura, M., Kawamura, T. et al. Intravenous high mobility group box 1 fragment improves cardiac function, fibrosis, and coronary flow in porcine ischemic cardiomyopathy model. Sci Rep 16, 8350 (2026). https://doi.org/10.1038/s41598-026-38592-7
Palavras-chave: insuficiência cardíaca, cardiomiopatia isquêmica, terapia regenerativa, células-tronco mesenquimais, fragmento HMGB1