Clear Sky Science · pt
Otimização de agentes ligantes de galectina-3 por síntese múltipla de compostos in situ e espectrometria de massa nativa
Por que isso importa para medicamentos futuros
Muitos medicamentos modernos atuam aderindo a proteínas dentro do nosso corpo, mas encontrar uma pequena molécula que se una com alta afinidade e seletividade ao sítio correto é um processo lento, caro e frequentemente frustrante. Este estudo apresenta uma forma mais rápida de ajustar essas moléculas diretamente na presença da proteína-alvo e, em seguida, identificar as melhores com uma técnica de pesagem altamente sensível. Os autores demonstram a abordagem na galectina‑3, uma proteína ligada ao crescimento do câncer, e chegam a um candidato promissor com propriedades semelhantes às de alguns dos melhores compostos existentes, porém em um bolso inesperado na superfície da proteína.

Repensando como procuramos melhores candidatos a fármacos
A otimização tradicional de fármacos assemelha-se a um jogo de adivinhação caro. Químicos alteram um composto inicial passo a passo, testam cada versão e esperam melhorar a afinidade pelo alvo proteico. Mas as superfícies proteicas são flexíveis, moléculas de água atrapalham, e o evento de ligação pode remodelar a proteína, tornando previsões computacionais pouco confiáveis. Mesmo quando uma estrutura de alta resolução está disponível, não há garantia de que uma modificação sugerida será benéfica. Métodos existentes de “síntese guiada pelo alvo” tentam deixar que a proteína escolha seus parceiros a partir de um conjunto de blocos construtores, mas essas abordagens ainda dependem de análises complexas e sinais indiretos para inferir qual composto realmente se liga melhor.
Deixe a proteína escolher e então pese os vencedores
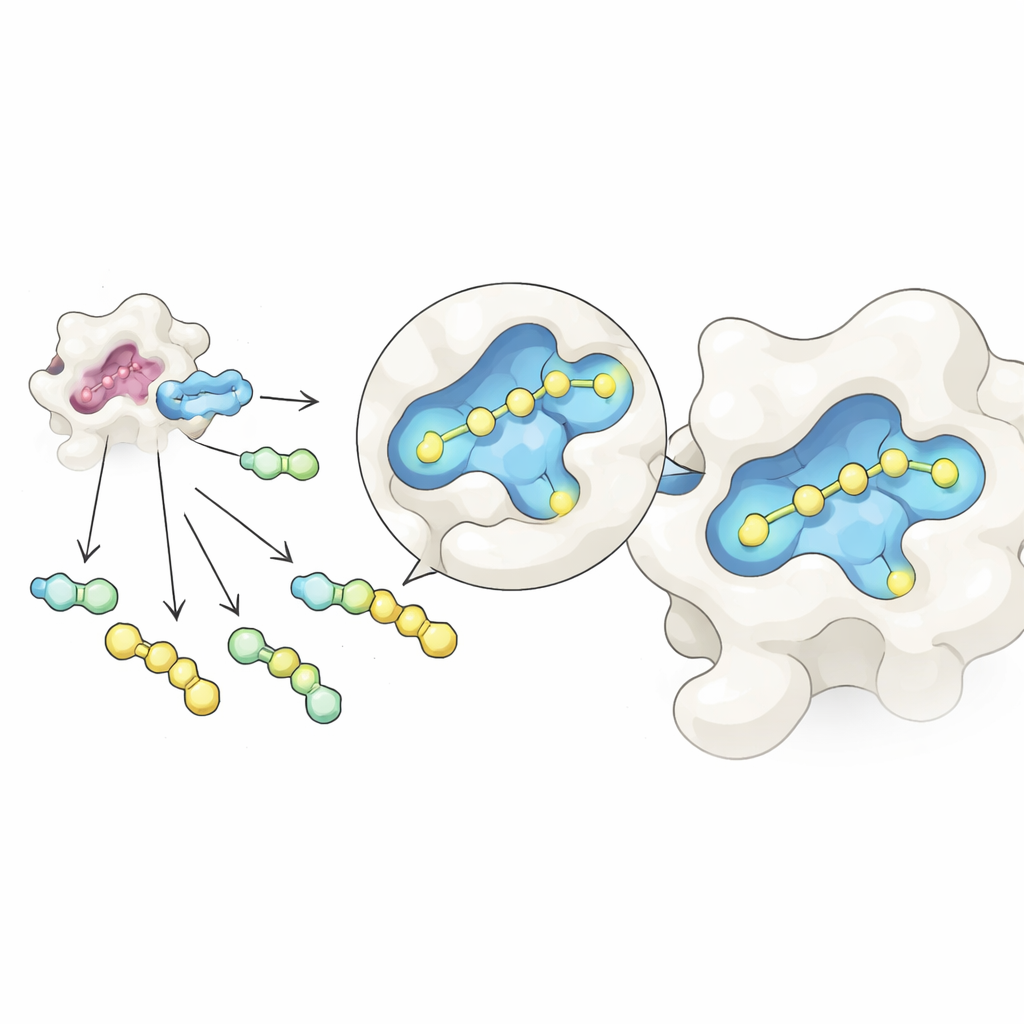
Os pesquisadores combinaram duas ideias em um fluxo de trabalho integrado. Primeiro, usaram uma reação química reversível que liga um núcleo comum baseado em açúcar a muitas diferentes peças laterais em um único tubo, formando uma mistura de moléculas relacionadas. Ao ajustar cuidadosamente as proporções iniciais, os produtos resultantes alcançam um estado equilibrado regido por regras simples de concentração, o que ajuda a equalizar suas quantidades apesar de diferenças na reatividade bruta. Segundo, expuseram essa mistura à galectina‑3 e a examinaram com espectrometria de massa nativa, uma forma de espectrometria de massa que mantém pares proteína–molécula intactos em uma solução suave, semelhante à água. Como cada candidato tem massa distinta, o instrumento pode detectar diretamente quais moléculas estão realmente ligadas à proteína, sem rótulos ou marcadores de referência.
De misturas lotadas a um ligante de destaque
Com essa montagem, a equipe criou dezenas de ligantes de galectina‑3 ao ligar vários grupos laterais a um núcleo de açúcar inspirado em um inibidor conhecido, GB1107. Eles dividiram 35 peças hidrazida diferentes em grupos manejáveis, formaram todas as combinações in situ e então adicionaram galectina‑3. A espectrometria de massa nativa destacou os compostos que mais frequentemente viajavam junto com a proteína, sinalizando-os como hits primários. Um teste posterior de estabilidade térmica, que mede como um composto estabiliza a proteína quando aquecida, filtrou falsos positivos causados por particularidades da medição no estado gasoso. Três candidatos principais permaneceram, e medições detalhadas de ligação baseadas em calor mostraram que um, chamado GalAldBZ20, ligou‑se à galectina‑3 com afinidade especialmente alta, na faixa sub‑micromolar.
Descobrindo um bolso oculto e tornando‑o mais forte
A próxima surpresa ocorreu quando a equipe analisou como GalAldBZ20 se posicionava na superfície da galectina‑3. A maioria dos ligantes conhecidos usa um bolso “alfa” próximo ao sítio de ligação do açúcar, mas métodos estruturais e simulações computacionais indicaram que o GalAldBZ20 favorecia em vez disso um bolso vizinho “beta”. Cristalografia de raios X sugeriu isso, ressonância magnética nuclear em solução revelou múltiplas conformações locais próximas a esse bolso, e simulações de dinâmica molecular apoiaram um modelo em que um anel contendo nitro da molécula se aloja no sítio beta. Raciocinando que poderiam fixar esse arranjo com mais firmeza, os químicos redesenharam o ligante químico entre o açúcar e o anel nitro para favorecer novos contatos polares com a proteína e reduzir a flexibilidade.
Transformando uma triagem inteligente em um candidato potente
Com essa visão, a equipe sintetizou um pequeno conjunto de moléculas subsequentes mais rígidas que mantinham o mesmo açúcar e o anel nitro, mas alteravam o conector entre eles. Uma versão, um N‑galactosídeo (composto 5), destacou‑se: ela ligou a galectina‑3 aproximadamente dez vezes mais fortemente que o hit original, alcançando uma afinidade comparável à do GB1107, e ainda assim preferindo o bolso beta. Uma estrutura cristalina de ultra‑alta resolução mostrou densidade clara para o anel nitro alojado nesse bolso, sustentado por várias ligações de hidrogênio e um contato catiônico‑π com aminoácidos-chave. Quando o grupo nitro foi removido ou substituído por um grupo metila simples, a ligação enfraqueceu notavelmente, enfatizando sua importância. Como a galectina‑1, uma proteína relacionada, carece desse bolso beta, o novo composto pode, em última instância, oferecer melhor seletividade — uma característica valorizada no desenho de fármacos.
O que isso significa para a descoberta de fármacos no futuro
Em termos acessíveis, este trabalho demonstra que é possível misturar muitas moléculas relacionadas, deixar uma proteína relevante para a doença “escolher” suas favoritas e então pesar diretamente esses pares proteína–molécula para ver quais aderem melhor. Aplicada à galectina‑3, essa estratégia encontrou inesperadamente e depois fortaleceu a ligação a um bolso pouco explorado, produzindo um composto que rivaliza com alguns dos melhores inibidores existentes e pode servir como ponto de partida para novos fármacos anticâncer. Mais amplamente, acoplar química in situ com espectrometria de massa nativa oferece um atalho geral para refinar candidatos a fármacos contra proteínas com múltiplos sítios de ligação possíveis, potencialmente poupando tempo, materiais e esforço nas fases iniciais da descoberta de fármacos.
Citação: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Palavras-chave: inibidores de galectina-3, espectrometria de massa nativa, descoberta de fármacos baseada em fragmentos, síntese guiada pelo alvo, candidatos a fármacos contra o câncer