Clear Sky Science · pt
Inibição direcionada de HDAC8 com compostos não-hidroxamato [1,2,4]triazolo[4,3-a]quinolina
Nova esperança para um câncer infantil
O neuroblastoma é um câncer infantil agressivo que surge de células nervosas e costuma ser difícil de tratar uma vez que se espalha. Este estudo explora uma nova forma de desacelerar ou eliminar células de neuroblastoma ao desligar um interruptor celular chave chamado HDAC8. Ao construir uma nova família de moléculas com propriedades de fármaco que atuam de forma muito seletiva sobre esse interruptor, os pesquisadores buscam criar tratamentos que sejam ao mesmo tempo mais eficazes contra tumores e mais suaves para o resto do corpo.
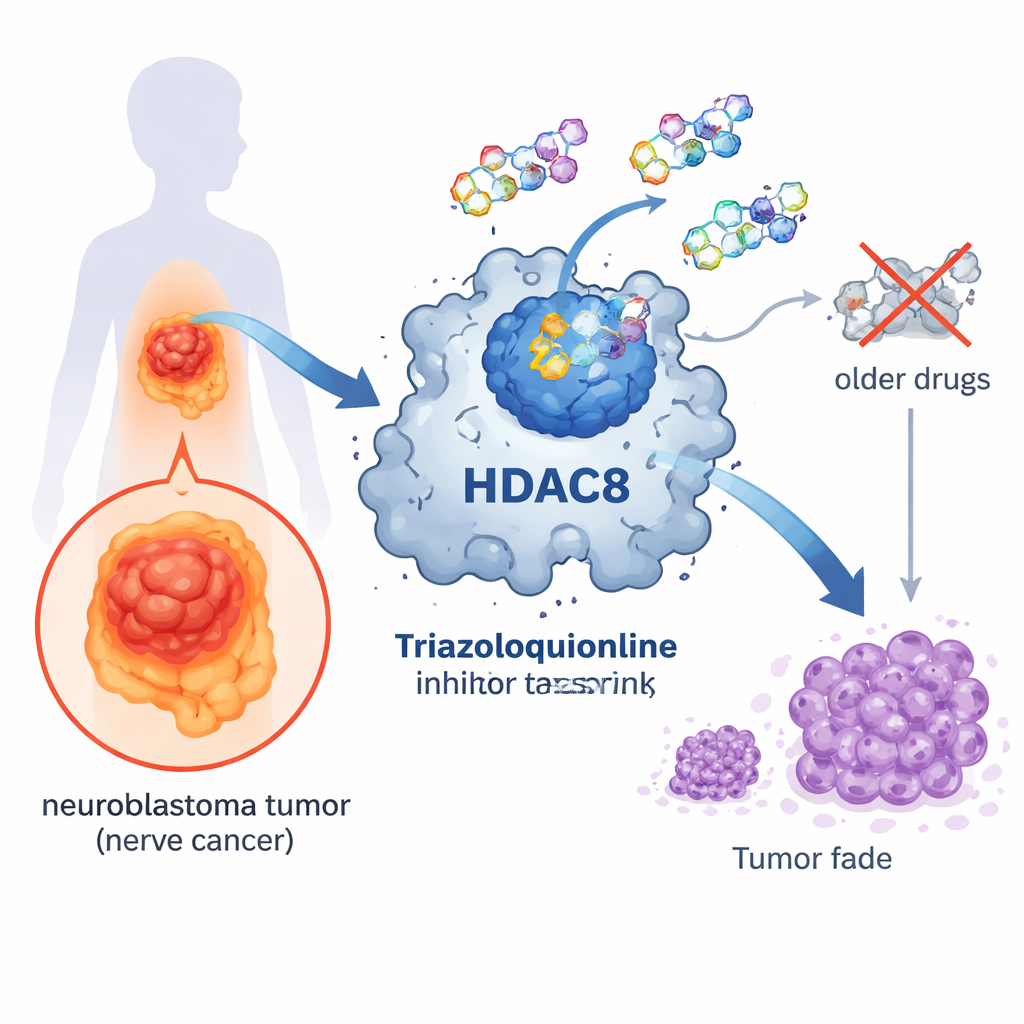
Um interruptor molecular no coração do câncer
Dentro de nossas células, genes estão constantemente sendo ativados e desativados. Um sistema de controle importante depende de pequenas etiquetas químicas chamadas grupos acetila que se ligam a proteínas associadas ao DNA. Enzimas chamadas histona desacetilases (HDACs) removem essas etiquetas, compactando o empacotamento do DNA e geralmente reduzindo a atividade gênica. A HDAC8 é um membro dessa família de enzimas e tem sido associada a vários cânceres, incluindo o neuroblastoma. Quando a HDAC8 está hiperativa, células cancerosas podem crescer, sobreviver e se disseminar mais facilmente, tornando-a um alvo atraente para novos fármacos.
Limitações dos antigos fármacos contra HDAC
Vários medicamentos que bloqueiam HDACs já são aprovados para alguns cânceres do sangue, mas tendem a atingir muitos tipos de HDAC ao mesmo tempo. A maioria dessas drogas usa um grupo químico hidroxamato para se ligar a um íon metálico no sítio ativo da enzima. Embora eficaz, esse grupo se liga aos metais com tanta força que pode levar a efeitos colaterais e limita a capacidade do fármaco de diferenciar com precisão entre diferentes HDACs. Como resultado, pacientes podem experimentar toxicidade, e células normais podem ser prejudicadas juntamente com as células tumorais. Por isso, os pesquisadores têm buscado desenhos químicos alternativos que mantenham os benefícios antitumorais enquanto reduzem os danos indesejados.
Desenvolvendo uma nova classe de inibidores direcionados
Neste trabalho, a equipe projetou e sintetizou 21 novos compostos construídos em torno de um esqueleto triazoloquinolina, conectado por um ligante flexível a uma região de "+alpha-amino amida" que pode se ligar ao átomo de zinco no sítio ativo da HDAC8. Usando projeto auxiliado por computador, escolheram essa arquitetura para se ajustar a um estreito “canal de liberação de acetato” único da HDAC8, uma característica estrutural que ajuda a alcançar alta especificidade. Estudos detalhados de docking e simulações de dinâmica molecular mostraram que várias das novas moléculas — especialmente as chamadas 9m e 9r — formam interações estáveis e de longa duração dentro do bolso da HDAC8 e se ligam tão fortemente quanto, ou mais fortemente que, um inibidor de referência bem caracterizado. Importante, testes bioquímicos confirmaram que os melhores compostos bloqueiam fortemente a HDAC8 enquanto deixam outros membros da família HDAC em grande parte intocados.
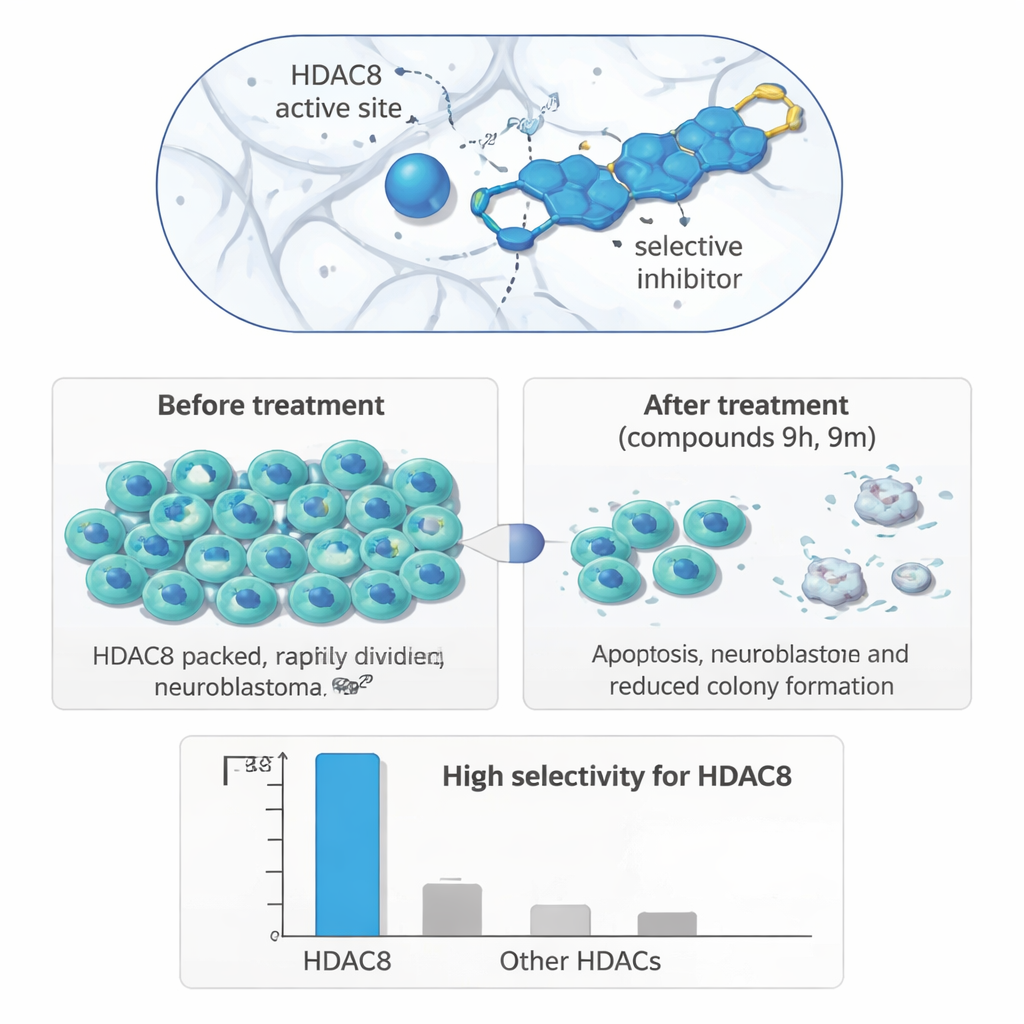
Do tubo de ensaio às células tumorais
Para verificar se esse direcionamento preciso da enzima se traduz em efeitos biológicos úteis, os pesquisadores testaram seus compostos em um painel de linhagens celulares humanas. Em células de neuroblastoma (IMR‑32), duas moléculas, 9h e 9m, se destacaram claramente: elas reduziram o crescimento celular em concentrações micromolares e fizeram isso de forma mais intensa no neuroblastoma do que em células de câncer de mama ou cólon, ou em células renais não cancerosas. Experimentos de formação de colônias a longo prazo mostraram que células de neuroblastoma tratadas perderam grande parte de sua capacidade de regeneração após a exposição ao fármaco. Em um ensaio de cicatrização de feridas, que acompanha a rapidez com que as células migram para fechar uma risca em uma camada celular, ambos os compostos retardaram o movimento das células de neuroblastoma, sugerindo redução do potencial metastático.
Investigando como os compostos matam células cancerosas
Experimentos de citometria de fluxo revelaram que 9h e 9m desencadeiam morte celular programada (apoptose) em células de neuroblastoma e causam um acúmulo de células em uma fase do ciclo celular associada a danos no DNA ou morte (Sub‑G1). Para confirmar que esses efeitos realmente decorrem do bloqueio de HDAC8, a equipe mediu o estado de acetilação de uma proteína chamada SMC3, um alvo conhecido da HDAC8 envolvido em manter as cromátides irmãs emparelhadas durante a divisão celular. Quando a HDAC8 é inibida, SMC3 acetilado se acumula. Após o tratamento com 9h ou 9m, os níveis de SMC3 acetilado aumentaram acentuadamente, enquanto a proteína SMC3 total permaneceu inalterada — forte evidência de que esses compostos atingem diretamente a HDAC8 em células vivas e perturbam sua função normal no controle cromossômico.
O que isso pode significar para tratamentos futuros
Em conjunto, a química, a modelagem computacional, os testes enzimáticos e os experimentos em células apresentam um quadro consistente: os compostos triazoloquinolina recém-desenvolvidos são bloqueadores potentes e altamente seletivos da HDAC8 que podem conter o crescimento e a disseminação de células de neuroblastoma ao mesmo tempo em que poupam outras enzimas HDAC. Por evitarem o grupo hidroxamato convencional, podem oferecer uma via mais segura para explorar a HDAC8 como alvo terapêutico. Embora muito trabalho ainda seja necessário — especialmente estudos em animais e, eventualmente, ensaios clínicos — esta pesquisa estabelece uma base sólida para o desenvolvimento de fármacos mais precisos contra o neuroblastoma infantil e possivelmente outras doenças impulsionadas pela HDAC8.
Citação: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Palavras-chave: inibidores de HDAC8, neuroblastoma, terapia epigenética, triazoloquinolina, fármacos oncológicos direcionados