Clear Sky Science · pt
O inibidor dual de G9a e antagonista do receptor de histamina H3 A-366 melhora comportamentos repetitivos e sociais e atenua a neuroinflamação em camundongos BTBR T + tf/J
Por que este estudo em camundongos é importante para o autismo
Famílias que convivem com o transtorno do espectro autista (TEA) frequentemente enfrentam um emaranhado de tratamentos que aliviam apenas alguns sintomas por vez. Este estudo explora um composto experimental novo, chamado A-366, concebido para atuar em dois sistemas biológicos muito diferentes ao mesmo tempo. Em um modelo murino amplamente utilizado de comportamento semelhante ao autismo, A-366 reduziu ações repetitivas, melhorou a interação social e acalmou a inflamação cerebral, sugerindo um futuro em que um único medicamento possa abordar várias características centrais do TEA simultaneamente.
Uma condição com muitas partes em movimento
O TEA não é uma única doença com uma causa única. Envolve dificuldades na comunicação social, comportamentos repetitivos e frequentemente outros desafios, como ansiedade ou problemas de atenção. Por trás desses sinais externos há um emaranhado de mudanças na química cerebral e na regulação gênica. Drogas atuais, como o antipsicótico aripiprazol, atuam principalmente em sistemas mensageiros cerebrais como a dopamina e a serotonina, e são aprovadas apenas para sintomas associados, como irritabilidade. Ao mesmo tempo, pesquisas revelaram que a forma como o DNA é embalado e marcado quimicamente dentro das células cerebrais — a epigenética — também muda no TEA, assim como a atividade das respostas imunes e inflamatórias do próprio cérebro. Essas múltiplas camadas sugerem que uma abordagem de “um alvo por vez” pode ser estreita demais.
Acertando tanto interruptores gênicos quanto mensageiros cerebrais
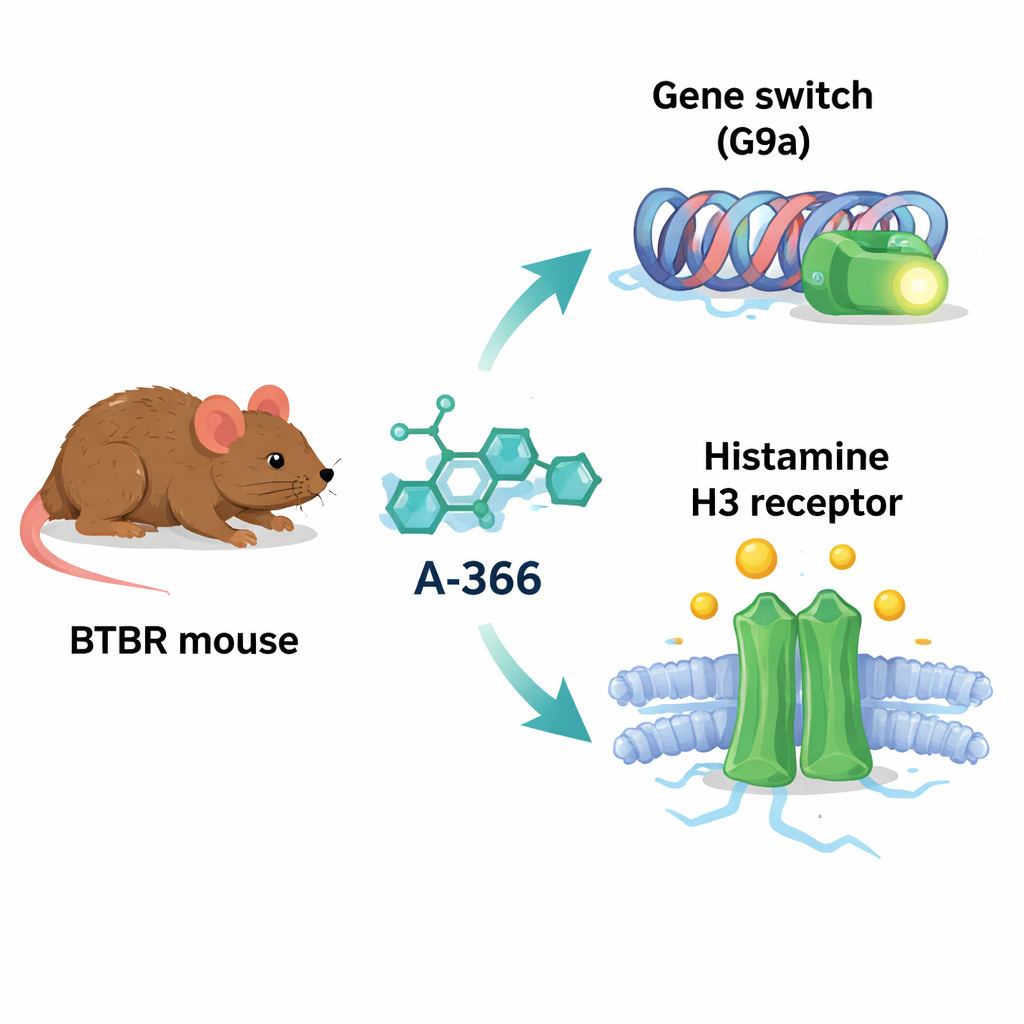
A-366 foi originalmente desenvolvida para bloquear uma proteína chamada G9a, uma enzima que adiciona marcas químicas às histonas e tende a silenciar genes. Em vários distúrbios cerebrais, a atividade da G9a e suas marcas estão aumentadas, potencialmente silenciando genes importantes para aprendizado, memória e o correto estabelecimento de circuitos cerebrais. Intrigantemente, a forma química do A-366 também se assemelha à de fármacos que bloqueiam o receptor de histamina H3, um regulador que controla a liberação de histamina e outros neurotransmissores e que tem sido ligado à atenção, ao estado de vigília e ao comportamento social. Por causa dessa sobreposição, os autores suspeitaram que A-366 poderia atuar como um “agente duplo”: aliviando o silenciamento gênico nocivo por meio da inibição de G9a e, ao mesmo tempo, potencializando a sinalização da histamina ao bloquear os receptores H3.
Testando A-366 em camundongos com comportamento semelhante ao autismo
A equipe trabalhou com camundongos BTBR T+tf/J, uma linhagem que apresenta naturalmente baixa sociabilidade, forte comportamento repetitivo de limpar-se e cavar, e inflamação cerebral elevada — características que ecoam aspectos centrais do TEA. Camundongos BTBR machos receberam injeções diárias de A-366 por três semanas em três doses diferentes, e seu comportamento foi comparado ao de camundongos típicos C57 e ao de BTBR tratados com pitolisant (um bloqueador padrão do receptor H3) ou aripiprazol. Em várias tarefas, A-366 reduziu de forma dependente da dose o ato repetitivo de cavar, rasgar e se limpar, e melhorou o desempenho no teste do labirinto em Y para memória de trabalho espacial. No teste social de três compartimentos, A-366 não apenas restaurou a preferência dos camundongos por passar tempo com outro camundongo em vez de uma gaiola vazia, como na dose mais alta elevou as pontuações sociais ao nível dos camundongos típicos, superando os efeitos do pitolisant e do aripiprazol.
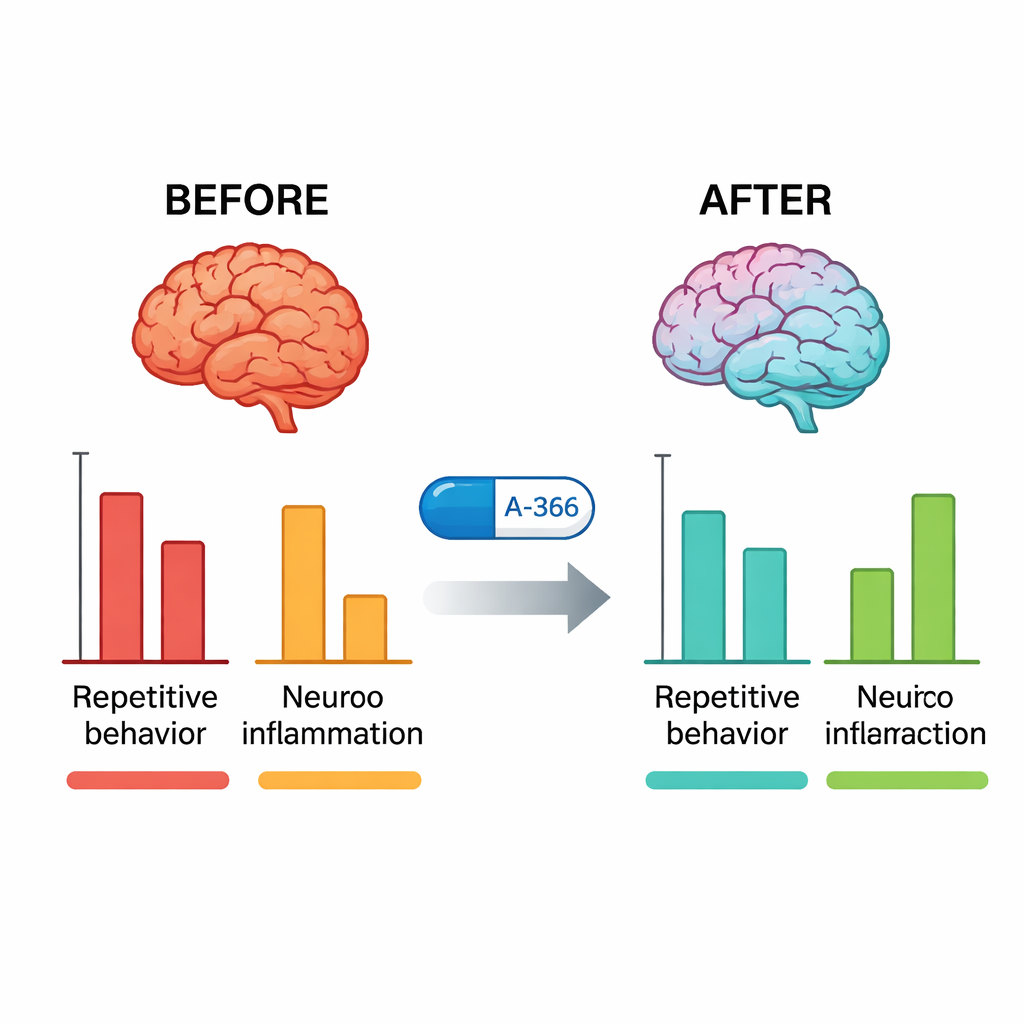
Silenciando a inflamação e confirmando os alvos
Após os testes comportamentais, os pesquisadores examinaram os cérebros dos camundongos. Em BTBR não tratados, a atividade da G9a no hipocampo e no cerebelo estava marcadamente maior do que em camundongos típicos. O tratamento com A-366 reduziu fortemente essa atividade em direção ao normal, enquanto o pitolisant isolado não o fez, confirmando que A-366 realmente atinge seu alvo epigenético. Ao mesmo tempo, moléculas inflamatórias-chave — TNF-α, IL-6 e IL-1β — estavam fortemente elevadas nos BTBR e foram significativamente reduzidas por A-366, mais do que pelo aripiprazol. Quando os cientistas adicionaram um fármaco que ativa os receptores H3 (RAMH) sobre o A-366, os benefícios comportamentais e anti-inflamatórios foram apenas parcialmente revertidos, e a queda da atividade de G9a permaneceu. Esse padrão apoia um mecanismo combinado: alívio epigenético estável por meio da inibição de G9a mais uma contribuição mediada por histamina via bloqueio do receptor H3.
O que isso pode significar para tratamentos futuros
Para um não especialista, esses achados sugerem que pode ser possível projetar medicamentos que atuem tanto no “software” quanto no “sistema de mensagens” do cérebro ao mesmo tempo. Neste modelo murino de comportamento semelhante ao autismo, A-366 reduziu ações repetitivas, melhorou o engajamento social e diminuiu sinais de inflamação cerebral crônica ao afrouxar simultaneamente desligamentos gênicos nocivos e ajustar a sinalização da histamina. O próprio A-366 foi desenvolvido para outras doenças e precisaria de otimização e extensivos testes de segurança antes de qualquer uso em pessoas. Ainda assim, ele fornece um roteiro para uma nova classe de fármacos multitarget voltada para a biologia complexa do TEA, onde abordar apenas uma via por vez até agora ofereceu alívio limitado.
Citação: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Palavras-chave: transtorno do espectro autista, terapia epigenética, receptor de histamina H3, neuroinflamação, modelo murino