Clear Sky Science · pt
aFGF resgata fibroblastos senescentes induzidos por glicose alta e melhora a cicatrização de feridas diabéticas regulando a via SIRT1/STAT3
Por que feridas de cicatrização lenta importam
Para muitas pessoas com diabetes, um pequeno corte no pé ou na perna pode evoluir para uma ferida persistente que permanece por meses, às vezes levando à infecção ou até à amputação. Essas úlceras crônicas não são apenas um problema superficial: as células da pele que deveriam reconstruir o tecido danificado muitas vezes envelhecem precocemente e deixam de funcionar adequadamente. Este estudo investiga uma maneira promissora de “rejuvenescer” algumas dessas células usando um sinal de reparo naturalmente presente, com o objetivo de ajudar as feridas diabéticas a fecharem mais rápida e completamente.
Células que envelhecem cedo demais
A pele saudável depende dos fibroblastos — células de sustentação que vivem nas camadas mais profundas da pele — para se multiplicarem, migrarem até uma ferida e depositarem uma nova matriz para o tecido. No diabetes, glicemia elevada de longa duração e moléculas danificadas pela glicose empurram esses fibroblastos para um estado chamado senescência celular. Fibroblastos senescentes já não se dividem bem, produzem menos das proteínas estruturais necessárias para a reparação e, em vez disso, liberam um coquetel de fatores que promovem irritação e alimentam a inflamação contínua. Os autores mostram que, em ratos diabéticos, a pele ao redor de uma ferida contém mais desses fibroblastos envelhecidos e menos das proteínas matriciais úteis, o que se correlaciona com cicatrização muito mais lenta.
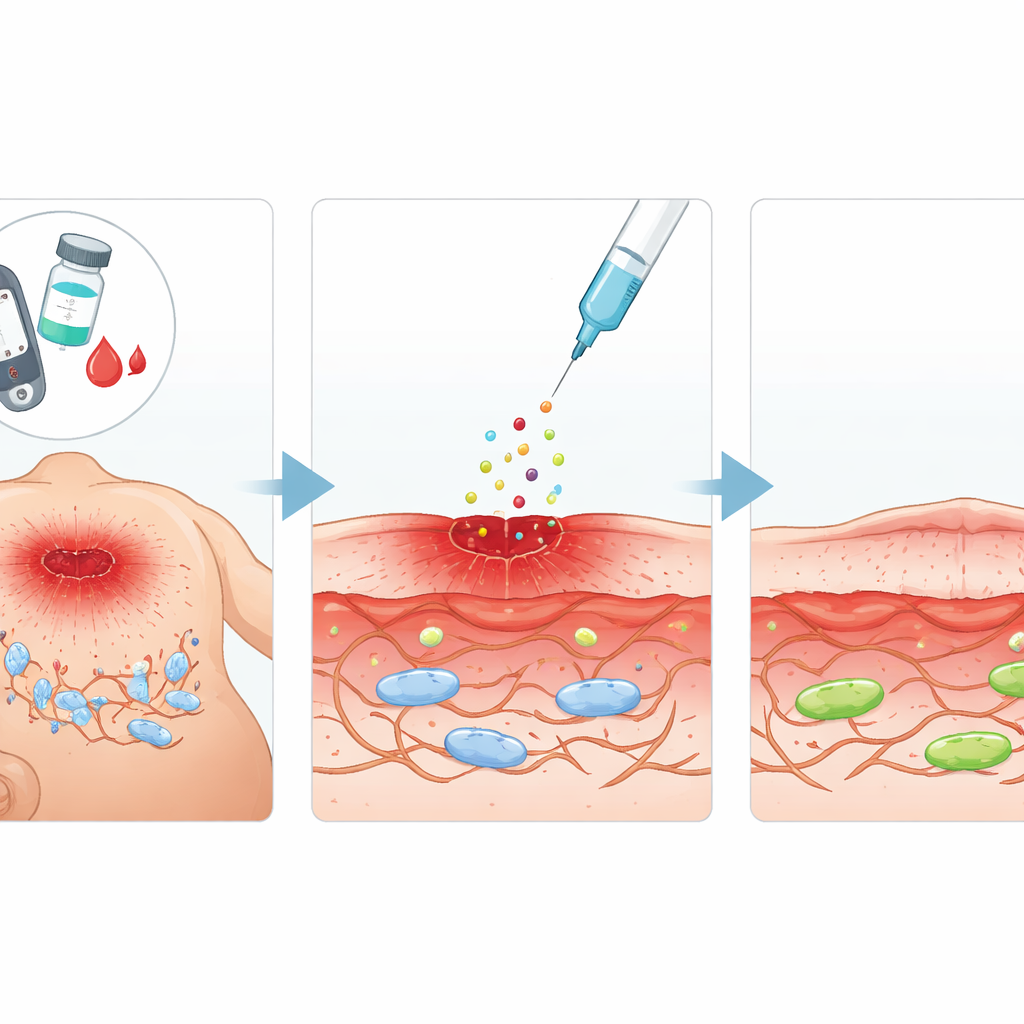
Um sinal de reparo com potencial
A equipe concentrou-se no fator de crescimento de fibroblastos ácido (aFGF), uma proteína natural conhecida por estimular o crescimento celular e a reparação tecidual. Eles investigaram se o aFGF poderia não apenas aumentar a atividade dos fibroblastos, mas também reverter as alterações semelhantes ao envelhecimento causadas pela glicose alta. Em ratos diabéticos, foram criadas feridas cutâneas padronizadas e o aFGF foi injetado ao redor da área lesionada a cada poucos dias. Em comparação com animais diabéticos não tratados, os ratos tratados com aFGF apresentaram redução mais rápida da área da ferida, melhor reconstrução do tecido subjacente e níveis mais baixos de marcadores que sinalizam senescência celular. Em experimentos paralelos em laboratório, usando uma linha celular de fibroblastos de camundongo exposta a glicose muito alta, o aFGF restaurou a capacidade das células de se dividir e migrar — dois comportamentos essenciais para o fechamento de uma ferida.
Calmando o estresse oxidativo dentro das células
A glicose alta faz mais do que apenas fornecer combustível extra às células: ela também estimula a superprodução de espécies reativas de oxigênio, moléculas instáveis que danificam proteínas, lipídios e DNA. Esse estresse oxidativo é um gatilho importante para que os fibroblastos se tornem senescentes. Os pesquisadores mensuraram vários indicadores padrão desse estresse em seu modelo celular, incluindo subprodutos danosos e a atividade das próprias enzimas antioxidantes da célula. Sob glicose alta, os fibroblastos mostraram mais dano e defesas antioxidantes mais fracas. Quando o aFGF foi adicionado, o equilíbrio mudou: os marcadores nocivos caíram e as enzimas protetoras se tornaram mais ativas. Isso sugere que o aFGF ajuda a restabelecer um ambiente interno mais saudável, tornando menos provável que os fibroblastos entrem em um estado de envelhecimento permanente.
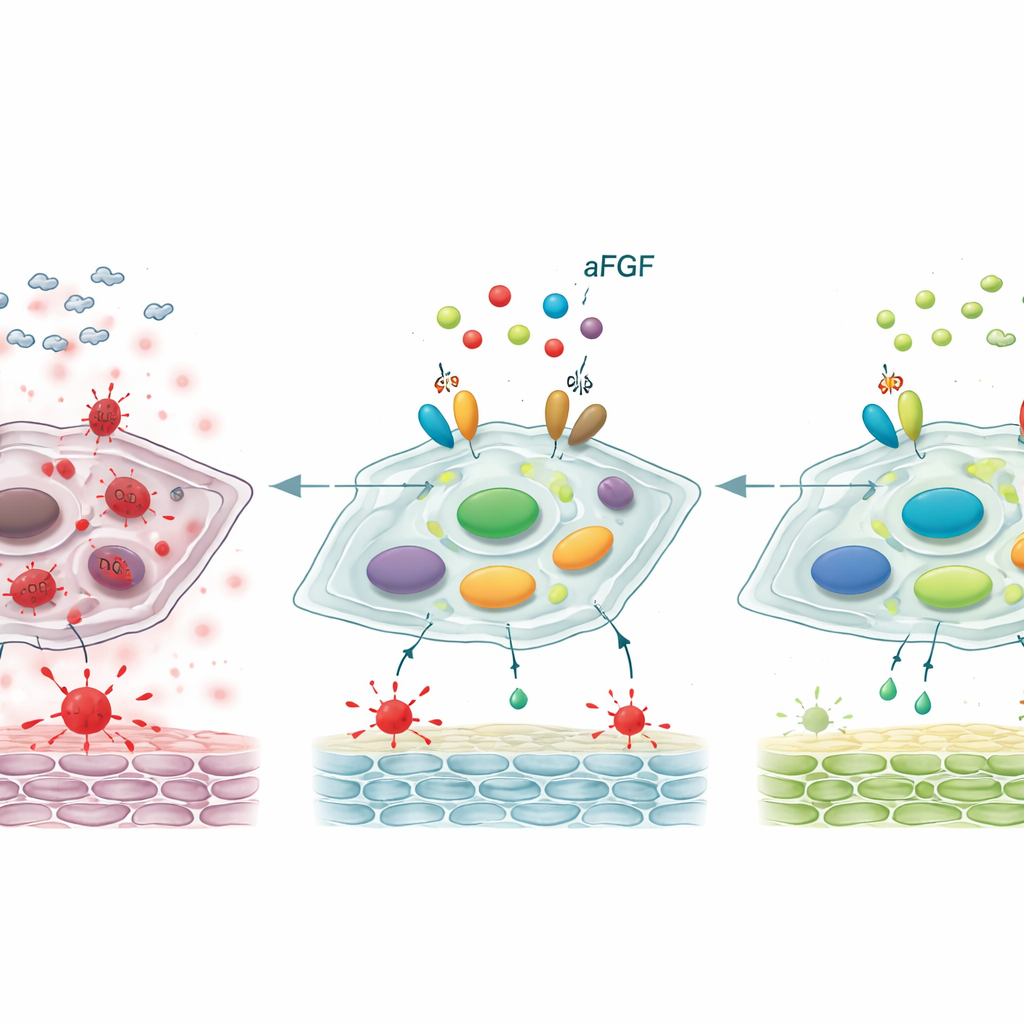
Reconfigurando um interruptor de controle chave
Aprofundando-se, os cientistas examinaram um eixo de controle molecular envolvendo duas proteínas, SIRT1 e STAT3, que conjuntamente influenciam se os fibroblastos permanecem jovens ou se tornam senescentes. Em feridas diabéticas e em células tratadas com glicose alta, os níveis de SIRT1, um guardião associado à resistência ao estresse, estavam reduzidos, enquanto a forma ativada de STAT3 — um motor de comportamento pró-envelhecimento e inflamatório — estava aumentada. O tratamento com aFGF inverteu esse padrão: SIRT1 aumentou e STAT3 ativado diminuiu. Quando a equipe bloqueou SIRT1 com um inibidor específico, o aFGF perdeu em grande parte sua capacidade de reduzir o estresse oxidativo, amortecer os marcadores de senescência e acelerar o fechamento das feridas nos ratos. Isso indica que os efeitos benéficos do aFGF dependem fortemente do reativamento de SIRT1, que por sua vez reprime o STAT3 e o programa de envelhecimento prejudicial que ele controla.
O que isso pode significar para pacientes
No conjunto, os achados sugerem que o aFGF faz mais do que simplesmente estimular o crescimento celular. Ele parece resgatar fibroblastos sobrecarregados em feridas diabéticas de um ciclo destrutivo de envelhecimento, aliviando o estresse oxidativo e reconfigurando um interruptor molecular chave para que essas células possam novamente ajudar a reconstruir o tecido. Embora o trabalho tenha sido feito em ratos e em células cultivadas, e feridas diabéticas reais sejam ainda mais complexas do que os modelos usados aqui, os resultados apontam o aFGF como um candidato promissor para tratamentos futuros. Se benefícios semelhantes forem confirmados em humanos, a terapia com aFGF cuidadosamente direcionada pode, um dia, ajudar úlceras diabéticas crônicas a cicatrizarem mais rápido, reduzindo dor, risco de infecção e a chance de complicações graves.
Citação: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Palavras-chave: cicatrização de feridas diabéticas, envelhecimento de fibroblastos, estresse oxidativo, terapia com fatores de crescimento, via SIRT1 STAT3