Clear Sky Science · pt
Segurança e eficácia preliminar da adição de tocilizumabe ao cisplatina/docetaxel para o tratamento de pacientes com câncer de mama triplo‑negativo localmente avançado: ensaio clínico prospectivo de fase 1/2
Por que este estudo importa para pacientes e famílias
O câncer de mama triplo‑negativo é uma das formas mais desafiadoras de tratar. Tende a crescer rápido, recidiva com mais frequência e não apresenta os “alvos” hormonais ou HER2 que muitos fármacos modernos utilizam. Este estudo testou se adicionar um medicamento imunomodulador chamado tocilizumabe, já usado em artrite e outras doenças inflamatórias, poderia tornar a quimioterapia padrão mais eficaz e segura para pessoas com câncer de mama triplo‑negativo localmente avançado na mama e nos linfonodos próximos.
Um câncer difícil com opções limitadas
O câncer de mama triplo‑negativo representa apenas cerca de um em cada cinco casos de câncer de mama, mas causa uma parcela desproporcional de mortes porque é agressivo e tem menos tratamentos alvo eficazes. Para muitos pacientes cujos tumores são grandes ou já atingiram linfonodos próximos, a principal opção é quimioterapia intensa administrada antes da cirurgia para reduzir o tumor. Mesmo com regimes modernos que incluem agentes de platina como cisplatina, um número significativo de pacientes permanece com tumor residual após o tratamento, o que está associado a maior risco de recidiva.
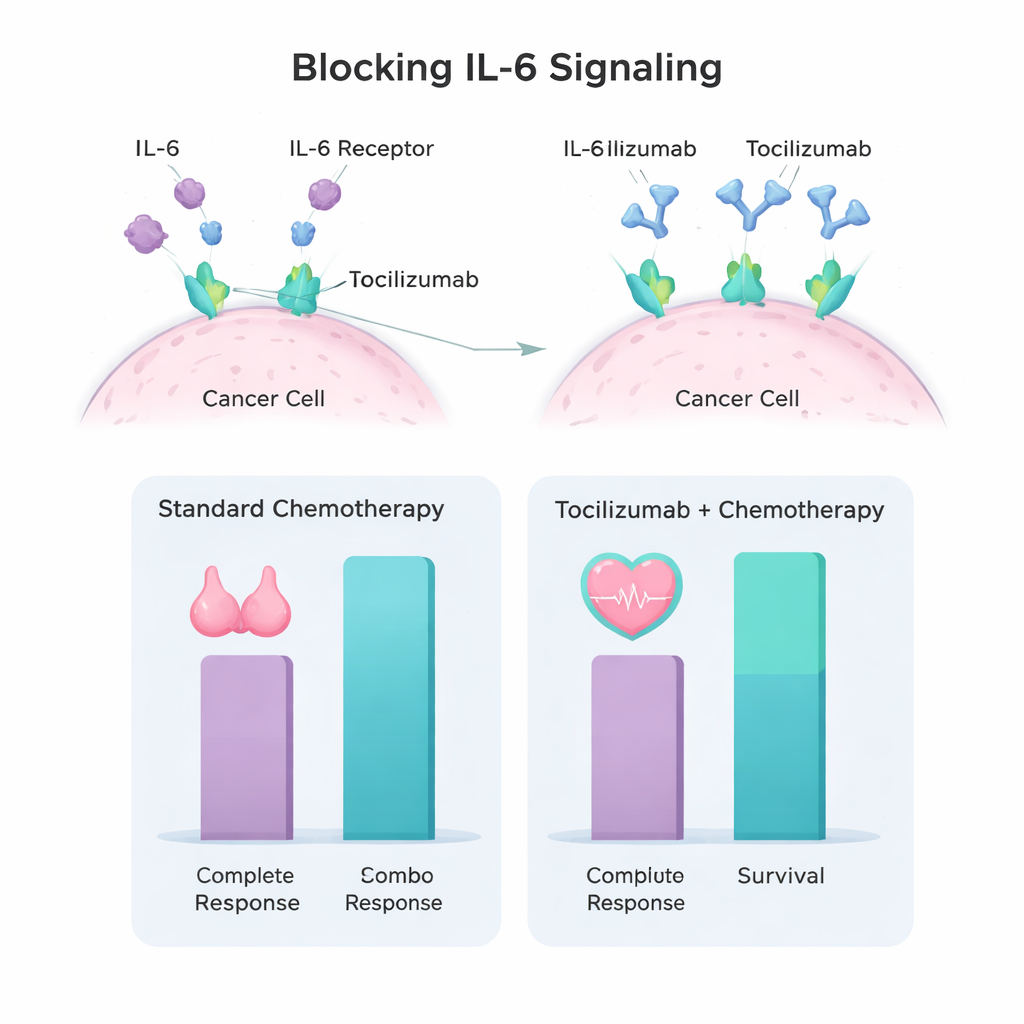
Reduzindo um sinal prejudicial
Cientistas descobriram que tumores triplo‑negativos e as células ao seu redor frequentemente produzem altos níveis de uma proteína de sinalização chamada interleucina‑6 (IL‑6). A IL‑6 funciona como uma mensagem constante de “crescer e resistir ao tratamento” para o câncer. O tocilizumabe é um anticorpo que bloqueia o receptor de IL‑6, interrompendo essa sinalização. Estudos laboratoriais e em animais do mesmo grupo de pesquisa mostraram que administrar tocilizumabe antes da cisplatina tornava as células do câncer de mama triplo‑negativo mais sensíveis à quimioterapia e retardava o crescimento tumoral. Esses achados levaram a equipe a desenhar um ensaio clínico pioneiro em humanos para avaliar se essa abordagem era segura e mostrava sinais precoces de benefício em pacientes.
Como o ensaio foi conduzido
O estudo foi um ensaio de fase 1/2, monocêntrico, em Riade, que incluiu 30 mulheres com câncer de mama triplo‑negativo localmente avançado (tamanho tumoral de pelo menos 4 cm, sem metástase à distância). Todas as pacientes receberam tocilizumabe por via intravenosa no dia 1, seguido de cisplatina e docetaxel no dia 2, a cada quatro semanas, por seis ciclos. A primeira parte do ensaio usou o desenho padrão de escalonamento de dose “3+3” para encontrar uma dose segura de quimioterapia a ser combinada com uma dose fixa de tocilizumabe. Uma vez escolhida essa dose, mais pacientes foram tratados em uma fase de expansão. Após a quimioterapia, as pacientes foram para cirurgia, e patologistas examinaram cuidadosamente o tecido mamário e os linfonodos para determinar se restava câncer invasivo. Os objetivos principais foram avaliar a segurança e medir quantas pacientes obtiveram resposta patológica completa — ou seja, ausência detectável de câncer invasivo na mama ou nos linfonodos axilares.
O que os pesquisadores encontraram
Das 30 pacientes inscritas, 28 completaram o tratamento e 26 foram submetidas à cirurgia. O grupo era relativamente jovem (mediana de idade de 42 anos), e a maioria tinha doença em estágio III e envolvimento linfonodal no início — características geralmente associadas a piores desfechos. No total, 62% das pacientes não apresentaram câncer invasivo residual após o tratamento, e 81% não tinham câncer nos linfonodos. Ao incluir respostas quase completas (pequenas manchas residuais de tumor com linfonodos limpos), 81% das pacientes enquadraram‑se na categoria de resposta completa ou quase completa, e nenhuma dessas pacientes teve recidiva durante o período de seguimento. Pacientes portadoras de mutações hereditárias BRCA1 ou BRCA2 se saíram especialmente bem: todas alcançaram resposta completa. Os resultados iniciais de sobrevida foram encorajadores, com sobrevida livre de doença estimada em três anos de 80% e sobrevida global de 90%, mesmo que muitas pacientes tivessem doença localmente muito avançada no início.
Efeitos colaterais e segurança
A segurança foi foco central porque o regime combinou um fármaco biológico com quimioterapia intensiva. Entre as 28 pacientes avaliadas, não houve mortes relacionadas ao tratamento. Os efeitos adversos mais comuns, de leves a moderados, foram náusea, dor nas articulações e músculos, vômito, diarreia, erupção cutânea e alterações temporárias nos hemogramas. Eventos mais graves incluíram neutropenia e febre, elevações das enzimas hepáticas e aumentos significativos, porém controláveis, do colesterol e dos triglicerídeos — alterações já conhecidas com o tocilizumabe e manejadas com medicações padrão. Apenas algumas pacientes necessitaram redução da dose de quimioterapia, e problemas renais relacionados à cisplatina foram raros e reversíveis, sugerindo que a combinação global foi tolerável.
O que isso pode significar adiante
Para pacientes e famílias enfrentando câncer de mama triplo‑negativo, esses resultados iniciais sugerem que adicionar um bloqueador de IL‑6 antes da quimioterapia padrão pode aumentar substancialmente as chances de que nenhum câncer seja encontrado na cirurgia, particularmente em pessoas com mutações BRCA, e pode fazê‑lo sem acrescentar efeitos colaterais perigosos. No entanto, o estudo foi pequeno, realizado em um único centro e não permitiu certos tratamentos complementares modernos para pacientes com doença residual. O tocilizumabe também foi interrompido após a cirurgia, de modo que os benefícios em longo prazo ainda precisam ser melhor definidos. Ensaios maiores e randomizados serão necessários para confirmar se essa abordagem deve fazer parte do cuidado padrão, mas este trabalho abre uma via promissora: mirar sinais inflamatórios no tumor e em seu entorno para ajudar a quimioterapia existente a agir com mais força e precisão contra um câncer de difícil tratamento.
Citação: Al-Tweigeri, T., Tulbah, A., Akhtar, S. et al. Safety and preliminary efficacy of adding tocilizumab to cisplatin/docetaxel for the treatment of locally advanced triple-negative breast cancer patients: prospective phase 1/2 clinical trial. Sci Rep 16, 7029 (2026). https://doi.org/10.1038/s41598-026-38465-z
Palavras-chave: câncer de mama triplo‑negativo, tocilizumabe, bloqueio de IL‑6, quimioterapia neoadjuvante, resposta patológica completa