Clear Sky Science · pt
Explorando os perfis de expressão gênica subjacentes aos fenótipos de diferenças no desenvolvimento sexual por meio da análise do transcriptoma
Por que esta pesquisa importa para todos nós
A maioria de nós aprende na escola que o sexo biológico é determinado de maneira simples e binária: cromossomos XX formam ovários, cromossomos XY formam testículos. Este estudo questiona essa imagem simplificada. Ao monitorar quais genes estão ativados ou desativados nas gônadas de pessoas com diferenças no desenvolvimento sexual (DSD), os pesquisadores revelam uma história mais complexa, na qual o desenvolvimento sexual humano se assemelha menos a um interruptor e mais a um espectro. O trabalho oferece uma janela sobre como os corpos se formam, por que algumas pessoas não se encaixam nas categorias típicas de masculino ou feminino e como a medicina pode compreender e cuidar melhor delas.
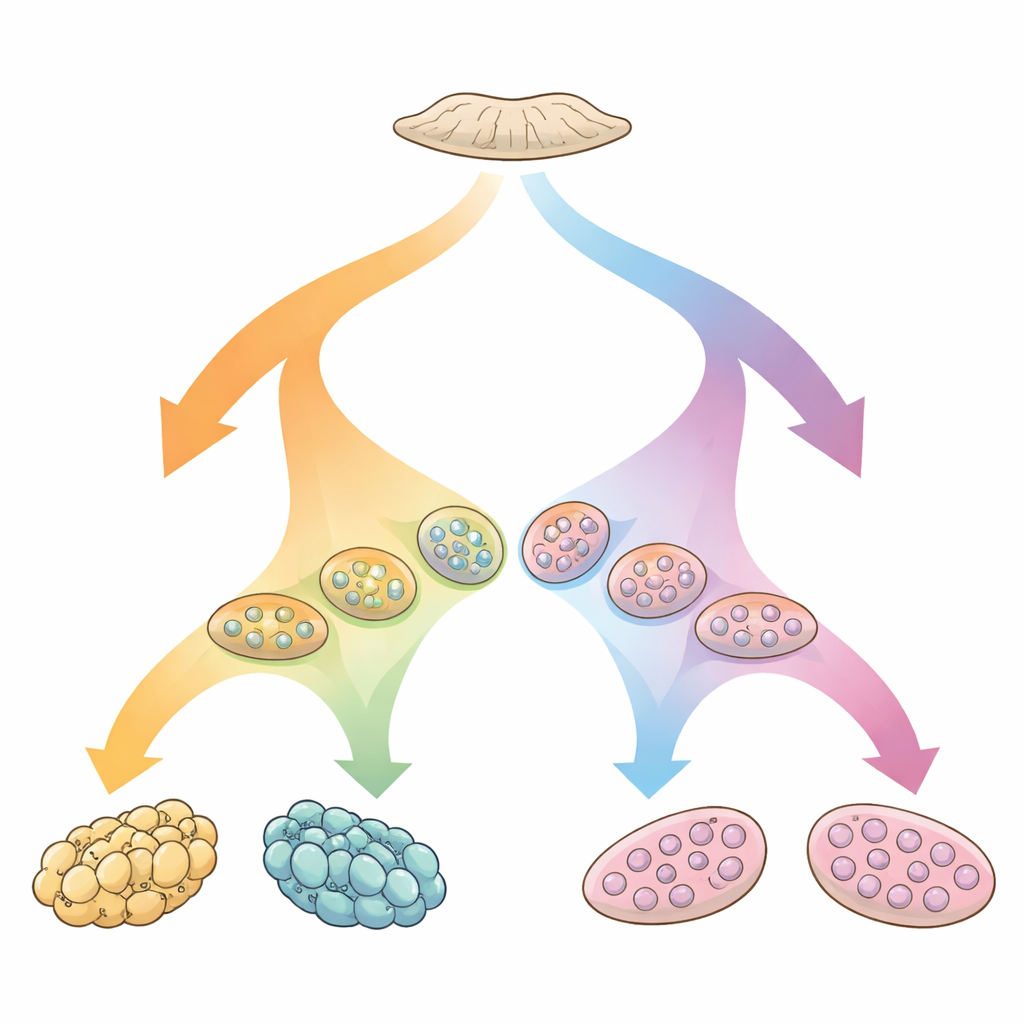
Um ponto de partida flexível na vida inicial
As gônadas começam a vida como uma estrutura flexível “bipotente” que pode se tornar testículos ou ovários. Uma rede de genes e sinais direciona esse tecido inicial para uma ou outra via, moldando eventualmente a produção hormonal e a anatomia visível. Quando qualquer parte dessa rede é perturbada, o resultado pode ser uma DSD, em que cromossomos, gônadas e anatomia não se alinham das maneiras usuais. Muitas dessas condições ainda são inexplicadas ao nível do DNA. A equipe por trás deste estudo raciocinou que observar diretamente a atividade gênica dentro do tecido gonadal poderia revelar padrões que testes genéticos clássicos deixam passar, lançando luz sobre como esses órgãos realmente escolhem — ou deixam de escolher — um caminho.
Ouvindo os genes gonadais
Os pesquisadores analisaram tecido gonadal de 11 indivíduos com diferentes condições DSD: disgenesia gonadal parcial, insensibilidade completa aos andrógenos e uma forma chamada DSD ovotesticular, em que uma pessoa apresenta tecido com características de testículo e de ovário. Usando sequenciamento de RNA, eles mediram níveis de atividade de dezenas de milhares de genes e compararam esses padrões com dados de referência de testículos e ovários saudáveis em estágios fetal, infantil e adulto. Um método de visualização que agrupa amostras por similaridade em genes-chave do desenvolvimento sexual mostrou que as amostras DSD não se encaixavam nitidamente em agrupamentos masculinos ou femininos. Em vez disso, ocupavam uma zona intermediária, formando seu próprio aglomerado entre testículos e ovários típicos. Algumas amostras ficaram mais próximas do grupo testicular, outras mais próximas do grupo ovariano, sugerindo uma gama graduada de identidades gonadais.
Sinais mistos dentro das gônadas
Quando a equipe se concentrou em genes conhecidos por direcionar as gônadas para testículo ou ovário, descobriram que esses “marcadores” frequentemente estavam fora de seus intervalos habituais. Em indivíduos 46,XY com disgenesia gonadal parcial ou insensibilidade aos andrógenos, genes necessários para o desenvolvimento testicular saudável e a produção de espermatozoides estavam diminuídos, enquanto genes envolvidos em desenvolvimentos mais amplos estavam aumentados, consistente com uma formação testicular interrompida ou incompleta. Em pessoas 46,XX com DSD ovotesticular, o quadro foi ainda mais misto: genes que normalmente promovem o desenvolvimento testicular estavam parcialmente ativados, enquanto vários genes associados ao ovário estavam reduzidos. Análises de vias em larga escala ecoaram esse padrão. Processos específicos do testículo, como formação de espermatozoides, divisão celular e metabolismo energético, estavam enfraquecidos em muitos casos 46,XY, ao passo que os casos 46,XX ovotesticulares mostraram ativação simultânea de vias relacionadas tanto ao testículo quanto ao ovário, refletindo as estruturas mistas observadas ao microscópio.
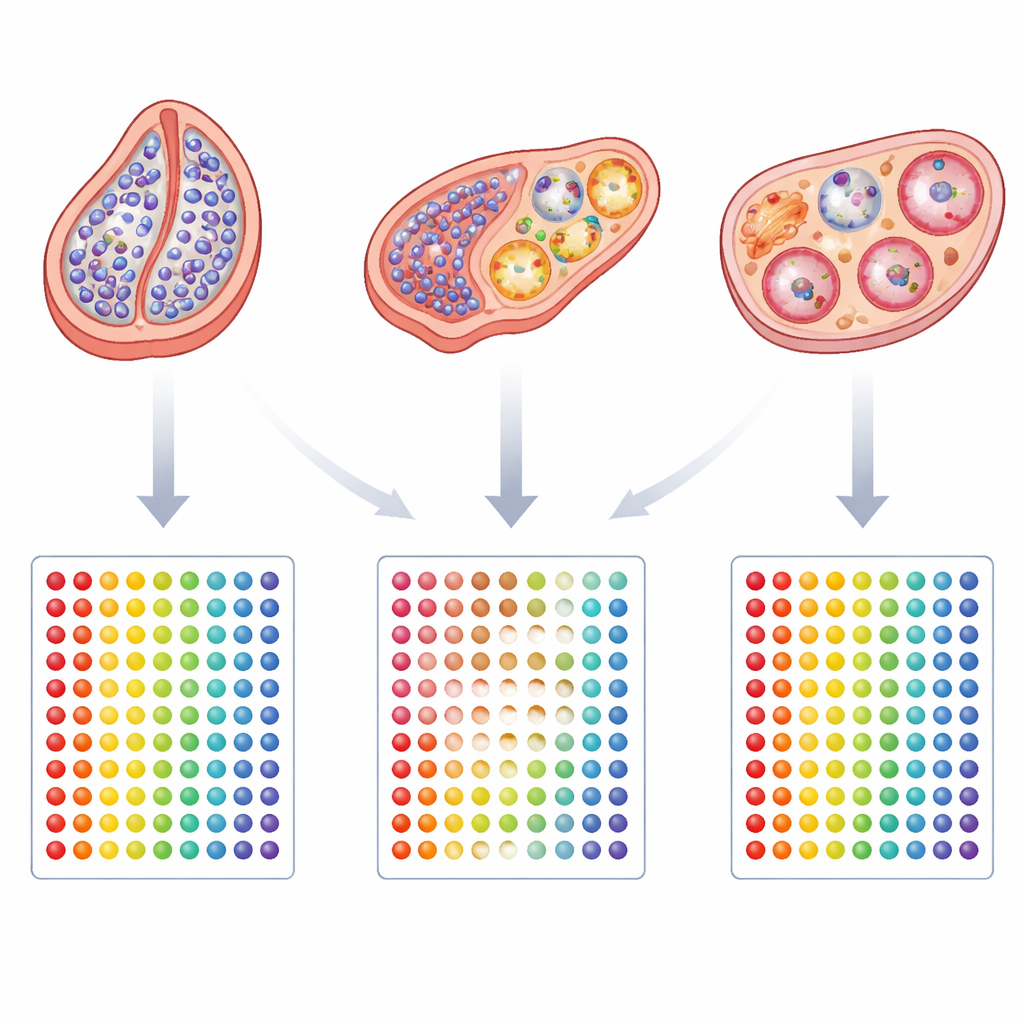
Um tema comum entre diferentes condições
Apesar da diversidade de apresentações clínicas, emergiu uma característica recorrente: redução da atividade de um gene chamado CBX2, que ajuda a organizar a forma como o DNA é empacotado e controla grandes conjuntos de genes determinantes do sexo. Experimentos em animais já haviam mostrado que a desregulação desse regulador pode borrar a fronteira entre desenvolvimento de testículo e ovário. Sua redução consistente em todos os grupos DSD sugere que instabilidade nesse nível regulatório pode favorecer que as gônadas se afastem de uma identidade claramente testicular ou ovariana e se acomodem em um ponto intermediário. O estudo também destaca que alguns pacientes mais jovens ainda mostram sinais de flexibilidade desenvolvimental, com sinais mais fortes em vias de crescimento e de células germinativas precoces do que adultos, indicando que o timing pode influenciar o quão firmemente o destino gonadal fica definido.
Repensando o interruptor simples
Para um observador leigo, esta pesquisa indica que as gônadas humanas não simplesmente alternam entre duas configurações fixas. Em vez disso, seguem um espectro de padrões de atividade gênica que podem atingir estados fortemente testiculares, fortemente ovarianos ou intermediários. Para pessoas com DSD, isso significa que o que importa biologicamente não é apenas os cromossomos que carregam ou a aparência externa do corpo, mas também como o tecido gonadal se desenvolveu ao nível molecular. Ao mapear essas paisagens internas, o estudo defende superar uma visão estritamente binária do desenvolvimento sexual e acrescentar testes baseados em RNA além do sequenciamento de DNA em trabalhos clínicos futuros. Ao fazê-lo, oferece uma compreensão mais sutil e fundamentada na biologia do sexo, que se ajusta melhor à verdadeira diversidade observada nos pacientes.
Citação: Fabbri-Scallet, H., Calonga-Solís, V., Guerra-Júnior, G. et al. Exploring the underlying gene expression profiles of differences of sex development phenotypes through transcriptome analysis. Sci Rep 16, 8801 (2026). https://doi.org/10.1038/s41598-026-38435-5
Palavras-chave: espectro do desenvolvimento sexual, transcriptoma gonadal, diferenças no desenvolvimento sexual, perfil de expressão gênica, DSD ovotesticular