Clear Sky Science · pt
Sinalização CNOT2 / c-Myc / STAT3 está criticamente envolvida na apoptose mediada por glicólise do benzil isotiocianato em carcinoma hepatocelular
Um ingrediente contra o câncer no seu prato
Benzil isotiocianato, ou BITC, é um composto natural encontrado em vegetais familiares como brócolis, repolho e couve. Embora médicos já saibam há tempos que pessoas que consomem mais desses alimentos tendem a ter taxas menores de câncer, como ingredientes específicos das plantas retardam ou matam células cancerosas ainda está sendo esclarecido. Este estudo investiga como o BITC afeta células de câncer de fígado em laboratório e revela uma ligação surpreendente entre a forma como as células cancerosas metabolizam a glicose e como são levadas à autodestruição.
Por que o câncer de fígado precisa de melhores opções
O câncer de fígado é um dos mais letais no mundo, e o carcinoma hepatocelular é sua forma mais comum. Mesmo com cirurgia, quimioterapia e medicamentos alvo, muitos tumores reaparecem ou deixam de responder ao tratamento. Uma razão é que células cancerosas reprogramam o uso de energia: em vez de dependerem principalmente do oxigênio nas mitocôndrias, elas queimam grandes quantidades de glicose muito rapidamente em um processo frequentemente chamado de “efeito Warburg”. Esse uso distorcido da glicose ajuda as células cancerosas a crescerem mais rápido e a resistirem à morte. Encontrar maneiras seguras de interromper esse suprimento de energia, especialmente usando moléculas derivadas de alimentos, é uma estratégia atraente.
Testando um composto de vegetal em células de câncer de fígado
Os pesquisadores trataram duas linhas celulares humanas de carcinoma hepatocelular, SK-Hep1 e Huh7, com doses crescentes de BITC. À medida que a dose aumentou, menos células sobreviveram, mostrando que o BITC é tóxico para células de câncer de fígado nessas condições. Ao examinarem mais de perto o que ocorria dentro das células, observaram sinais clássicos de morte celular programada, ou apoptose. Proteínas-chave que normalmente existem em forma “inativa” antes de serem clivadas durante a apoptose, como PARP e caspase-3, diminuíram em suas formas intactas, ou “pro-”. Testes por citometria de fluxo também mostraram mais células na fração sub-G1 do ciclo celular e mais células positivas para Annexina V, ambos indícios de que as células cancerosas estavam ativamente passando por apoptose em vez de simplesmente estarem danificadas.
Reprimindo o apetite por açúcar do câncer
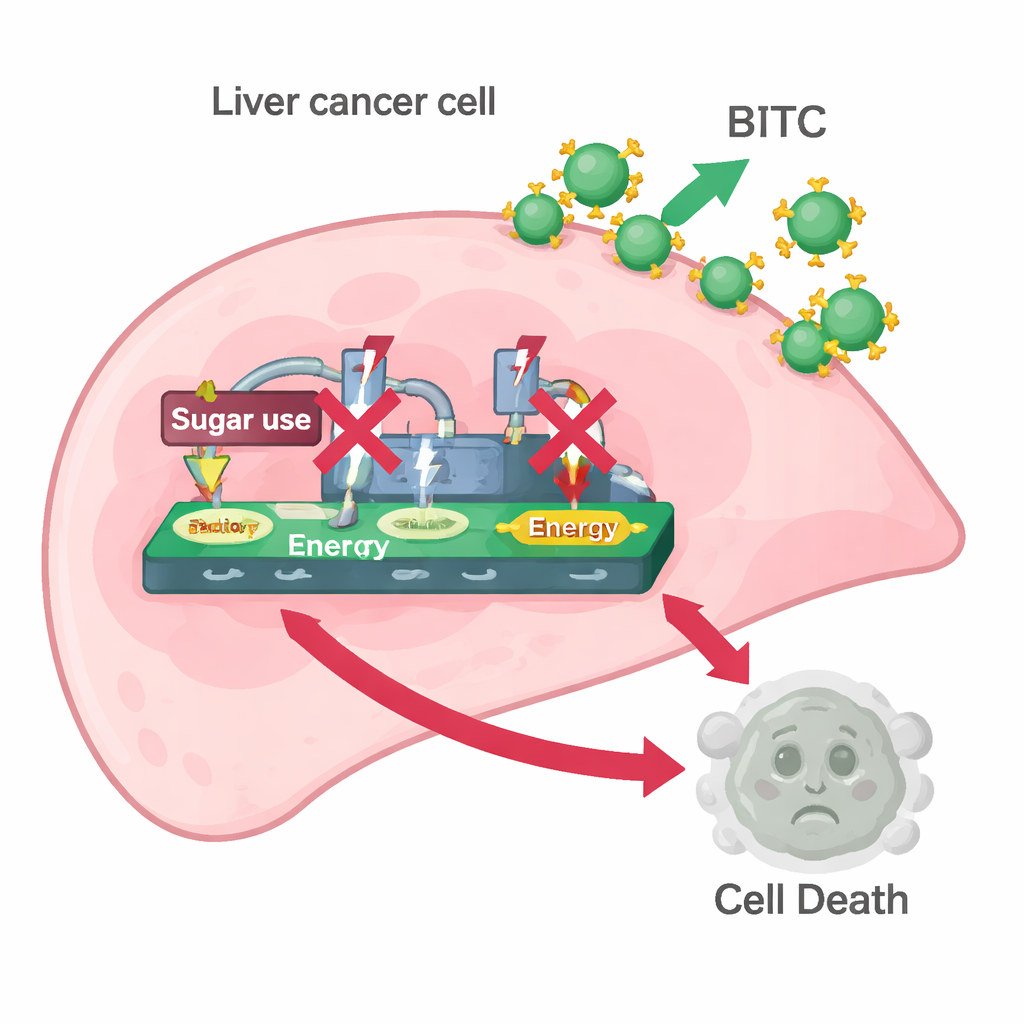
A equipe então investigou se o BITC afetava o efeito Warburg. Mediram proteínas que ajudam as células cancerosas a captar glicose e convertê-la em energia e lactato — especificamente HK2, PKM2 e LDH. O tratamento com BITC reduziu os níveis desses três em ambas as linhas celulares e diminuiu a quantidade de lactato liberado e de glicose consumida no meio de cultura. Em outras palavras, o BITC tornou as células de câncer de fígado menos capazes de operar sua máquina de queima rápida de glicose. Quando os cientistas adicionaram piruvato, um produto downstream da quebra da glicose que ainda pode alimentar o metabolismo celular, muitos dos efeitos do BITC foram revertidos: as células recuperaram níveis maiores de PARP, caspase-3 e das enzimas da glicólise. Essa resgate sugeriu que interferir no processamento da glicose é parte crucial de como o BITC desencadeia a morte celular.
Desvendando os interruptores de controle dentro da célula
Para entender camadas de controle mais profundas, os pesquisadores focaram em um trio de sinalização: CNOT2, c-Myc e STAT3. Essas proteínas ajudam a impulsionar crescimento, sobrevivência e reprogramação metabólica em muitos tumores. Dados de pacientes com câncer de fígado mostraram que CNOT2 tende a ser mais alto em pessoas com piores desfechos. Em laboratório, o tratamento com BITC reduziu a forma ativa, fosforilada, de STAT3, seu ativador a montante JAK1, a proteína promotora de crescimento c-Myc e o próprio CNOT2. O uso de ferramentas genéticas para reduzir os níveis de CNOT2 ou STAT3 fortaleceu ainda mais o efeito letal do BITC, reduzindo adicionalmente PARP e caspase-3. Experimentos de interação protéica revelaram que o BITC também interrompeu as parcerias físicas entre CNOT2 e STAT3 e entre CNOT2 e c-Myc. Quando CNOT2 ou c-Myc foram artificialmente aumentados, o BITC perdeu grande parte de sua capacidade de desligar as enzimas da glicólise e induzir apoptose, reforçando que esse eixo de sinalização atua como um interruptor mestre que liga o metabolismo da glicose à sobrevivência.
O que isso pode significar para terapias futuras
Em conjunto, os achados desenham um quadro coerente: o BITC ataca células de câncer de fígado cortando sua linha preferida de combustível à base de glicose e acionando sinais de morte celular que dependem do eixo CNOT2/c-Myc/STAT3. Ao bloquear tanto os sinais de crescimento quanto o uso de glicose, o BITC empurra as células cancerosas além de um ponto de equilíbrio metabólico rumo à apoptose. Esses resultados vêm de experimentos em cultura celular, não de pacientes, e apenas dois tipos de células de câncer de fígado foram estudados, portanto muito mais trabalho em animais e humanos é necessário. Ainda assim, a pesquisa reforça a ideia de que certos compostos de vegetais do dia a dia poderiam ser refinados ou combinados com outros tratamentos para privar tumores hepáticos com mais precisão enquanto estimulam sua autodestruição.
Citação: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Palavras-chave: câncer de fígado, benzil isotiocianato, metabolismo do câncer, apoptose, vegetais crucíferos