Clear Sky Science · pt
Modelo prognóstico baseado em aprendizado de máquina de genes relacionados à plasticidade celular e angiogênese para prever prognóstico e infiltração imune em pacientes com CHC
Por que esta pesquisa importa para pacientes com câncer de fígado
O carcinoma hepatocelular, a forma mais comum de câncer de fígado, frequentemente recorre ou se dissemina mesmo após o tratamento. Este estudo investiga por que isso ocorre e como médicos podem prever melhor quais pacientes têm maior risco. Ao combinar grandes conjuntos de dados genéticos com técnicas modernas de aprendizado de máquina, os pesquisadores construíram uma ferramenta que relaciona dois traços poderosos do câncer — a “plasticidade/stemness” (células que se comportam como sementes persistentes) e o crescimento de novos vasos — às chances de sobrevida dos pacientes e à provável resposta a terapias baseadas no sistema imune.
“Células‑semente” do câncer e novos vasos sanguíneos
Muitos tumores contêm um pequeno grupo de células que agem como sementes. Essas células‑tronco cancerígenas podem se autorrenovar, resistir ao tratamento e reiniciar o tumor após cirurgia ou quimioterapia. Ao mesmo tempo, tumores precisam formar novos vasos sanguíneos para trazer oxigênio e nutrientes e assim crescer e metastizar. Trabalhos recentes mostram que esses dois processos estão interligados: células com características de stemness liberam sinais que incentivam a angiogênese, enquanto um microambiente rico em vasos ajuda essas células‑semente a sobreviver. Entender e atingir essa parceria de forma conjunta é especialmente importante no câncer de fígado, que é altamente vascularizado e propenso à recidiva.
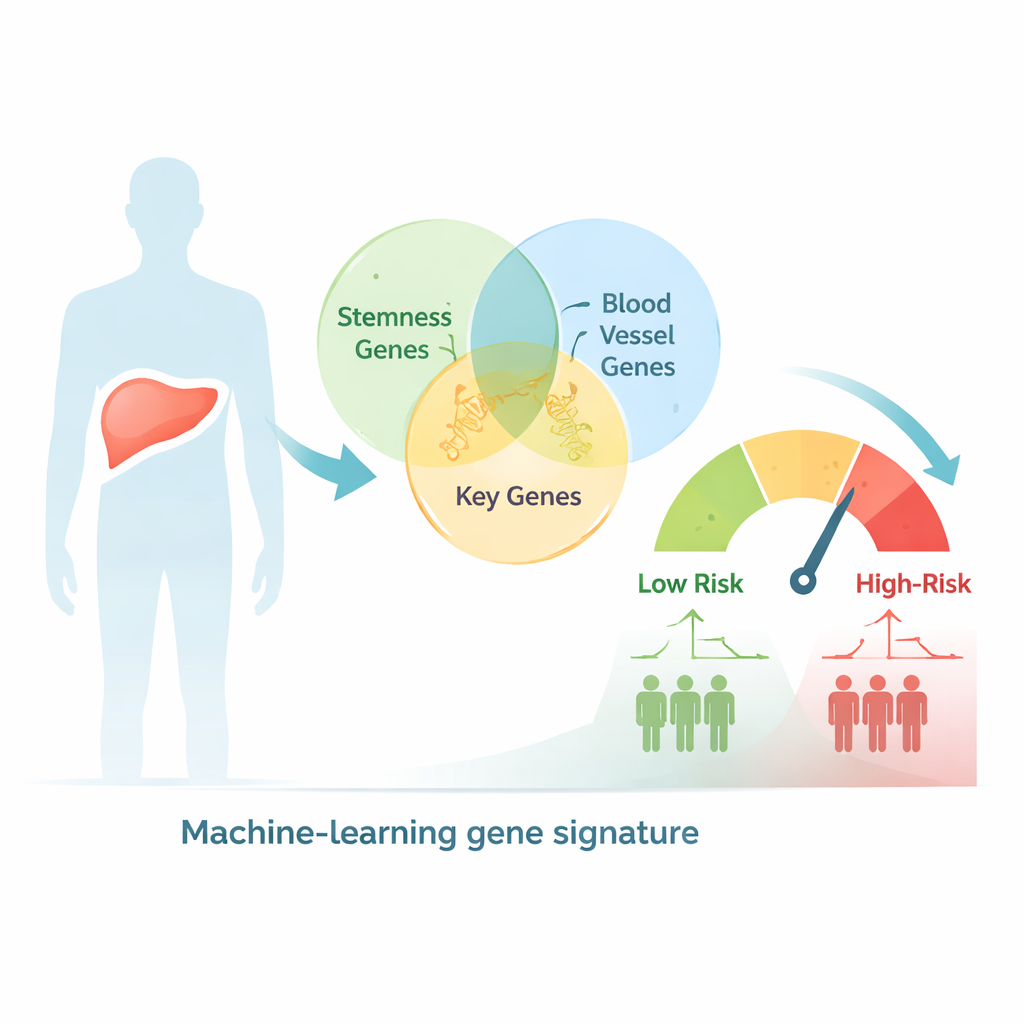
Usando big data para classificar pacientes por risco
Os pesquisadores começaram procurando em um grande banco de dados genômicos humanos genes associados tanto ao comportamento semelhante a células‑tronco quanto à formação de vasos, obtendo mais de 2.600 candidatos sobrepostos. Em seguida, examinaram amostras de carcinoma hepático de centenas de pacientes cujas atividades gênicas tumorais e desfechos clínicos estavam registradas em bases públicas. Com testes estatísticos e métodos de agrupamento, eles classificaram os pacientes em dois subtipos genéticos que mostraram diferenças claras em estágio, tamanho do tumor e sobrevida, sugerindo que os sinais combinados de stemness e angiogênese capturam biologia relevante nessa doença.
Construindo um escore de risco de nove genes
A partir desse grande conjunto de genes, a equipe usou uma abordagem de aprendizado de máquina para reduzir a lista a apenas nove genes-chave cuja atividade combinada melhor previu a duração de vida dos pacientes. Esses nove genes foram usados para calcular um escore de risco para cada pessoa. Pacientes cujos tumores apresentavam escore alto tiveram sobrevida global significativamente menor, tanto no conjunto de dados original quanto em um grupo independente de validação. A acurácia do modelo foi competitiva ou superior à de muitas ferramentas existentes e, quando o escore foi combinado com informações clínicas simples, como o estágio tumoral, em um nomograma, a previsão de sobrevida em 1, 3 e 5 anos melhorou ainda mais.
Relações com o sistema imune e resposta ao tratamento
A equipe também investigou o que o escore de nove genes revelava sobre o microambiente imune do tumor. Tumores de baixo risco tendiam a ser mais “inflamados”, com níveis maiores de várias células imunes e sinais mais fortes de vias de ataque. Tumores de alto risco, em contraste, mostraram padrões consistentes com evasão imune e maiores taxas de mutação em genes importantes como TP53. Usando ferramentas computacionais estabelecidas que estimam a provável resposta tumoral a imunoterapias modernas, o estudo sugeriu que pacientes de baixo risco poderiam responder melhor a bloqueadores de pontos de checagem imune do que pacientes de alto risco. Embora essas previsões precisem ser testadas em cenários de tratamento reais, elas apontam para uma maneira prática de identificar pacientes que poderiam se beneficiar mais desses fármacos.
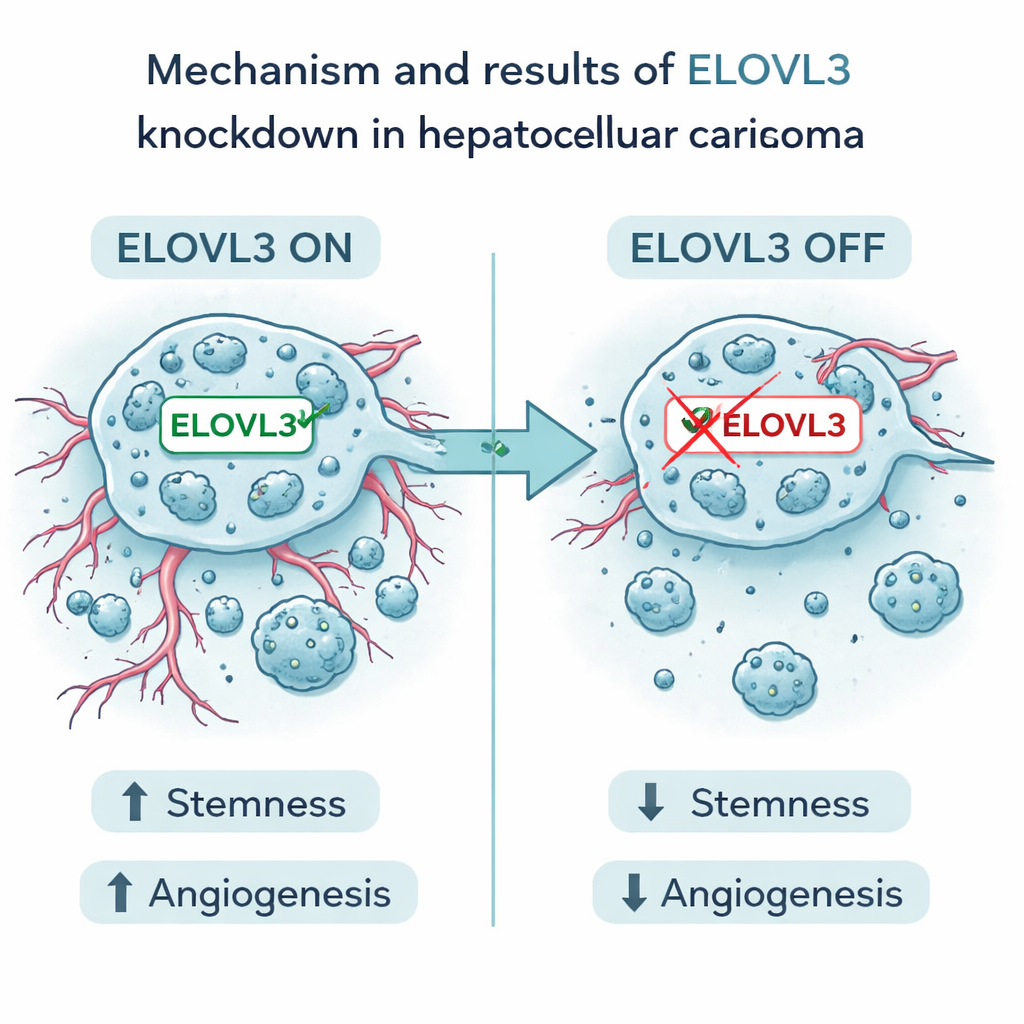
Focando em um alvo promissor
Entre os nove genes, um chamado ELOVL3 destacou‑se. Níveis altos desse gene estiveram associados a pior sobrevida. Em experimentos laboratoriais, os autores reduziram a expressão de ELOVL3 em células humanas de câncer de fígado. Isso tornou as células menos capazes de formar agregados com características de stemness e reduziu os níveis de marcadores bem conhecidos de plasticidade. Também diminuiu a produção e liberação de dois fatores principais que promovem vasos, VEGFA e FGF2. As células cancerígenas proliferaram, migraram e invadiram menos e, em modelos murinos, tumores com ELOVL3 reduzido eram menores e apresentavam menos características de doença agressiva. Esses achados sustentam a ideia de que ELOVL3 ajuda a alimentar tanto o comportamento de células‑semente do câncer de fígado quanto sua capacidade de construir vasos de suporte.
O que isso pode significar para o cuidado futuro
Em termos práticos, este trabalho transmite duas mensagens principais. Primeiro, um escore simples de nove genes obtido de amostras tumorais pode classificar pacientes com câncer de fígado em grupos de maior e menor risco e indicar como eles podem responder a tratamentos baseados no sistema imune. Segundo, um dos genes desse escore, ELOVL3, parece ocupar uma interseção entre a capacidade do câncer de se regenerar e de promover angiogênese, tornando‑o um alvo atraente para futuras terapias. Embora o modelo e o alvo precisem de confirmação em ensaios clínicos prospectivos, eles abrem a porta para um cuidado mais personalizado do câncer de fígado e para estratégias combinadas que bloqueiem tanto as “células‑semente” do câncer quanto seu suprimento sanguíneo.
Citação: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Palavras-chave: carcinoma hepatocelular, células‑tronco cancerígenas, angiogênese, assinatura gênica prognóstica, ELOVL3