Clear Sky Science · pt
Variabilidade de genes de referência por idade e sexo em camundongos 5XFAD destaca desafios de normalização em modelos de Alzheimer
Por que este estudo em camundongos importa para a pesquisa sobre Alzheimer
Quando cientistas procuram sinais precoces ou efeitos de tratamentos na doença de Alzheimer, frequentemente medem o quanto diferentes genes estão ativados ou desativados no cérebro. Mas, para saber se um gene realmente mudou, eles precisam primeiro de uma "régua" estável para comparação: genes de referência que se supõe permanecer constantes. Este artigo mostra que, em um modelo de camundongo de progressão rápida da doença de Alzheimer, esses genes supostamente estáveis não são tão estáveis quanto muitos pesquisadores assumem — especialmente entre idades diferentes, regiões cerebrais e entre machos e fêmeas.
Como os cientistas leem a atividade genética do cérebro
A pesquisa cerebral moderna frequentemente depende de uma técnica chamada RT-qPCR, que conta quanto da mensagem de um dado gene está presente em uma amostra de tecido. Como as amostras nunca contêm exatamente a mesma quantidade total de material, os cientistas normalizam suas medidas por um ou mais genes de referência, muitas vezes chamados de genes "housekeeping", que se espera serem constantes entre as condições. Na prática, no entanto, doenças como Alzheimer alteram dramaticamente tipos celulares, metabolismo e inflamação no cérebro, o que pode deslocar silenciosamente os níveis desses genes de referência. Se a referência em si muda, qualquer medida baseada nela pode ser enganosa, exagerando ou ocultando mudanças biológicas reais.
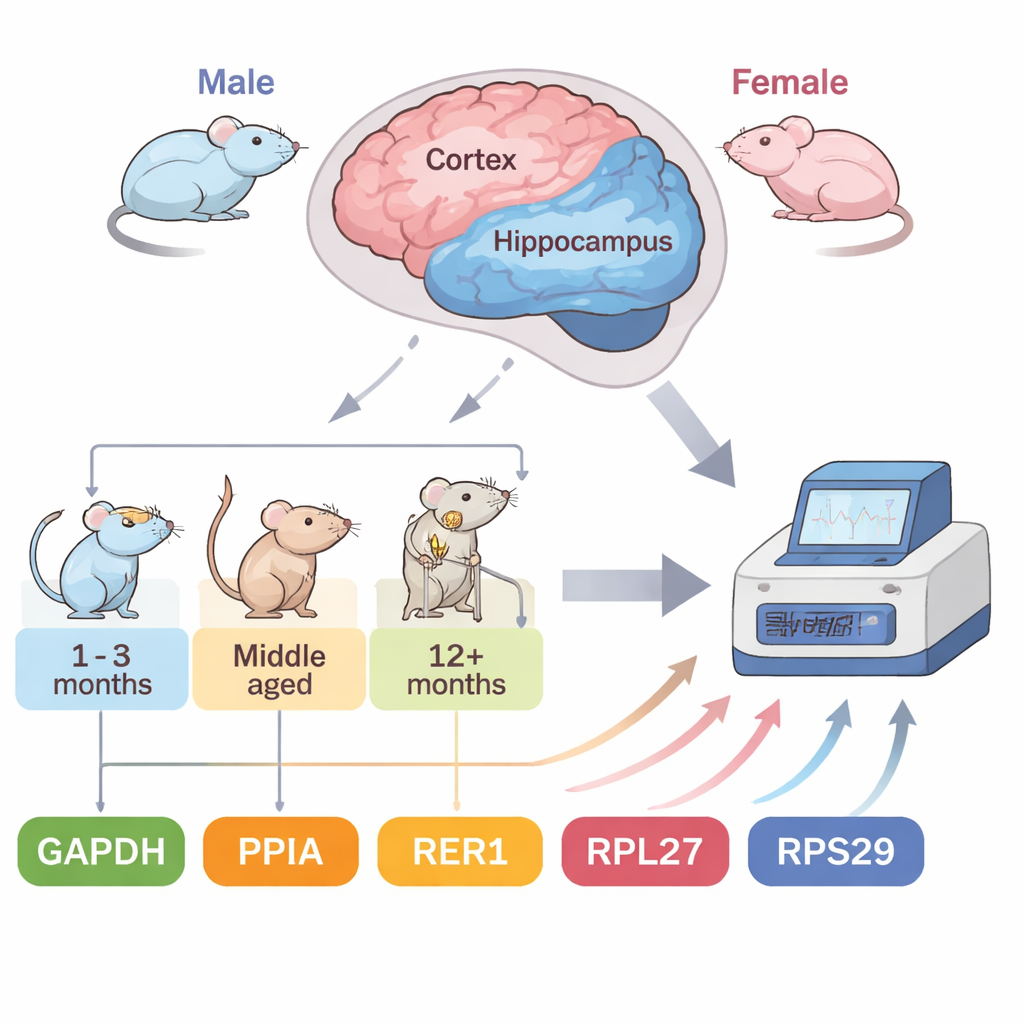
Um modelo de camundongo em via rápida para Alzheimer
A equipe focou nos camundongos 5XFAD, um modelo amplamente usado que carrega cinco mutações humanas associadas à forma familiar da doença de Alzheimer. Esses animais desenvolvem placas amiloides — aglomerados proteicos que são uma marca da doença — notavelmente cedo: por volta de dois meses de idade, com acúmulo intenso de placas aos quatro a cinco meses. Essa linha do tempo acelerada permite que pesquisadores acompanhem mudanças relacionadas à doença ao longo de meses em vez de anos. Os autores examinaram duas regiões cerebrais vulneráveis, o córtex e o hipocampo, em machos e fêmeas de quatro estágios: inicial (2 meses), em desenvolvimento (4 meses) e mais avançado (7 e 10 meses). Testaram cinco genes de referência comuns e usaram quatro ferramentas estatísticas independentes para ranquear quão estável cada um se comportou sob essas condições variáveis.
Genes de referência não servem para todas as situações
Os resultados mostram que nenhum gene único permaneceu perfeitamente estável em todos os contextos. Em vez disso, a estabilidade dependeu de onde a amostra do cérebro foi coletada, se o camundongo era macho ou fêmea e de quão avançada estava a doença. Alguns genes, como Gapdh — um clássico amplamente usado em muitos estudos — tiveram desempenho relativamente bom em vários cenários, especialmente no córtex em idades mais precoces, mas mostraram mais variabilidade em estágios posteriores ou em certas amostras do hipocampo. Outros candidatos, como Rps29, Ppia, Rpl27 e Rer1, surgiram como melhores pares em combinações específicas, e esses "melhores pares" mudaram com a idade e o sexo. No geral, o córtex tende a mostrar mais variabilidade que o hipocampo, e estágios mais avançados da doença, particularmente em camundongos machos, prejudicaram a estabilidade suposta de vários genes de referência.
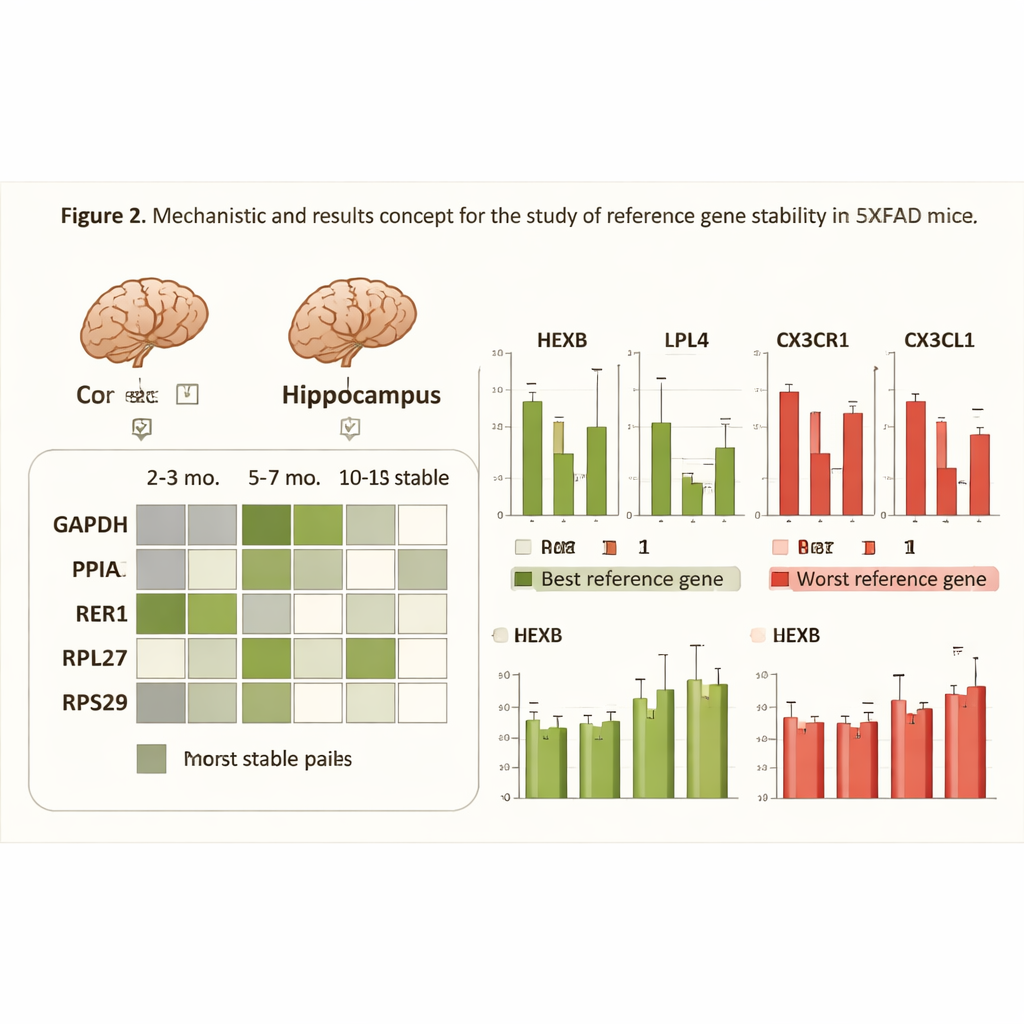
O que acontece quando a régua se curva
Para demonstrar por que a escolha cuidadosa de genes de referência importa, os pesquisadores analisaram quatro genes cerebrais envolvidos em inflamação, metabolismo e sinalização imune — processos fortemente implicados na doença de Alzheimer. Compararam como as mudanças aparentes nesses genes-alvo diferiam quando normalizadas com o par de referência mais estável, com o gene único menos estável ou com todos os cinco genes juntos. Quando genes de referência inadequados foram usados, os dados ficaram mais ruidosos e algumas mudanças biologicamente significativas pareceram mais fracas ou até não significativas estatisticamente. Em contraste, usar o par melhor ajustado para cada condição reduziu a dispersão nas medidas e fortaleceu a detecção de diferenças reais entre camundongos saudáveis e doentes, especialmente em estágios mais avançados da patologia.
Sinais mais claros para uma doença complexa
Para não especialistas, a conclusão é direta: até as réguas básicas usadas em estudos gênicos podem se deformar sob a pressão de uma doença cerebral que muda rapidamente, como o Alzheimer. Este trabalho oferece um guia prático para escolher melhores genes de referência em um modelo de camundongo importante e ressalta que os pesquisadores devem validar suas "réguas" para cada região do cérebro, idade e sexo estudados. Ao fazer isso, os cientistas podem obter leituras mais claras e confiáveis de quais genes realmente mudam durante a degeneração semelhante ao Alzheimer — um passo essencial para entender os mecanismos da doença e avaliar possíveis tratamentos.
Citação: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Palavras-chave: Doença de Alzheimer, expressão gênica, camundongos 5XFAD, genes de referência, RT-qPCR