Clear Sky Science · pt
DGCR8 regula múltiplos processos do reparo por excisão de nucleotídeos acoplado à transcrição
Como a luz solar se comunica com nossos genes
Cada vez que nos expomos ao sol, raios ultravioleta (UV) invisíveis atingem a pele e danificam o DNA das nossas células. Na maior parte das vezes, as células consertam silenciosamente esses danos antes que causem problemas. Este estudo revela um participante inesperado nesse sistema de proteção: uma proteína chamada DGCR8, conhecida anteriormente por ajudar a produzir microRNAs. Os pesquisadores mostram que o DGCR8 pode mudar de função após a exposição a UV, coordenando várias etapas de uma via-chave de reparo do DNA que ajuda a prevenir câncer e outras doenças.
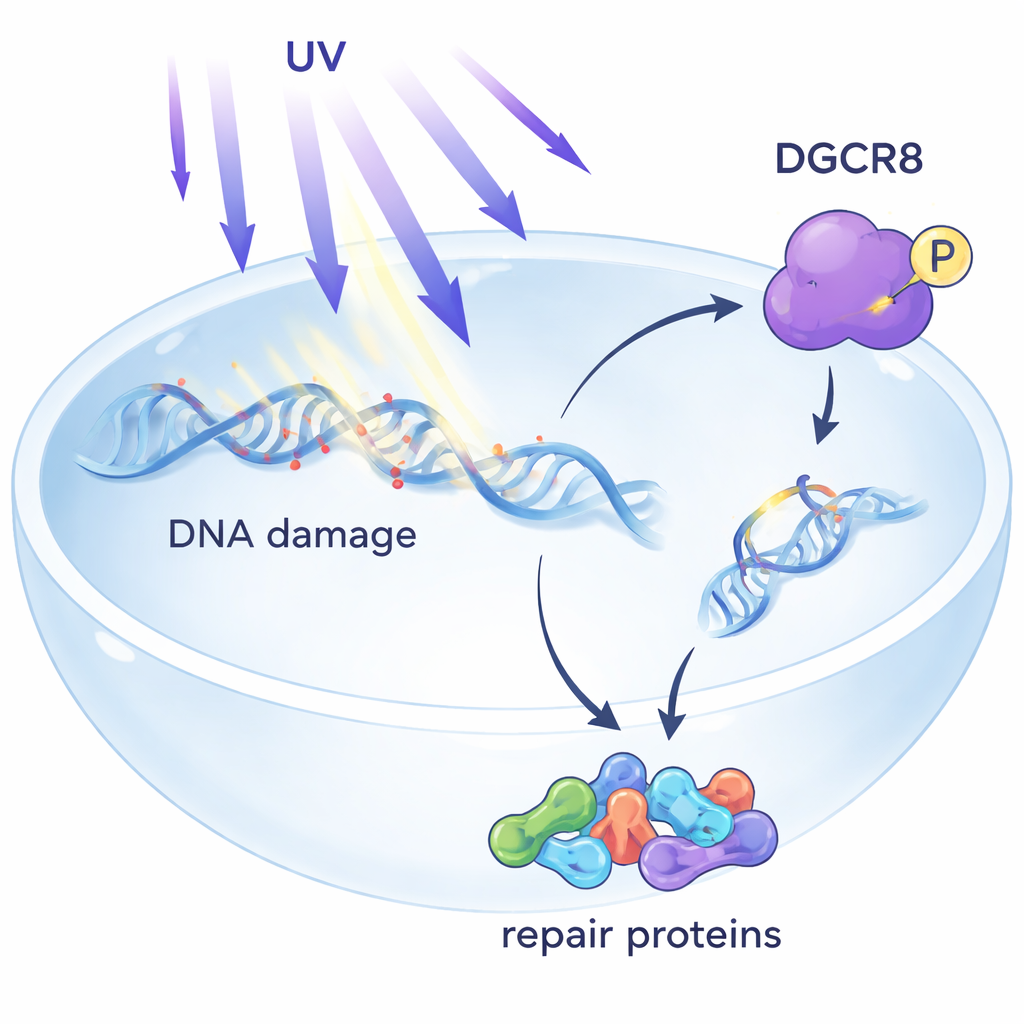
Um guardião oculto dentro do reparo do DNA
A luz UV cria pequenas lesões no DNA que podem bloquear as máquinas moleculares que leem os genes. Uma das principais defesas do organismo é o reparo por excisão de nucleotídeos acoplado à transcrição, ou TC-NER, que se concentra em danos que paralisam as enzimas leitoras de genes. Até agora, o DGCR8 era conhecido principalmente por processar microRNAs, pequenas moléculas de RNA que ajustam a atividade gênica. Trabalhos anteriores sugeriam que o DGCR8 também protegia as células contra UV, mas o mecanismo era obscuro. Este artigo mostra que, após exposição a UV, o DGCR8 se associa fisicamente a fatores centrais do TC-NER, agindo como um organizador que reúne componentes de reparo exatamente onde a leitura genética é bloqueada.
Um interruptor molecular liga/desliga para o DGCR8
A chave para o novo papel do DGCR8 é uma única marca química em um de seus blocos estruturais, o aminoácido serina na posição 153. Quando esse sítio é fosforilado — ou seja, quando um grupo fosfato é adicionado — o DGCR8 adquire a capacidade de se ligar a elementos centrais do TC-NER, incluindo a RNA polimerase II (a enzima que lê genes) e fatores de reparo chamados CSB, CSA e UVSSA. Células engenheiradas com uma versão do DGCR8 que não pode ser fosforilada nesse sítio (o mutante S153A) mostraram interações fracas ou perdidas entre essas proteínas de reparo, e a montagem normal do complexo de reparo desencadeada por UV falhou. Uma versão “fosfomimética” que se comporta como se estivesse sempre fosforilada teve o efeito oposto, fortalecendo interações-chave mesmo sem UV. Esses resultados indicam que a fosforilação em Ser153 funciona como um interruptor liga/desliga que converte o DGCR8 de seu papel usual no processamento de RNA para um coordenador do reparo do DNA.
Desembaraçando nós perigosos de DNA–RNA
Além de reunir proteínas de reparo, o DGCR8 também ajuda a gerenciar estruturas chamadas R-loops — trechos curtos onde o RNA recém-sintetizado se reassocia ao DNA de origem, formando um híbrido DNA–RNA. Em pequenas quantidades, R-loops podem ser úteis, mas quando se acumulam após exposição a UV podem impedir a cópia do DNA e desestabilizar cromossomos. Usando anticorpos especializados e sondas fluorescentes, os autores descobriram que células sem DGCR8, ou que carregam a forma não fosforilável S153A, acumulam muito mais R-loops após UV. O DGCR8 fosforilado foi observado nessas estruturas híbridas, especialmente onde elas se sobrepunham a lesões induzidas por UV, sugerindo que ele ajuda a prevenir ou eliminar R-loops nocivos precisamente em genes ativos sob estresse.
Controlando a cópia do DNA
Quando danos ao DNA ou R-loops atrapalham a cópia do genoma, as células normalmente desaceleram a replicação por meio de um circuito de segurança conhecido como ponto de verificação ATR–CHK1. Experimentos de rastreamento de fibras mostraram que células com DGCR8 normal reduziram suas trilhas de replicação após a exposição a UV, refletindo um ponto de verificação ativado. Em contraste marcante, células sem DGCR8 ou com a mutação S153A continuaram replicando em velocidade quase normal, mesmo tendo acumulado danos no DNA e R-loops. Testes adicionais revelaram que, embora o ATR em si fosse ativado, seu parceiro-chave CHK1 foi pouco ativado nessas células mutantes. Isso indica que o DGCR8 fosforilado ajuda a transmitir o sinal de estresse proveniente do DNA danificado e dos R-loops para o CHK1, permitindo que a célula pause e estabilize a replicação.
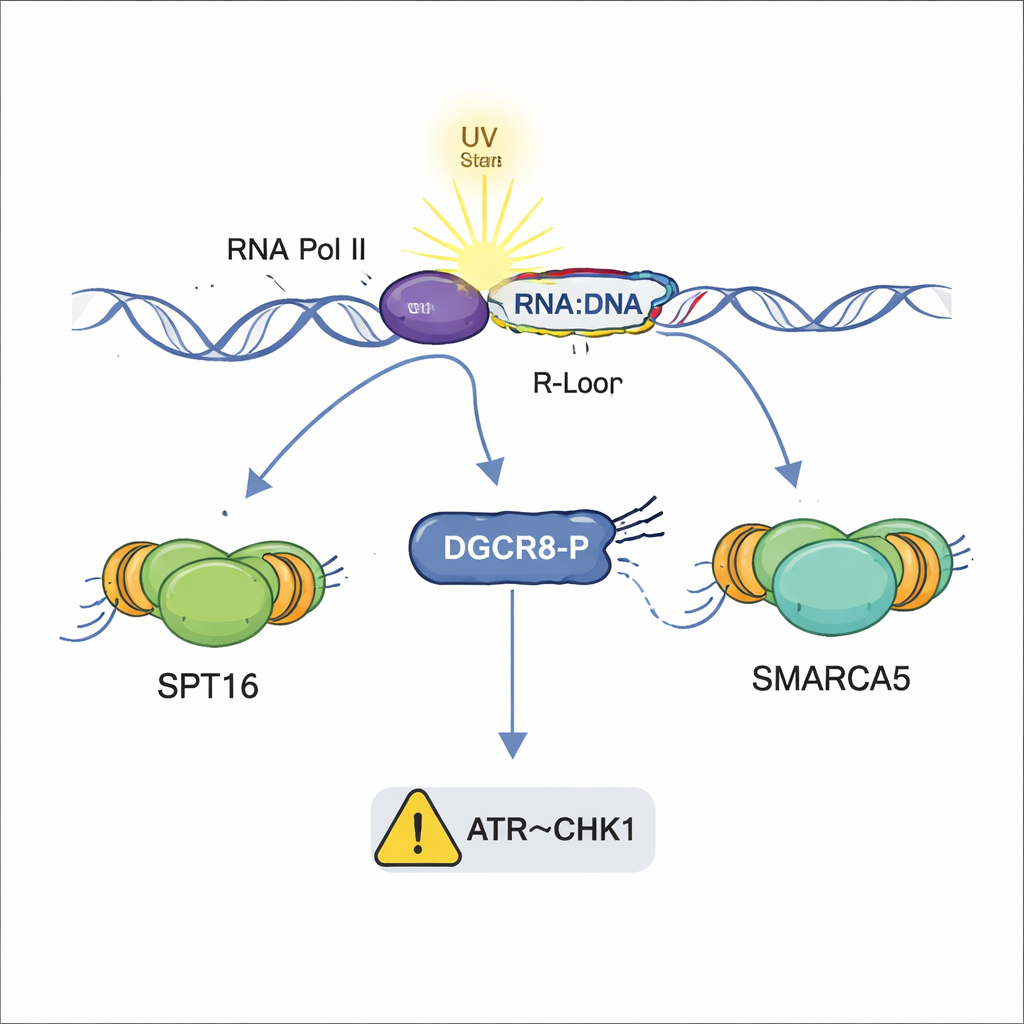
Por que isso importa para a saúde e a doença
Em conjunto, os achados revelam o DGCR8 como um guardião multitalentoso que coordena várias camadas da resposta ao dano por UV: montar a equipe de reparo do TC-NER, recrutar remodeladores de cromatina que abrem o DNA, conter híbridos DNA–RNA nocivos e ajudar a desencadear a desaceleração da replicação por meio da via ATR–CHK1. De forma crucial, essas ações são separadas do trabalho tradicional do DGCR8 na biogênese de microRNAs e dependem da fosforilação de um único sítio. Como falhas no reparo do DNA e no controle de R-loops estão ligadas ao câncer e a doenças neurológicas, e mutações em DGCR8 foram encontradas em alguns tumores, compreender esse interruptor molecular pode abrir novas vias para diagnosticar ou tratar condições impulsionadas por danos por UV e instabilidade genômica.
Citação: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Palavras-chave: Lesão de DNA por UV, DGCR8, Reparo de DNA, R-loops, Estabilidade do genoma