Clear Sky Science · pt
PARP-1 conecta a sinalização β-catenina/TCF4 à transição epitélio–mesênquima na endometriose
Por que esta pesquisa importa para a saúde da mulher
A endometriose é uma condição dolorosa na qual tecido semelhante ao revestimento do útero cresce em locais inadequados, como os ovários. Esses fragmentos deslocados podem invadir estruturas vizinhas, causar cicatrizes e contribuir para a infertilidade; ainda assim, os tratamentos atuais costumam ser imperfeitos e os sintomas frequentemente retornam. Este estudo investiga um “interruptor” molecular chamado PARP‑1 e pergunta se ele ajuda as lesões da endometriose a se tornarem mais invasivas — e se fármacos já existentes que bloqueiam o PARP‑1 poderiam reduzir suavemente essa ativação.
Uma análise mais detalhada do comportamento de lesões invasivas
Embora a endometriose seja classificada como uma doença benigna, o tecido ectópico (deslocado) muitas vezes se comporta de maneira surpreendentemente agressiva: migra, implanta e persiste de forma semelhante a um câncer de crescimento lento. Um processo central por trás desse comportamento é a transição epitélio–mesênquima, ou TEM (EMT, na sigla em inglês), em que células organizadas em camadas perdem suas conexões e adotam uma identidade mais móvel e fibrótica. Os autores examinaram tecido de mulheres com e sem endometriose e descobriram que as lesões endometrióticas ovarianas exibiam um padrão claro semelhante à TEM: a proteína «cola» E‑cadherina estava reduzida, enquanto marcadores de células mais móveis, como N‑cadherina e vimentina, estavam aumentados. Ao mesmo tempo, os níveis de PARP‑1 e de componentes de uma via de controle do crescimento conhecida como Wnt/β‑catenina eram mais altos nessas lesões, sugerindo que todas essas mudanças ocorrem de forma correlacionada.
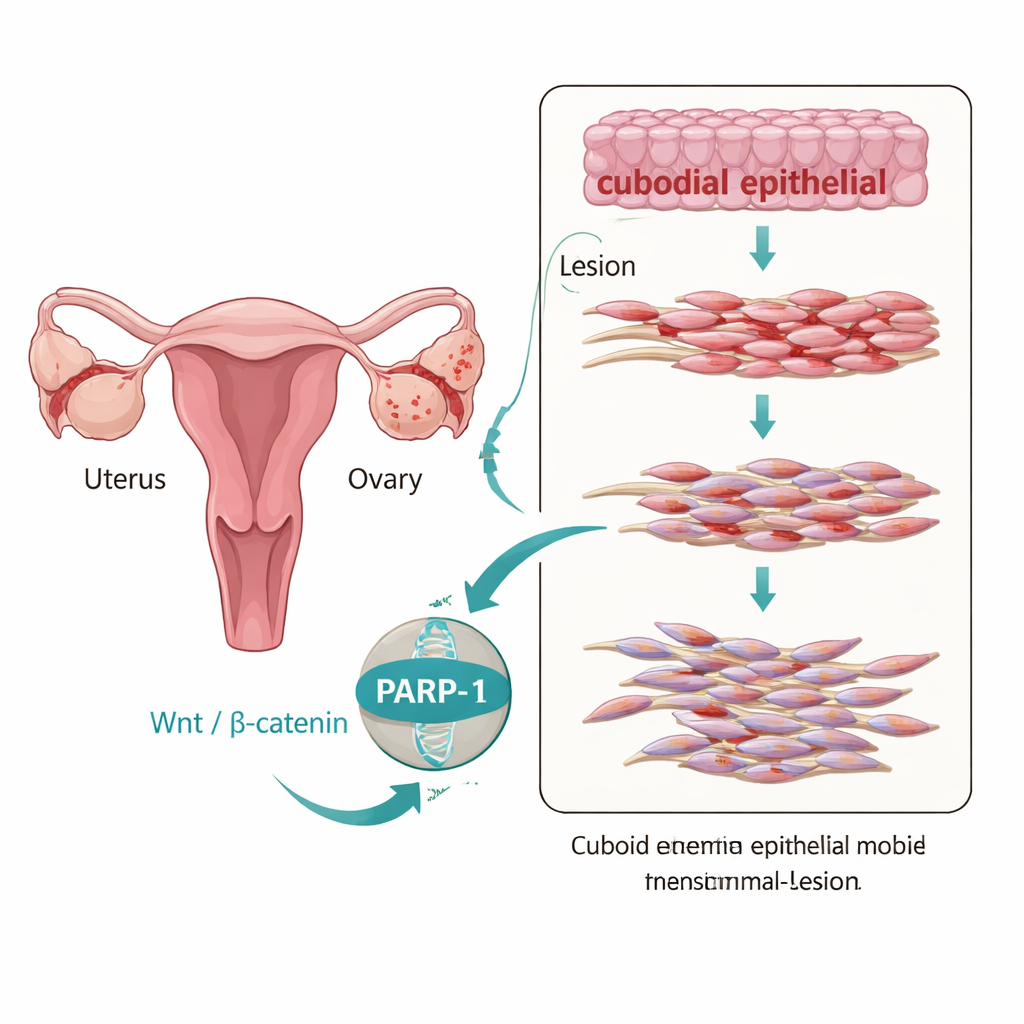
A ponte molecular entre sinais e mudança celular
Para descobrir se o PARP‑1 está apenas presente ou se realmente dirige essas mudanças, os pesquisadores usaram uma linhagem imortalizada de células epiteliais endometrióticas chamada 12Z. Quando aumentaram artificialmente os níveis de PARP‑1 nessas células, os marcadores de TEM mudaram para um perfil mais invasivo e as células ficaram mais móveis e viáveis em testes de laboratório que simulam cicatrização e invasão tecidual. Quando reduziram o PARP‑1 com moléculas de RNA direcionadas, o padrão se inverteu: a E‑cadherina aumentou, os marcadores mesenquimais caíram e as células moveram‑se e proliferaram menos. Importante, o PARP‑1 associou‑se fisicamente à β‑catenina e à TCF4, dois fatores-chave que traduzem sinais Wnt em atividade gênica, apontando o PARP‑1 como uma ponte que ajuda a ligar sinais externos ao programa gênico de TEM dentro do núcleo.
Diminuindo o interruptor com um medicamento contra o câncer
Como medicamentos que bloqueiam a atividade de PARP já são usados no tratamento do câncer, a equipe investigou se um desses fármacos, olaparibe, poderia atenuar traços semelhantes à TEM e reduzir o crescimento de lesões em um modelo murino de endometriose. Camundongos implantados com pequenos fragmentos de tecido uterino desenvolveram lesões ectópicas no abdome, imitando aspectos da doença humana. Quando tratados com olaparibe por duas semanas, esses animais apresentaram volume total de lesões marcadamente menor e úteros mais leves com lesões aderentes, em comparação com controles não tratados. O tecido de camundongos tratados também mostrou um padrão de marcadores mais “epitelial” — maior E‑cadherina e menores N‑cadherina, vimentina, β‑catenina e TCF4 — indicando que a inibição de PARP empurrou as células para longe do estado invasivo semelhante à TEM.
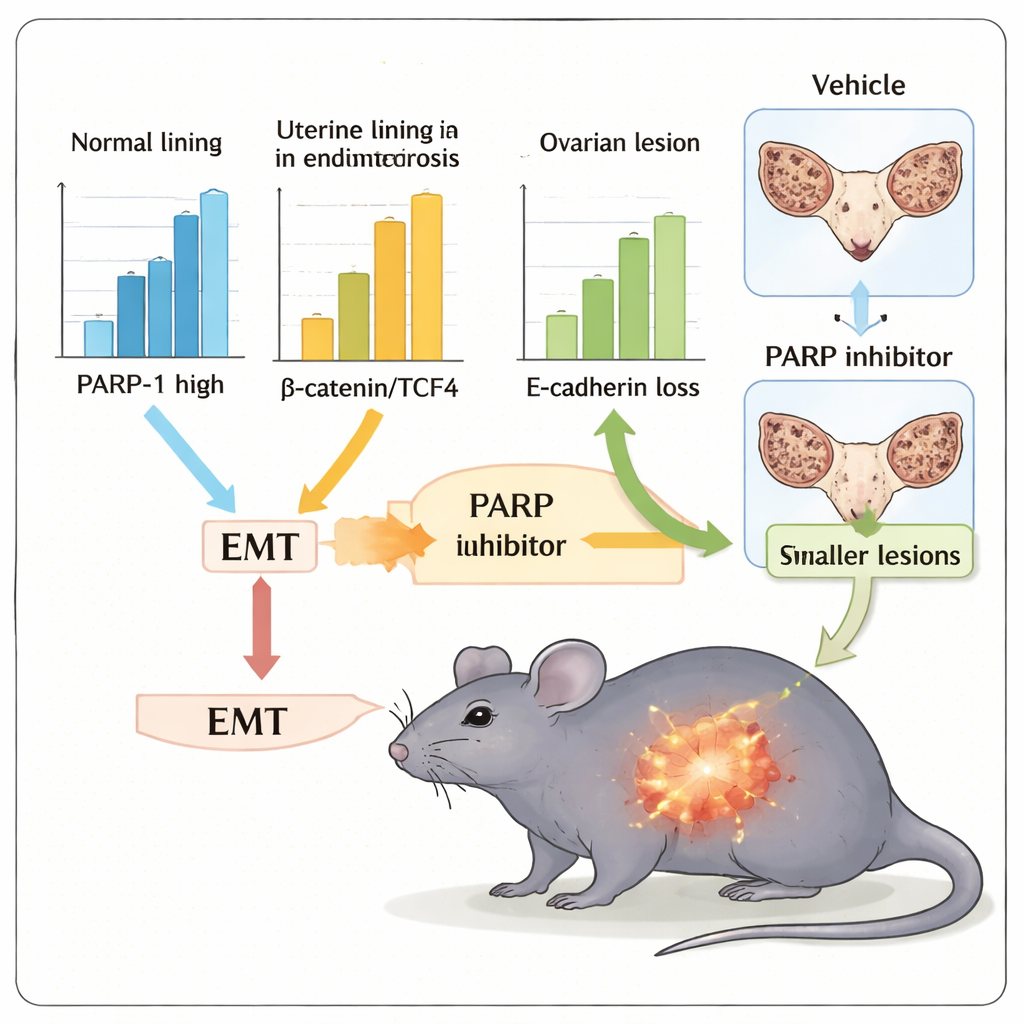
O que isso pode significar para cuidados futuros
Em conjunto, as descobertas de amostras de pacientes, experimentos em cultura celular e no modelo murino sustentam uma ideia unificadora: o PARP‑1 atua como um ponto central alvo por fármacos que conecta a sinalização Wnt/β‑catenina ao comportamento semelhante à TEM na endometriose. Em vez de ser o único interruptor mestre, o PARP‑1 parece ser um conector-chave em uma rede maior de inflamação, estresse oxidativo e sinais hormonais que moldam como as lesões crescem e invadem. Como inibidores de PARP já existem, este trabalho levanta a possibilidade de reaproveitá‑los ou adaptá‑los — talvez em combinação com outros fármacos que atinjam vias específicas ou o sistema imune — para reduzir a carga de lesões, a formação de cicatrizes e possivelmente o impacto sobre a fertilidade. Estudos maiores e de mais longo prazo serão necessários, mas esta pesquisa abre um caminho concreto rumo a terapias mais direcionadas e baseadas em mecanismos para uma condição que afeta milhões de mulheres em todo o mundo.
Citação: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
Palavras-chave: endometriose, PARP-1, transição epitélio–mesênquima, Wnt/β-catenina, terapia com inibidor de PARP