Clear Sky Science · pt
Um novo método com câmara de fluxo acoplada a IA que quantifica a fragilidade osmótica de eritrócitos
Por que a fragilidade dos glóbulos vermelhos importa
Cada segundo, milhões de seus glóbulos vermelhos passam por vasos tão finos quanto um fio enquanto transportam oxigênio. A facilidade com que essas células se rompem sob estresse — chamada de “fragilidade” — pode revelar anemia, problemas no armazenamento de sangue e complicações de infecções graves como a sepse. Este estudo apresenta um dispositivo moderno, assistido por IA, que mede a velocidade com que os glóbulos vermelhos se desfazem em soluções salinas, com o objetivo de tornar esse exame importante mais rápido, mais preciso e mais fácil de executar tanto em laboratórios de pesquisa quanto, um dia, em hospitais.
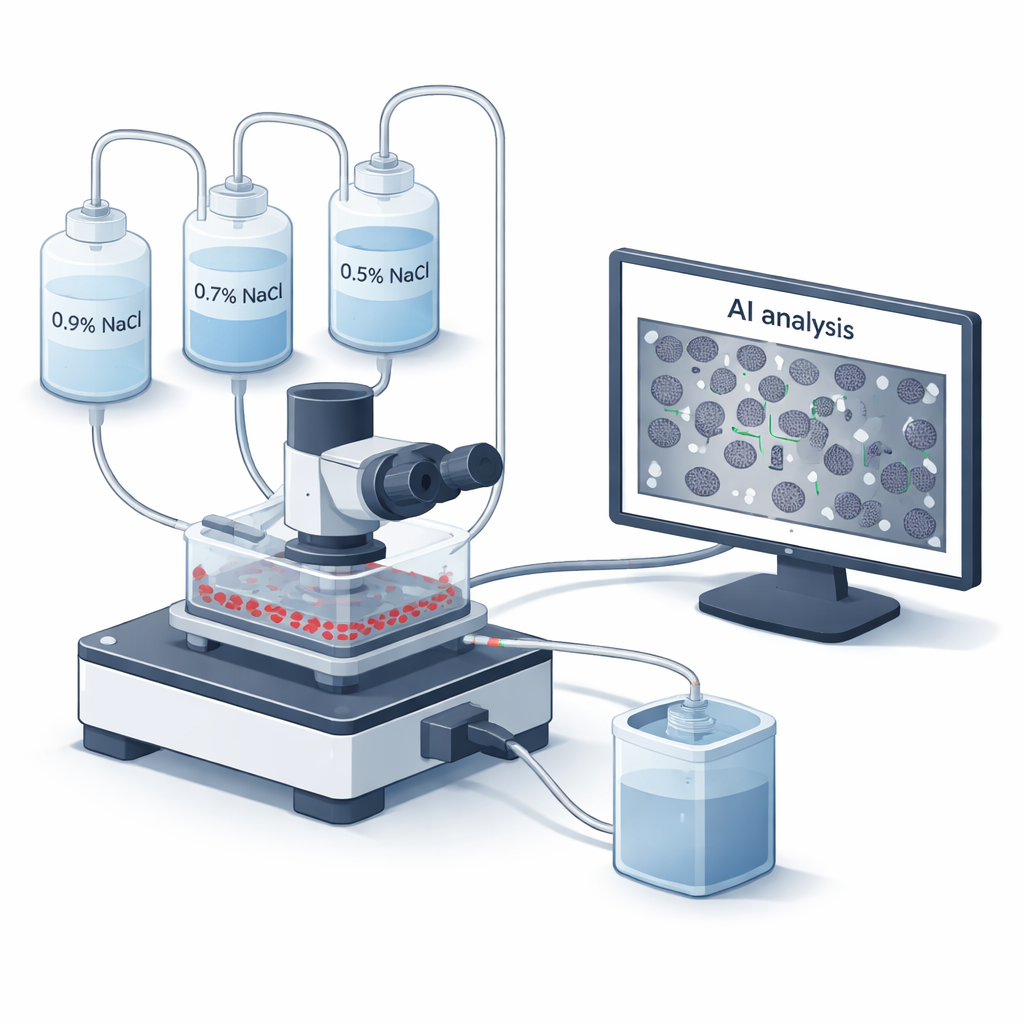
Uma nova forma de observar células sanguíneas sob estresse
Médicos usam testes de fragilidade osmótica desde a década de 1940 para avaliar a resistência das membranas dos glóbulos vermelhos. Tradicionalmente, o sangue é misturado com uma série de soluções salinas, e uma máquina mede quanto hemoglobina vaza quando as células se rompem. Embora confiável, esse método clássico é lento, manual e não mostra como células individuais realmente se comportam ao falhar. A equipe por trás deste trabalho desenvolveu um novo sistema microfluídico de “câmara de fluxo”, chamado BioExP, que espalha os glóbulos vermelhos em uma monocamada fina sobre uma lâmina de vidro tratada. Diferentes soluções salinas são bombeadas sobre essa camada enquanto um microscópio e uma câmera registram o que acontece em tempo real, e um software integrado usa inteligência artificial para contar quantas células permanecem intactas em cada nível de salinidade.
Testando IA e controle de fluxo
Para avaliar se o BioExP é confiável, os pesquisadores o compararam diretamente com o ensaio clássico por espectrofotometria usando sangue de quatro doadores saudáveis. Eles se concentraram em um número-chave chamado MCF₅₀: a concentração de sal na qual metade dos eritrócitos se rompeu. Primeiro, tiveram de ajustar o novo sistema encontrando o melhor “tempo de saturação” — quanto tempo expor as células a uma dada solução de baixa salinidade para que as células mais vulneráveis lisessem sem exagerar. Ao acompanhar quantas células desapareciam em 0,4% de sal durante 15 minutos, observaram que quase 80% de toda a hemólise ocorreu nos primeiros três minutos. Essa janela de três minutos tornou-se o tempo-padrão de exposição, equilibrando velocidade e medidas confiáveis.
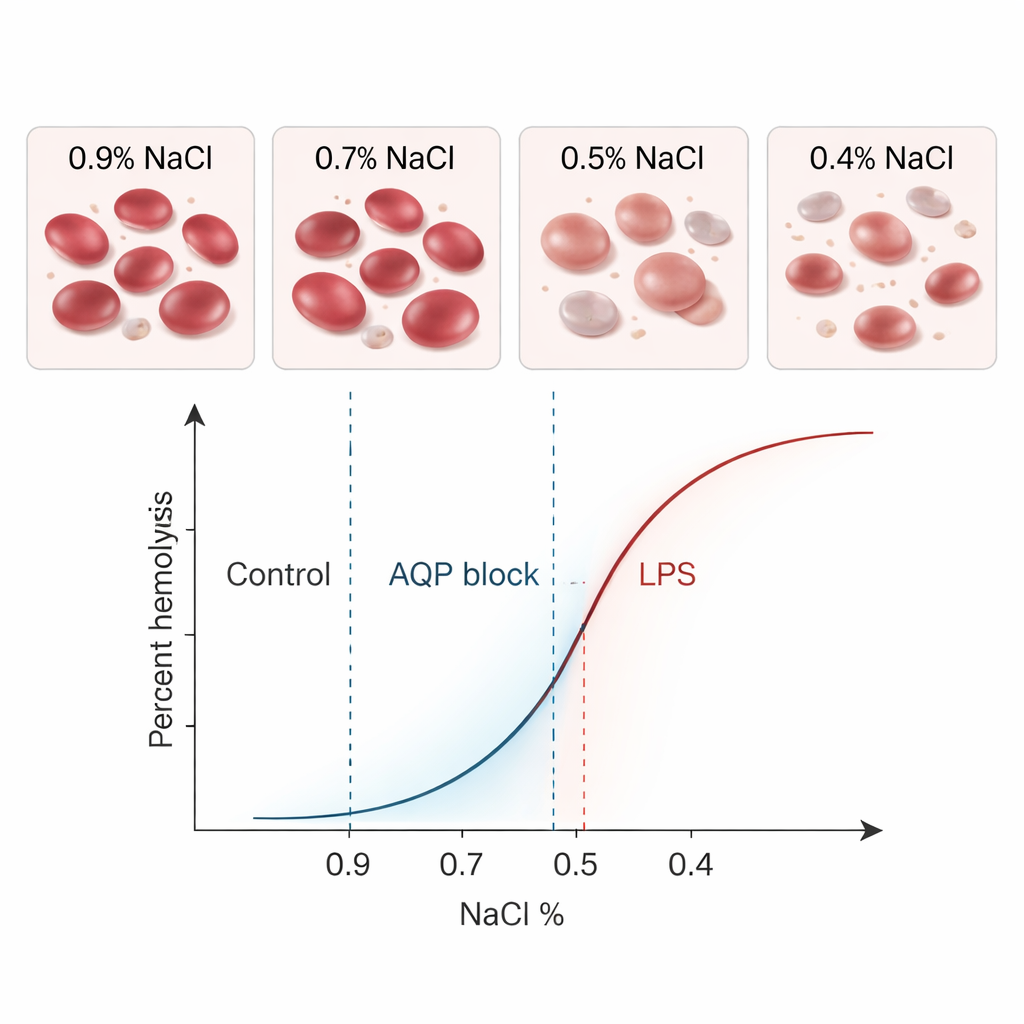
Concordando com o teste clássico e sondando a biologia real
Quando executaram as mesmas amostras saudáveis em ambos os métodos, BioExP e o teste clássico apresentaram valores médios quase idênticos de MCF₅₀ — 0,41% de sal — com variabilidade semelhante. Análises estatísticas não mostraram diferença relevante entre os métodos, e a maioria dos resultados pareados caiu dentro de limites estreitos de concordância. Em outras palavras, o novo dispositivo estava efetivamente “falando a mesma língua” que o ensaio estabelecido. O verdadeiro poder do BioExP, no entanto, está em sua capacidade de testar como várias condições alteram a fragilidade celular. Os pesquisadores escolheram dois modificadores biologicamente importantes: cloreto de mercúrio, que bloqueia proteínas canais de água chamadas aquaporinas na membrana celular, e lipopolissacarídeo (LPS) bacteriano, uma toxina associada à sepse.
Como toxinas e canais de água alteram a resistência celular
O bloqueio das aquaporinas tornou os glóbulos vermelhos mais difíceis de romper: o MCF₅₀ deslocou-se para níveis de sal menores, o que significa que as células toleraram maior diluição antes de se romperem. Tanto o BioExP quanto o método clássico detectaram claramente esse deslocamento para a esquerda. O LPS teve o efeito oposto. Quando as células foram incubadas com alta dose de LPS na ausência de plasma, tornaram-se mais frágeis, rompendo-se em concentrações salinas mais altas. Ao microscópio, muitas células mudaram de forma, ficando mais esféricas ou espiculadas — sinais visuais de que suas membranas foram perturbadas. Mais uma vez, ambos os métodos registraram um deslocamento forte e estatisticamente significativo para a direita nas curvas de fragilidade. Em todos esses testes, o novo sistema de câmara de fluxo acompanhou consistentemente as mesmas tendências biológicas do ensaio antigo, apenas com valores absolutos ligeiramente menores, porém pequenos e sistemáticos.
O que isso significa para pacientes e laboratórios
A plataforma BioExP reduz o tempo do ensaio de várias horas para menos de uma hora, precisa de volumes de sangue muito pequenos (potencialmente apenas uma picada no dedo) e automatiza a contagem e o ajuste de curvas com IA em vez de depender de muitos passos manuais. Como imagens das mesmas células são feitas ao longo do tempo, é possível conectar a aparência das células à facilidade com que se rompem, e testar muitos níveis de salinidade ou condições de drogas em uma única rodada. O estudo mostra que essa abordagem moderna pode igualar a precisão do teste clássico de fragilidade osmótica, ao mesmo tempo em que adiciona velocidade, flexibilidade e detalhes visuais ricos. Se validado em grupos maiores e mais diversos de doadores, tais sistemas podem virar ferramentas valiosas para diagnosticar anemias hemolíticas, monitorar sangue armazenado em bancos e explorar como infecções ou novos medicamentos enfraquecem ou protegem nossos glóbulos vermelhos.
Citação: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Palavras-chave: glóbulos vermelhos, fragilidade osmótica, microfluídica, sepse, inteligência artificial