Clear Sky Science · pt
Inativação seletiva de Lis1 interrompe migração e posicionamento de interneurônios corticais de somatostatina
Por que células cerebrais minúsculas e um único gene importam
Dentro dos nossos cérebros, bilhões de neurônios precisam terminar exatamente no lugar certo para que pensamentos, emoções e memórias funcionem adequadamente. Este estudo examina um grupo pequeno, mas poderoso, de células cerebrais chamadas interneurônios de somatostatina e um gene chamado Lis1, já conhecido por causar um grave transtorno de “cérebro liso” quando mutado. Ao investigar o que acontece quando Lis1 é desligado apenas nessa população celular reduzida, os pesquisadores revelam como erros sutis no movimento celular durante o desenvolvimento podem remodelar regiões cerebrais-chave envolvidas em humor, memória e doenças mentais.
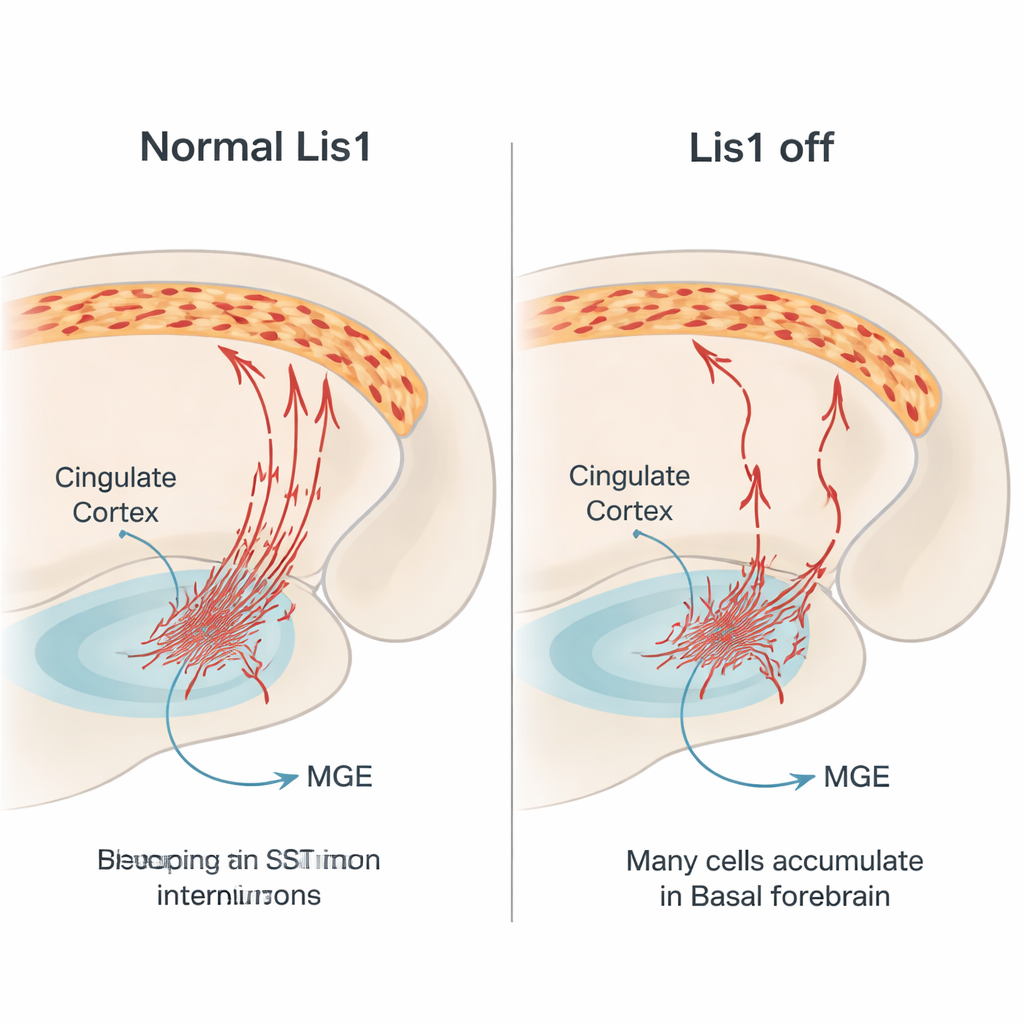
Principais atores no sistema de freio do cérebro
Os interneurônios de somatostatina atuam como parte do sistema de freio do cérebro. Eles liberam o sinal inibitório GABA e um peptídeo chamado somatostatina, mirando principalmente nos ramos dos neurônios piramidais excitatórios. Isso ajuda a manter o equilíbrio da atividade cerebral, essencial para percepção normal, tomada de decisão e controle emocional. Muitos desses interneurônios nascem em uma região profunda do cérebro embrionário chamada eminência ganglionar medial. Dali, eles viajam lateralmente por longas distâncias até o córtex cerebral, incluindo o córtex do cíngulo, um centro para emoção, dor e memória. Como essa jornada é complexa e rigidamente temporizada, genes que guiam o movimento celular são críticos. Lis1 é um desses genes, conhecido por regular a estrutura interna da célula e a maquinaria motora que movimenta o núcleo e molda a célula durante a migração.
Um experimento genético de “desligamento” direcionado
Para descobrir o que Lis1 faz especificamente nos interneurônios de somatostatina, os autores criaram camundongos nos quais Lis1 é deletado apenas nas células que ativam o gene da somatostatina. Eles também usaram uma proteína fluorescente vermelha para marcar essas células permanentemente e acompanhá‑las durante o desenvolvimento. Esse desenho experimental permitiu à equipe distinguir efeitos ocorrendo dentro das próprias células de somatostatina de alterações no restante do cérebro. Em seguida, examinaram duas regiões do cíngulo — o córtex cingulado anterior e o córtex retrosplenial — por volta de um mês após o nascimento, época em que os circuitos corticais estão relativamente maduros, mas ainda plásticos. Métodos de contagem cuidadosos foram usados para estimar tanto o número absoluto quanto a densidade de interneurônios de somatostatina em cada camada cortical.
Menos interneurônios e um padrão cortical deslocado
Em camundongos jovens adultos sem Lis1 nos interneurônios de somatostatina, tanto o córtex cingulado anterior quanto o córtex retrosplenial continham muito menos dessas células do que em animais controle. A redução foi grande e consistente em todas as camadas examinadas, indicando uma perda real em vez de uma simples redistribuição. Quando os pesquisadores olharam mais de perto como as células remanescentes estavam dispostas, encontraram uma mudança no padrão habitual por camadas. Em camundongos saudáveis, os interneurônios de somatostatina tendem a se concentrar mais nas camadas profundas do córtex. Nos mutantes, esse gradiente foi invertido, com relativamente mais células nas camadas superficiais e menos na camada mais profunda. Importante: o tamanho geral das regiões do cíngulo não diminuiu, de modo que a menor densidade reflete verdadeiramente interneurônios ausentes, não um volume de tecido comprimido.
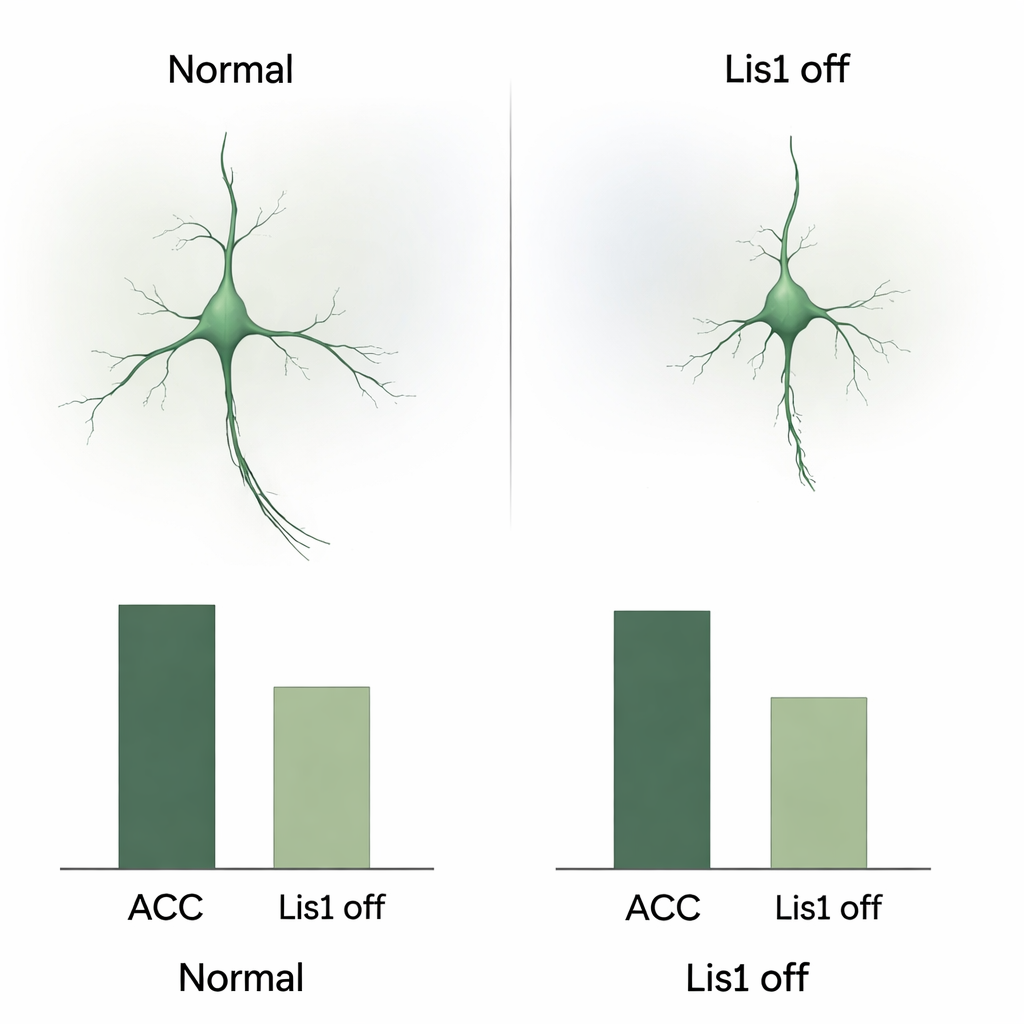
Jornada do desenvolvimento que deu errado
Para entender como essa perda surge, a equipe acompanhou as células de somatostatina marcadas em vermelho nos embriões. Confirmaram que a deleção de Lis1 começa depois que essas células deixam de se dividir, o que afasta um efeito direto sobre seu nascimento. Em vez disso, o problema emergiu durante a longa migração. Em estágios de meio de gestação, muito menos células marcadas foram encontradas seguindo pelos caminhos normais em direção ao córtex, e muitas pareciam estagnar no prosencéfalo basal, uma região ventral que precisam atravessar. As células migratórias que se moveram apresentaram formas alteradas: extensões principais mais curtas, menos ramificações e corpos celulares menores e mais arredondados — todos sinais de que sua maquinaria de transporte interna estava comprometida. Em estágios posteriores, a região ventral nos mutantes continha mais células exibindo marcadores de morte celular programada, sugerindo que muitos interneurônios estagnados morrem antes de alcançar o córtex.
O que isso significa para a saúde do cérebro
Em termos simples, quando Lis1 é desligado apenas nos interneurônios de somatostatina, muitas dessas células iniciam sua jornada normalmente, mas não conseguem alcançar seus destinos finais no córtex do cíngulo. Algumas se acumulam e morrem pelo caminho, e as que chegam são menos numerosas e posicionadas de forma desigual entre as camadas corticais. Como os sistemas de somatostatina têm sido repetidamente associados à depressão, esquizofrenia, epilepsia e doenças neurodegenerativas, este trabalho destaca uma via direta e específica por célula pela qual o mau funcionamento de Lis1 poderia contribuir para ritmos cerebrais perturbados e sintomas psiquiátricos. O estudo mostra que mesmo uma população moderada de neurônios, guiada por um único gene, pode ser crucial para construir os circuitos balanceados que sustentam pensamento e comportamento saudáveis.
Citação: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Palavras-chave: interneurônios de somatostatina, gene Lis1, migração neuronal, <keyword>transtornos do neurodesenvolvimento