Clear Sky Science · pt
A inibição de PERK atenua a morte celular multiprogramada via ativação Nrf2/HO-1 na retinopatia diabética com proteômica integrada e validação funcional em HRECs
Por que proteger a visão no diabetes é importante
Para milhões de pessoas que vivem com diabetes, uma das complicações mais temidas é a perda gradual da visão conhecida como retinopatia diabética. Esse dano ao tecido sensível à luz na parte de trás do olho costuma começar de forma silenciosa, muito antes de surgirem sintomas. O estudo por trás deste texto investiga o que realmente mata as pequenas células dos vasos sanguíneos que mantêm a retina saudável — e testa uma nova forma de protegê‑las. Ao entender e acalmar as “respostas ao estresse” celulares desencadeadas pelo excesso de açúcar, os pesquisadores esperam retardar ou até prevenir a cegueira em pessoas com diabetes.
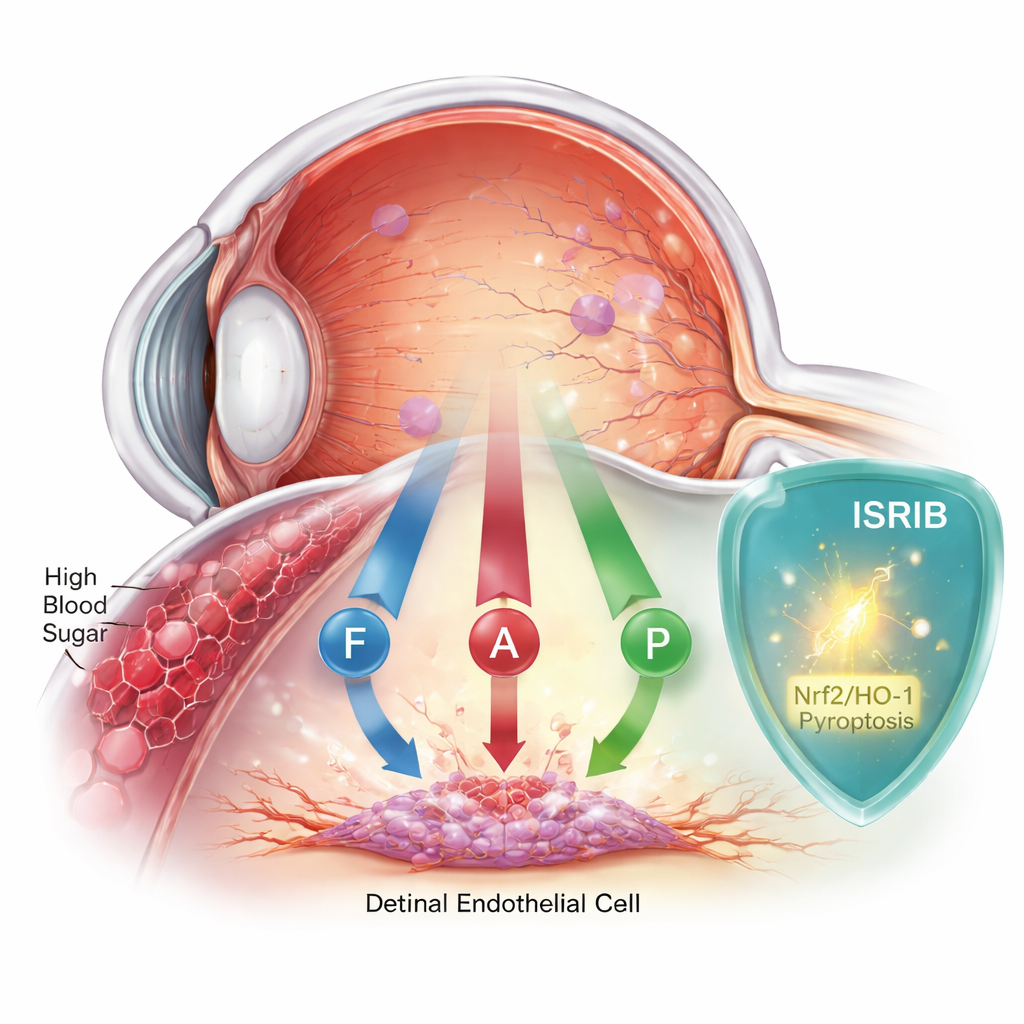
Quando o açúcar no sangue danifica o olho em silêncio
A retinopatia diabética começa quando a glicemia alta prejudica o delicado revestimento interno dos vasos da retina. Essas células formam uma barreira que mantém a retina nutrida e protegida. Durante anos, os cientistas pensaram que uma única forma de morte celular, chamada apoptose, era a principal culpada. Mas evidências crescentes sugerem que a história é mais complexa. A equipe concentrou‑se em células endoteliais retinais humanas cultivadas em laboratório e as expôs a níveis de açúcar semelhantes aos observados no diabetes mal controlado, acompanhando a resposta celular ao longo de dois dias.
Três modos de morte celular ocorrendo ao mesmo tempo
Usando uma técnica poderosa de quantificação de proteínas chamada proteômica, os pesquisadores descobriram que altos níveis de açúcar alteraram centenas de proteínas, especialmente aquelas envolvidas em respostas ao estresse, metabolismo e manejo de ferro. Testes complementares mostraram que as células não morriam por apenas um mecanismo, mas por três: a morte programada clássica (apoptose), uma forma inflamável ligada à inflamação (piropoptose) e uma forma mais recente dependente de ferro chamada ferroptose. Marcadores de dano oxidativo, sobrecarga de ferro e redução de antioxidantes aumentaram, enquanto enzimas protetoras diminuíram. Juntas, essas alterações desenharam o quadro de células sobrecarregadas por estresse, inflamação e acúmulo tóxico de moléculas reativas.
Um interruptor de estresse no centro do problema
A equipe então focalizou um sensor de estresse chave dentro das células chamado PERK, que fica na membrana do retículo endoplasmático, uma estrutura que ajuda a dobrar e processar proteínas. Em condições de glicose alta, o PERK tornou‑se hiperativo, agindo como um alarme de emergência travado que não para de tocar. Isso aparentemente alimentou os três programas de morte. Ao mesmo tempo, um sistema de defesa natural que normalmente ajuda as células a lidar com danos oxidativos — a via antioxidante Nrf2/HO‑1 — estava enfraquecido. Em termos simples, os sinais de perigo estavam aumentados enquanto os extintores internos estavam reduzidos.
Diminuindo o estresse, reforçando a proteção
Para ver se era possível interromper esse ciclo destrutivo, os pesquisadores trataram as células expostas a alto açúcar com ISRIB, uma pequena molécula que reduz efetivamente o sinal de estresse mediado por PERK. Os resultados foram notáveis. O ISRIB melhorou a sobrevivência celular, reduziu marcadores de dano por ferro e estresse oxidativo e diminuiu sinais químicos tanto da apoptose quanto da piropoptose. Ao mesmo tempo, aumentou a via de defesa Nrf2/HO‑1, ajudando as células a restaurar sua capacidade antioxidante. Um fármaco separado que bloqueia especificamente a ferroptose também foi benéfico, mas o ISRIB se destacou por acalmar as três rotas de morte ao mesmo tempo, em vez de apenas uma.
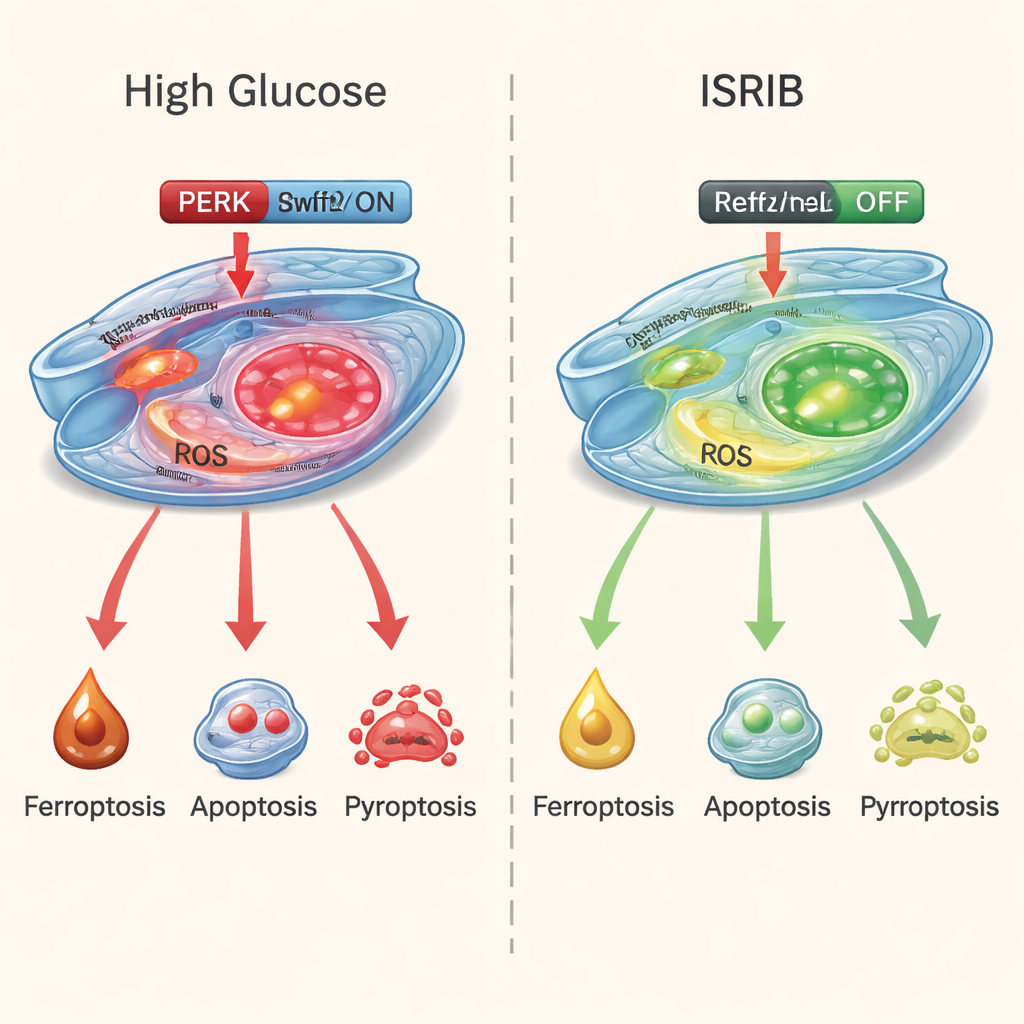
O que isso pode significar para pessoas com diabetes
Este trabalho sugere que o dano inicial na retinopatia diabética não é causado por um único “vilão”, mas por uma convergência de vários programas de morte que se reforçam, impulsionados pelo estresse celular crônico. Ao reduzir o interruptor de estresse PERK e reativar os sistemas protetores da própria célula, fármacos como o ISRIB podem oferecer uma maneira mais unificada de manter os vasos sanguíneos da retina vivos. Embora esses experimentos tenham sido realizados em células, não em pacientes, eles apontam para tratamentos futuros que miram as respostas ao estresse dentro do olho — potencialmente acrescentando uma nova camada de proteção ao controle da glicemia e às injeções atuais no olho para ajudar a preservar a visão no diabetes.
Citação: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Palavras-chave: retinopatia diabética, morte de células retinais, estresse oxidativo, via PERK, Nrf2 HO-1