Clear Sky Science · pt
Inibição da via SHH e co-cultura com astrócitos induzem respostas distintas em glioblastoma e células‑tronco cancerígenas
Por que tumores cerebrais são tão difíceis de tratar
O glioblastoma é um dos cânceres cerebrais mais letais e, mesmo com cirurgia, radioterapia e quimioterapia, apenas uma pequena fração dos pacientes vive além de cinco anos. Uma razão é que esses tumores não são formados por um único tipo de célula. Incluem um pequeno grupo de “células‑tronco” cancerígenas especialmente resistentes, que podem sobreviver ao tratamento e ajudar o tumor a reaparecer. Este estudo investiga uma questão central: como esses diferentes tipos celulares do tumor respondem quando um sinal promotor de crescimento é bloqueado, e como a presença de células normais de suporte do cérebro, chamadas astrócitos, altera essa resposta?
Um olhar mais atento às células mais resistentes do tumor
Os pesquisadores trabalharam com dois tipos principais de células de um modelo comum de glioblastoma: as células do tumor em massa e uma pequena subpopulação marcada por uma proteína chamada CD133, que se comporta como células‑tronco cancerígenas. Essas células com características de tronco se dividiam menos, eram menores e mais arredondadas, e formavam aglomerados mais compactos do que as células em massa. A equipe também cultivou as células tumorais junto com astrócitos, as células em forma de estrela que ajudam a manter o tecido cerebral saudável. Essa cultura mista imita melhor o ambiente tumoral real, onde as células cancerígenas constantemente “conversam” com seus vizinhos. 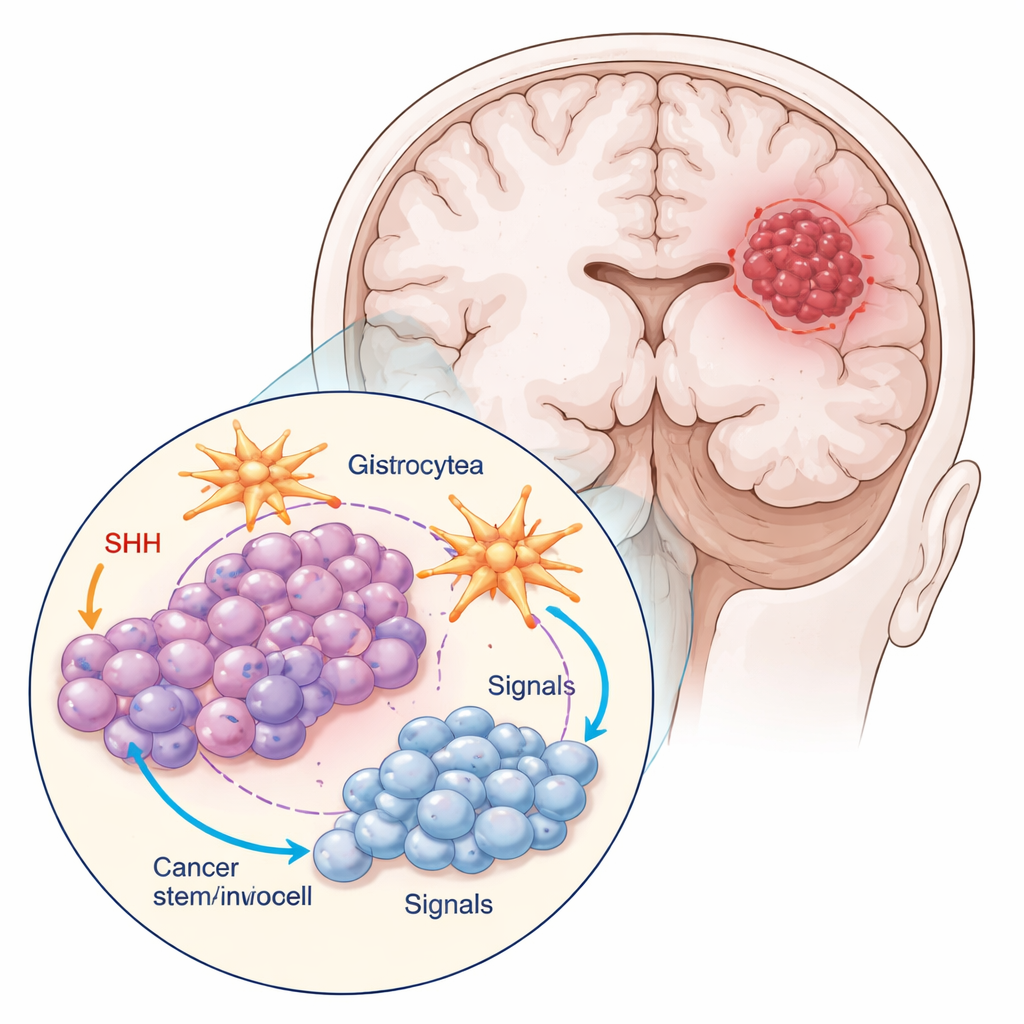
Bloqueando um sinal de desenvolvimento que os tumores reaproveitam
Muitos glioblastomas, especialmente suas células com traços de tronco, sequestram uma via de comunicação molecular chamada Sonic Hedgehog (SHH), normalmente ativa durante o desenvolvimento cerebral. A equipe usou a ciclopamina, um composto que bloqueia um componente-chave da via SHH, para ver como tanto as células tumorais em massa quanto as células‑tronco cancerígenas respondem. Eles mediram a atividade de genes e proteínas relacionados à SHH, a velocidade com que as células avançavam no ciclo celular e a frequência de morte celular programada (apoptose). A ciclopamina alterou a sinalização SHH de maneira fortemente dependente do tipo celular e da presença de astrócitos. As células‑tronco cancerígenas produziram o maior sinal SHH quando cultivadas isoladamente, mas essa secreção caiu quando foram cultivadas com astrócitos e expostas ao fármaco, sugerindo que as células cerebrais circundantes podem atenuar o “auto‑suporte” químico do tumor.
Como a vizinhança altera crescimento e morte
Além da própria SHH, a equipe acompanhou outras redes gênicas que orientam se as células continuam a se dividir, fazem uma pausa ou começam a se especializar. Em culturas simples apenas com tumor, o bloqueio da SHH levou as células em massa a uma paralisação na fase tardia da divisão (G2/M), enquanto as células com traços de tronco tendiam a se acumular mais cedo, na fase de repouso ou de entrada (G0/G1). Quando os astrócitos foram adicionados, esses padrões mudaram: as células‑tronco cancerígenas, que antes eram mais quiescentes, passaram a apresentar bloqueio em G2/M, indicando um conjunto diferente de “freios” sendo aplicados no ambiente misto. Os pesquisadores também observaram que sinais ligados ao destino celular e à moldagem dos tecidos — como as vias WNT, BMP e TGF‑β — foram modulados de forma distinta em células em massa e em células‑tronco quando astrócitos estavam presentes, o que significa que o microambiente pode inclinar as células tanto para manter um comportamento mais de tronco quanto para um estado mais diferenciado e menos agressivo.
Induzindo morte nas células mais resistentes
O estudo examinou ainda com que facilidade as células passavam por apoptose. Leitura genética e um ensaio que detecta dano ao DNA (TUNEL) mostraram que a ciclopamina favoreceu uma via “externa” de morte celular, conduzida por uma proteína chamada CASP8, particularmente na população de células‑tronco cancerígenas. Curiosamente, em células tumorais cultivadas sozinhas, a morte celular total às vezes diminuiu após o bloqueio da SHH, sugerindo que essas células poderiam ativar estratégias alternativas de sobrevivência. Por outro lado, quando as células com características de tronco foram co‑cultivadas com astrócitos, a ciclopamina aumentou marcadores de apoptose, indicando que as células cerebrais circundantes podem tornar essas células normalmente resistentes mais vulneráveis uma vez que a sinalização SHH é bloqueada. 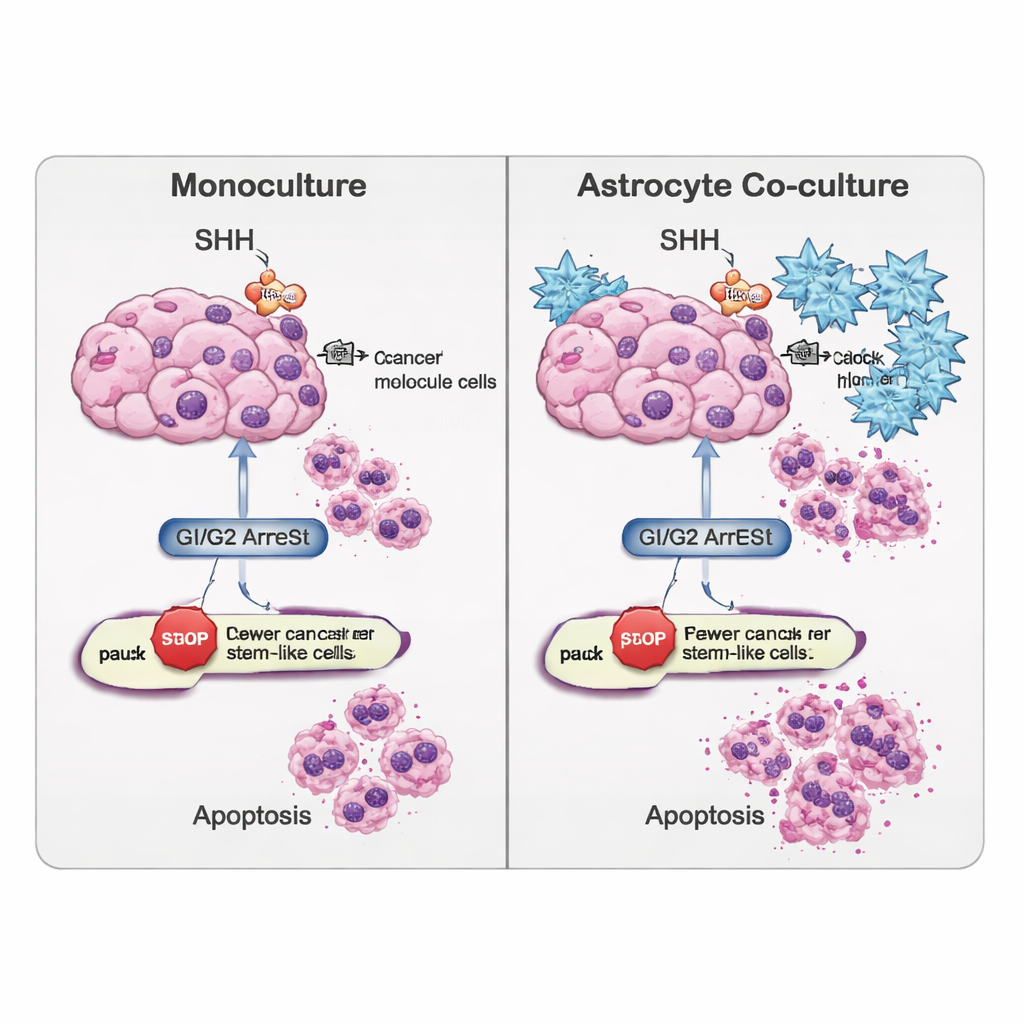
O que isso significa para tratamentos futuros do câncer cerebral
Para um público não especializado, a mensagem-chave é que mirar um único sinal de crescimento no glioblastoma não é suficiente se ignorarmos a vizinhança do tumor. Este trabalho mostra que os astrócitos — as células normais que compartilham espaço com o tumor — podem alterar profundamente como tanto as células tumorais em massa quanto as células‑tronco respondem ao bloqueio da via SHH. As células‑tronco cancerígenas, em particular, tornaram‑se mais propensas a parada do ciclo celular e a formas de morte celular quando astrócitos estavam presentes. Os autores concluem que fármacos direcionados à SHH e vias relacionadas têm mais chance de funcionar se forem testados e, eventualmente, usados de formas que reflitam o ambiente real do cérebro, possivelmente em combinação com outros tratamentos que ataquem as rotas de sobrevivência alternativas do tumor. Em resumo, compreender e explorar a “conversa” entre as células tumorais e seus vizinhos pode abrir estratégias mais precisas e duradouras contra esse câncer notoriamente implacável.
Citação: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Palavras-chave: glioblastoma, células‑tronco cancerígenas, via Sonic Hedgehog, microambiente tumoral, astrócitos