Clear Sky Science · pt
Identificação e validação de uma nova assinatura gênica relacionada à ferroptose associada à degeneração retinal hereditária em camundongos Rd10
Por que as células oculares que morrem importam para todos nós
A retinite pigmentosa é um grupo de doenças oculares hereditárias que gradualmente roubam a visão das pessoas, frequentemente começando com cegueira noturna e culminando na perda total da visão. Não existe cura, e as terapias gênicas atuais só beneficiam uma pequena fração dos pacientes. Este estudo explora um ângulo diferente: uma forma especial de morte celular chamada ferroptose, impulsionada por ferro e dano oxidativo, para descobrir novos alvos gênicos que um dia possam proteger as células sensíveis à luz na retina — independentemente da mutação com que a pessoa nasceu.
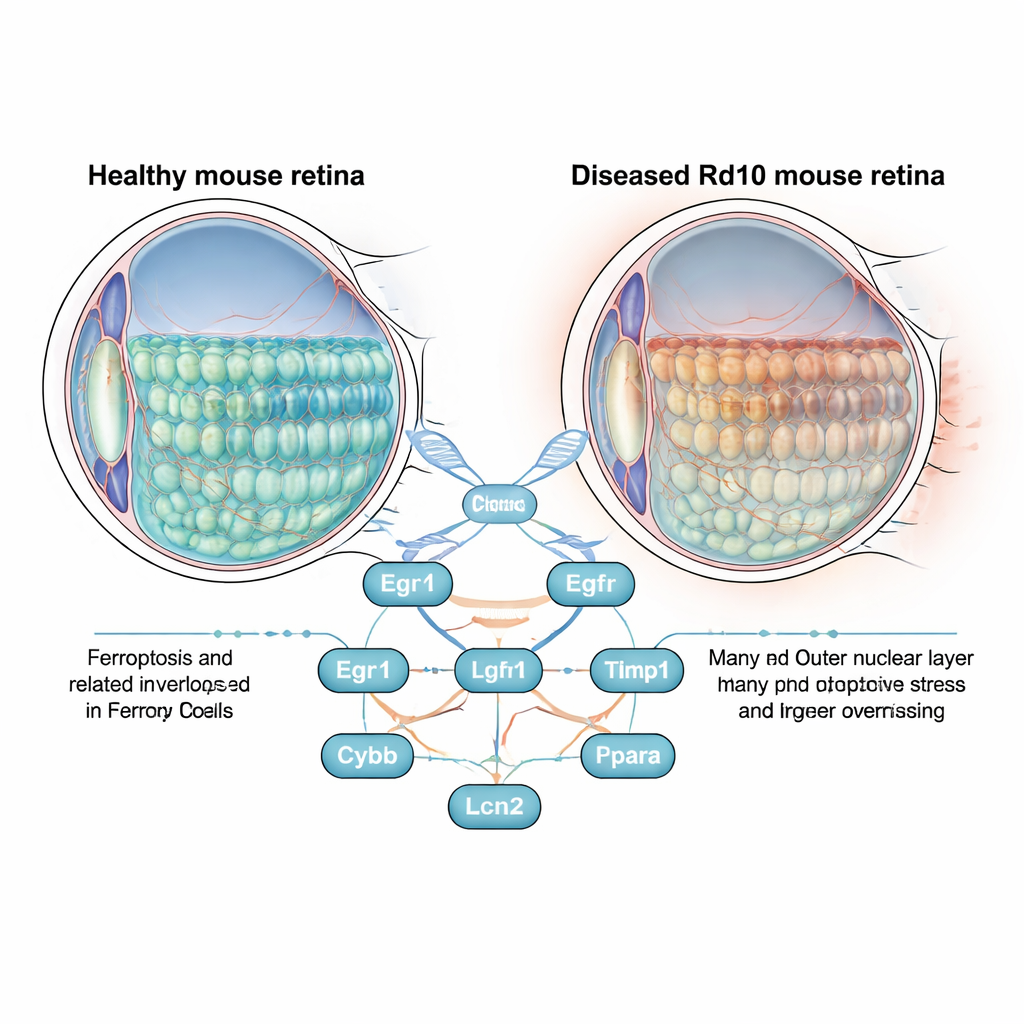
Um olhar mais atento sobre uma doença ocular que causa cegueira
A retina é uma camada fina de tecido na parte de trás do olho que abriga os fotorreceptores bastonetes e cones, as células que convertem luz em sinais elétricos. Na retinite pigmentosa, essas células morrem lentamente, primeiro roubando a visão noturna e periférica e depois a visão central. Os cientistas frequentemente estudam esse processo em camundongos Rd10, que carregam uma mutação que imita de perto a doença humana. Em vez de focar apenas no gene defeituoso, os autores fizeram uma pergunta mais ampla: à medida que a retina degenera, quais genes ligados à ferroptose são ativados ou desativados, e eles poderiam estar impulsionando a perda celular?
Encontrando os genes-chave em um mar de dados
A equipe explorou grandes conjuntos públicos de expressão gênica de retinas saudáveis e de camundongos Rd10, essencialmente tirando um “instantâneo” global de quais genes estavam mais ou menos ativos. Eles encontraram mais de 2.000 genes que mudaram, e então confrontaram essa lista com um catálogo curado de genes relacionados à ferroptose. Isso reduziu o conjunto para 37 candidatos ligados à morte celular oxidativa dirigida pelo ferro. Análises computacionais mostraram que esses genes se agrupavam em processos como resposta ao estresse oxidativo, regulação da morte neuronal e vias de metabolismo lipídico — marcas registradas da ferroptose e respostas ao estresse conhecidas em nervos em degeneração.
Oito genes que se destacam
Para identificar os atores mais influentes, os pesquisadores construíram uma rede de interação proteica e aplicaram vários algoritmos de ranqueamento. Surgiram oito genes “hub”: Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 e Ppara. Sete deles mostraram maior atividade nas retinas doentes, enquanto Ppara apresentou menor atividade. O grupo confirmou esses padrões em um conjunto de dados independente e depois examinou mais de perto onde os genes principais apareciam no olho. Usando coloração fluorescente e sequenciamento de RNA em célula única, demonstraram que Egr1 está fortemente aumentado em fotorreceptores bastonetes e cones, enquanto Cd44 está marcadamente elevado em células de Müller, as células gliais de suporte que atravessam a retina. Isso sugere que fotorreceptores estressados e suas células de suporte podem cooperar — possivelmente de forma prejudicial — por meio de vias ligadas à ferroptose.
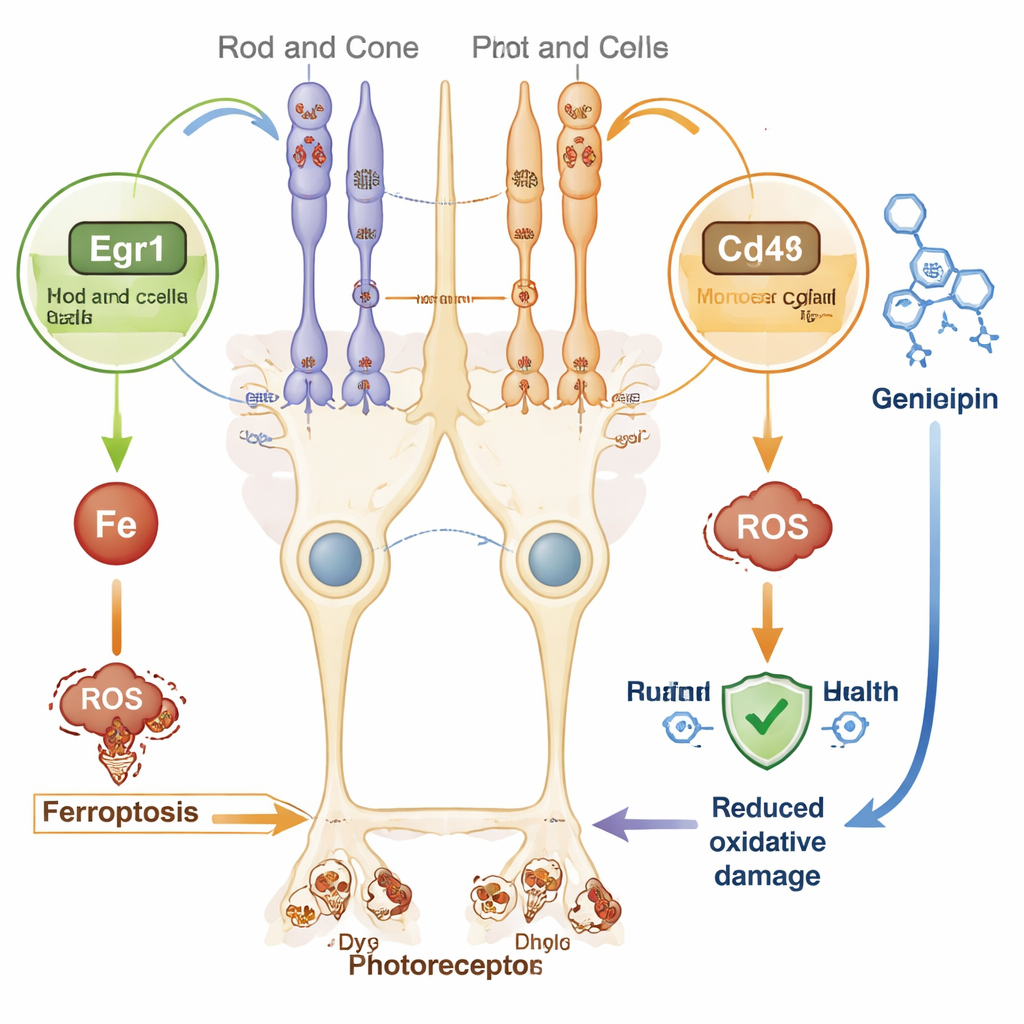
O que isso significa para tratamentos futuros
Como a terapia gênica adaptada a cada gene defeituoso é complexa e cara, estratégias de ação ampla são atraentes. A nova assinatura gênica identificada aponta para várias dessas possibilidades. Por exemplo, Egr1 é um interruptor de ação rápida que responde ao estresse oxidativo e pode promover ferroptose em outros órgãos. Cd44, uma molécula de superfície nas células de Müller, tem sido mostrada em diferentes tecidos como agravante de sobrecarga de ferro e morte celular. Ao mesmo tempo, a diminuição de Ppara, um regulador do metabolismo lipídico e do uso de energia, pode deixar as células retinianas mais vulneráveis ao dano. Ao direcionar essas vias de estresse compartilhadas, pode ser possível retardar a degeneração retiniana em muitas formas genéticas de retinite pigmentosa.
Fármacos que podem ajudar a proteger a visão
Usando um banco de dados de interação droga–gênio, os autores buscaram compostos que pudessem influenciar Egr1 ou Cd44. Surgiram várias moléculas existentes, incluindo o composto natural genipina, que mostrou efeitos protetores em modelos de doença de Parkinson, degeneração nervosa e retinopatia diabética ao reduzir o estresse oxidativo e a inflamação. Embora nenhuma dessas drogas candidatas tenha sido testada ainda neste modelo específico de camundongo com retinite pigmentosa, elas fornecem pontos de partida promissores para futuros estudos laboratoriais e em animais voltados a proteger os fotorreceptores da ferroptose.
Mensagem principal para não especialistas
Este trabalho mostra que a morte celular oxidativa dirigida pelo ferro está intimamente entrelaçada com as mudanças de atividade gênica observadas em um modelo clássico de cegueira hereditária. Ao destacar oito genes-chave, e especialmente o gene sensível ao estresse Egr1 nos fotorreceptores e Cd44 nas células de Müller, o estudo mapeia um novo território para potenciais terapias que não dependem de corrigir um único gene mutado. Se experimentos futuros confirmarem que acalmar a ferroptose por meio desses alvos pode manter as células retinianas vivas, isso poderá abrir a porta para tratamentos que beneficiem uma ampla gama de pacientes enfrentando perda progressiva da visão.
Citação: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Palavras-chave: retinite pigmentosa, ferroptose, fotoreceptores, degeneração retiniana, Egr1 Cd44