Clear Sky Science · pt
Metabolômica integrada e sequenciamento de 16S rRNA revelam o mecanismo das flavonas totais de Abelmoschus manihot (L.) Medic contra a fibrose hepática
Poder das Flores para um Fígado Cicatrizado
Cicatrização do fígado, ou fibrose, é um perigo silencioso que pode, gradualmente, levar à cirrose e à insuficiência hepática. A medicina moderna ainda carece de medicamentos seguros e amplamente eficazes para interromper ou reverter esse processo. Este estudo investiga se compostos naturais das flores amarelas de Abelmoschus manihot — uma planta da medicina tradicional chinesa já usada para doenças renais — podem proteger o fígado de danos tóxicos crônicos e como eles podem fazê‑lo agindo tanto na química do organismo quanto nos micróbios do intestino.
Um Problema Hepático Global em Crescimento
Centos de milhões de pessoas no mundo vivem com doença hepática crônica causada por vírus, álcool, acúmulo de gordura ou toxinas. Quando o fígado é lesionado repetidamente, responde depositando tecido cicatricial, como uma ferida que nunca cicatriza totalmente. Com o tempo, essa fibrose pode enrijecer o órgão, obstruir o fluxo sanguíneo e progredir para cirrose, uma causa importante de mortes relacionadas ao fígado. Como muitos gatilhos diferentes podem causar esse dano ao mesmo tempo, os pesquisadores mostram particular interesse por misturas de plantas capazes de atuar em vários alvos simultaneamente, em vez de fármacos de molécula única que atingem apenas uma via.
Testando um Remédio Tradicional em Camundongos
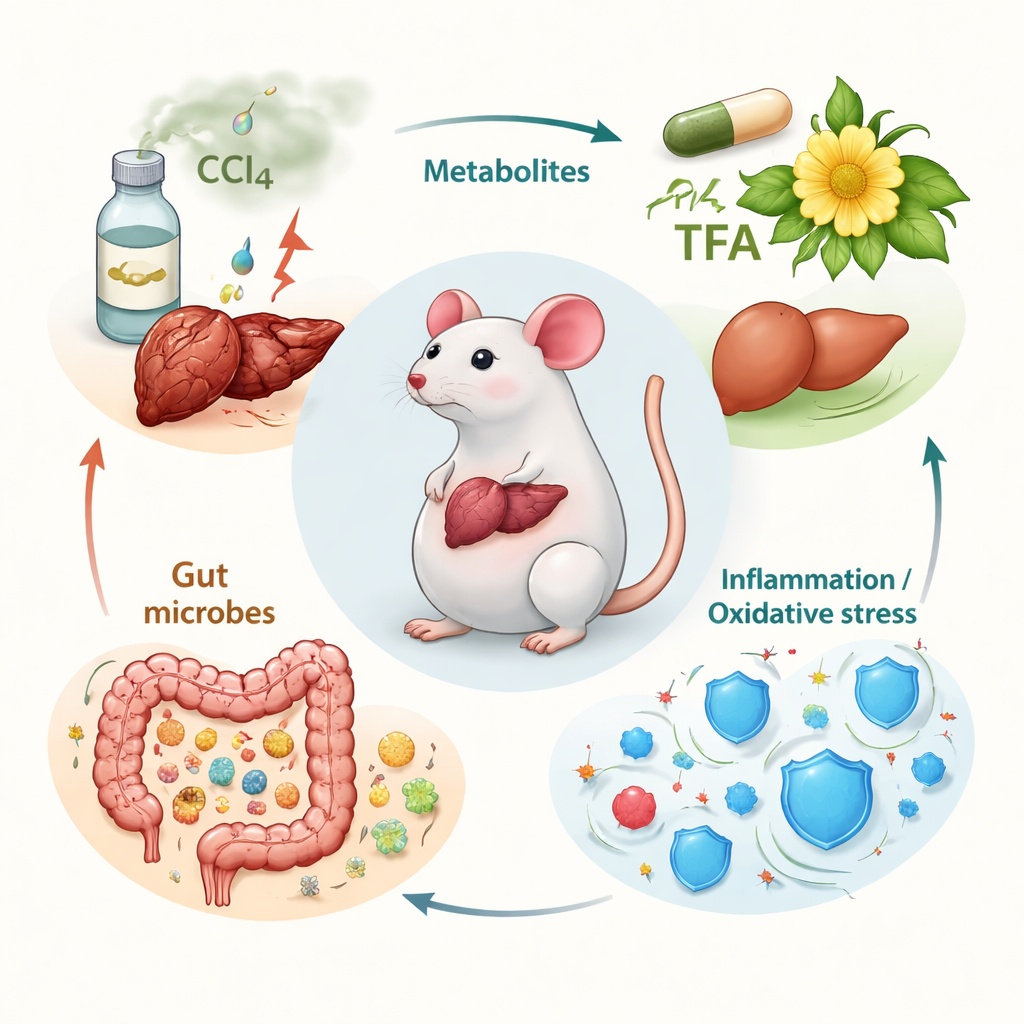
A equipe focou nas “flavonas totais” de Abelmoschus manihot (TFA) — uma mistura concentrada de sete compostos vegetais relacionados previamente demonstrados como anti‑inflamatórios e antioxidantes. Utilizaram um modelo de camundongo bem estabelecido no qual a exposição repetida ao químico industrial tetracloreto de carbono (CCl4) causa lesão hepática crônica e cicatrização semelhante à fibrose humana. Camundongos machos foram divididos em grupos: controles saudáveis, camundongos “modelo” danificados por CCl4, um grupo com fármaco padrão e três grupos com diferentes doses de TFA. Após semanas de exposição ao CCl4, os pesquisadores trataram os animais com TFA por via oral e então examinaram sangue, tecido hepático e conteúdo intestinal.
Exames de Sangue Mais Limpos e Tecido Hepático Mais Saudável
A TFA mostrou efeitos protetores claros. Os níveis sanguíneos das enzimas hepáticas ALT e AST — indicadores clínicos de dano às células do fígado — aumentaram fortemente em camundongos expostos ao CCl4, mas caíram cerca de metade nos animais tratados com TFA. O exame microscópico contou a mesma história: fígados fibróticos não tratados exibiam arquitetura distorcida, células mortas, depósitos pesados de colágeno e acúmulo de células inflamatórias. Fígados tratados com TFA apresentaram menos “pseudo‑lóbulos” cicatriciais, menor coloração por colágeno e sinais reduzidos de morte celular. Marcadores de estresse oxidativo também melhoraram: defesas antioxidantes (SOD e GSH‑Px) aumentaram, enquanto subprodutos danosos (MDA) diminuíram. Mediadores inflamatórios chave, incluindo TNF‑α, IL‑6 e TGF‑β1, também foram reduzidos, assim como marcadores químicos de fibrose, como hidroxiprolina, colágeno IV e ácido hialurônico.
Reequilibrando a Química Corporal e os Micróbios Intestinais
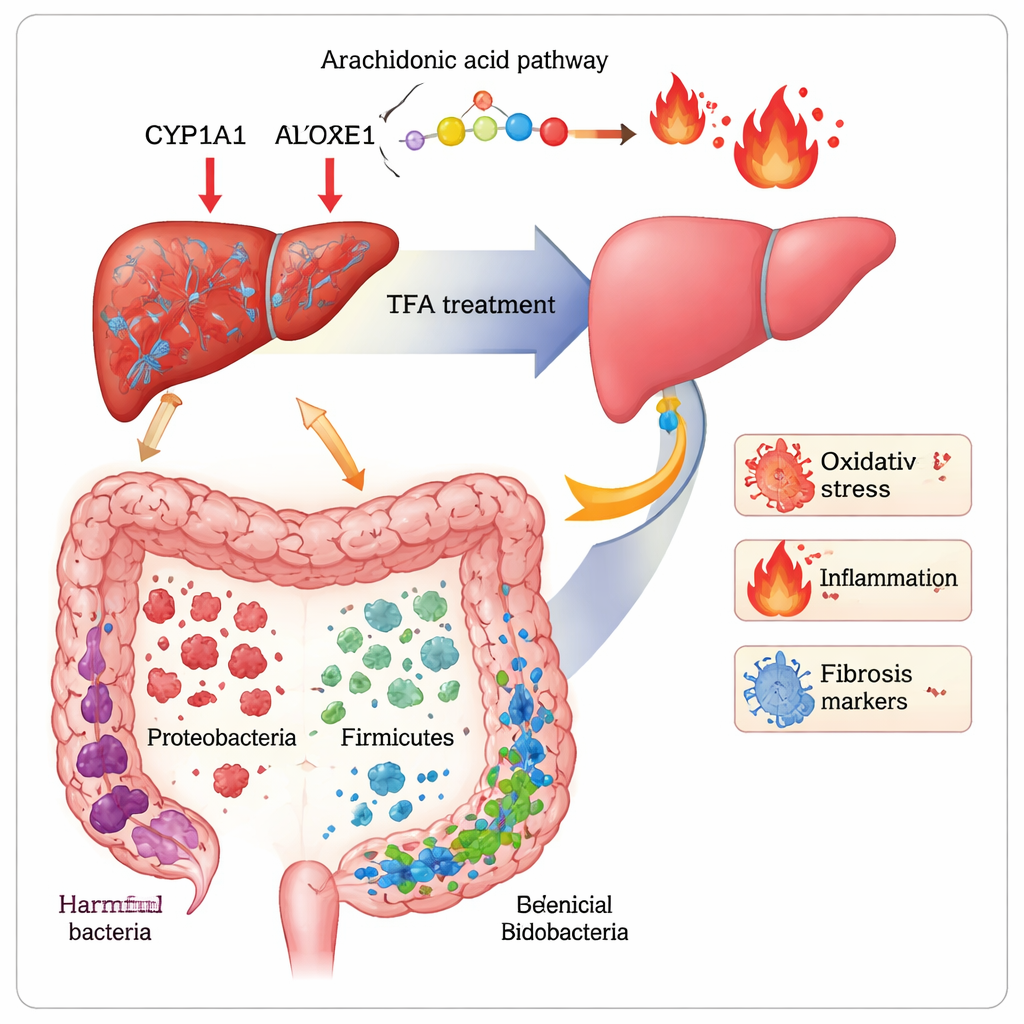
Para descobrir como a TFA produz esses benefícios, os pesquisadores combinaram duas ferramentas poderosas: metabolômica, que perfila centenas de pequenas moléculas no sangue, e sequenciamento de 16S rRNA, que mapeia os tipos de bactérias no intestino. Em camundongos fibróticos, dezenas de metabólitos envolvidos no manejo de gorduras e na degradação de aminoácidos estavam perturbados. A TFA restaurou parcialmente o equilíbrio em vias ligadas às membranas celulares (glicerofosfolipídios), ao aminoácido relacionado ao humor triptofano, e a um ácido graxo chamado ácido araquidônico que alimenta sinais inflamatórios. Níveis de dois produtos do ácido araquidônico, 20‑HETE e 16(R)‑HETE — ambos ligados ao estresse oxidativo e à fibrose — foram reaproximados ao normal. No fígado, a TFA reduziu a abundância de três enzimas (CYP1A1, CYP2E1, ALOX15) que ajudam a gerar essas moléculas nocivas. Ao mesmo tempo, o CCl4 perturbou a microbiota intestinal, diminuindo grupos benéficos como Firmicutes, Lactobacillus e Bifidobacterium e permitindo que potenciais Proteobacteria nocivas proliferassem. A TFA reverteu grande parte dessa mudança, aumentando a diversidade e restaurando bactérias “amistosas” associadas a melhor função de barreira e menor inflamação.
Uma Estratégia Multifocal na Autoestrada Intestino–Fígado
Ao conectar alterações bacterianas com químicos sanguíneos e marcadores de doença, o estudo sugere que a TFA age ao longo do “eixo intestino–fígado” — a via movimentada de sinais, nutrientes e toxinas que viajam do intestino ao fígado. Bactérias e seus produtos nocivos parecem acompanhar maior inflamação e cicatrização, enquanto micróbios benéficos correlacionam‑se com perfis metabólicos mais saudáveis e menos fibrose. A TFA parece empurrar todo esse sistema de volta ao equilíbrio: fortalece defesas antioxidantes, acalma vias inflamatórias alimentadas pelo ácido araquidônico, remodela a comunidade microbiana intestinal e, em última instância, reduz a resposta de cicatrização no fígado.
O Que Isso Pode Significar para Tratamentos Futuros
Para não‑especialistas, a mensagem principal é que um extrato floral usado há muito na medicina tradicional mostrou promessa real em um teste moderno e rigoroso de cicatrização hepática crônica. Em camundongos, a TFA fez mais do que proteger células do fígado — modulou a química tóxica e micróbios intestinais prejudiciais ao mesmo tempo. Embora esses resultados ainda não provem benefício em humanos, e tenham sido obtidos apenas em animais machos usando um tipo de lesão hepática, eles destacam uma potencial terapia multifocal que atua com as redes do próprio corpo em vez de contra uma única molécula. Com testes adicionais, tais flavonas de origem vegetal poderão, um dia, fazer parte de um conjunto mais amplo de ferramentas para retardar ou até reverter a fibrose hepática.
Citação: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Palavras-chave: fibrose hepática, microbiota intestinal, metabolômica, flavonoides, medicina tradicional chinesa