Clear Sky Science · pt
INHBA: um gene pan-morte relacionado à mitocôndria associado ao prognóstico e à imunidade do OSCC
Por que isso importa para o câncer de boca
O carcinoma espinocelular oral, uma forma comum de câncer de boca, pode tirar das pessoas capacidades básicas como falar, comer e até sorrir confortavelmente. Apesar de cirurgia, radioterapia e quimioterapia, muitos pacientes ainda enfrentam recidiva e baixa sobrevida a longo prazo. Este estudo oferece um novo olhar sobre o câncer de boca ao focar em como um único gene, chamado INHBA, ajuda a moldar a morte celular, o bairro de células de suporte do tumor e o sucesso ou fracasso de tratamentos modernos como a imunoterapia.
Um olhar mais atento a um câncer de boca letal
A maioria dos cânceres de cabeça e pescoço começa no revestimento da boca, e mais de 90% destes são carcinoma espinocelular oral (OSCC). Mundialmente, casos e mortes por OSCC estão aumentando e espera-se que cresçam cerca de 40% até 2040. O cuidado padrão depende de cirurgia mais radioterapia e quimioterapia, mas muitos tumores resistem ao tratamento e retornam. Imunoterapias mais recentes, que visam despertar as defesas do próprio corpo, ajudam apenas uma fração dos pacientes. Para ir além do tratamento por tentativa e erro, os pesquisadores precisam entender quais genes impulsionam o OSCC e como eles interagem com o sistema imunológico.
Morte celular, usinas de força e uma nova categoria de genes
Nossas células estão programadas para morrer de várias maneiras cuidadosamente controladas, incluindo processos com nomes como apoptose, autofagia, ferroptose e outros. No câncer, esses programas de morte frequentemente são reconfigurados para que as células tumorais sobrevivam quando não deveriam. A equipe por trás deste estudo concentrou-se em um grupo amplo que chamou de genes de “pan‑morte celular” — genes que estão na encruzilhada de diferentes vias de morte — e aprofundou-se naqueles ligados às mitocôndrias, as pequenas usinas de força das células. Ao combinar grandes conjuntos públicos de dados de câncer com um catálogo especializado de genes mitocondriais, definiram um conjunto de “genes pan‑morte celular associados à mitocôndria” e procuraram aqueles mais fortemente relacionados ao comportamento do OSCC e ao desfecho dos pacientes.
Encontrando INHBA entre muitos suspeitos
Usando estatística avançada e nove algoritmos diferentes de aprendizado de máquina, os pesquisadores filtraram milhares de genes e identificaram 19 genes pan‑morte celular mitocondriais com fortes vínculos ao prognóstico no OSCC. Entre eles, INHBA destacou‑se. Sua atividade foi consistentemente mais alta em amostras tumorais do que no tecido bucal normal e esteve associada a pior sobrevida tanto no OSCC quanto no grupo mais amplo de cânceres de cabeça e pescoço. Quando os tumores foram divididos em grupos de alto e baixo INHBA, aqueles com níveis mais altos exibiram sinais biológicos mais agressivos, incluindo vias relacionadas à invasão tecidual, crescimento de vasos sanguíneos e estresse mitocondrial. Testes laboratoriais em amostras de pacientes confirmaram que os níveis da mensagem de INHBA estavam de fato elevados em tumores do mundo real.
O papel oculto das células de suporte ao redor do tumor
Para entender onde o INHBA é mais ativo, a equipe recorreu ao sequenciamento de RNA de célula única e à transcriptômica espacial, tecnologias que mapeiam a atividade gênica em células individuais e em cortes de tecido. Eles descobriram que o INHBA não é produzido principalmente pelas próprias células cancerosas, mas pelos fibroblastos associados ao câncer — células de suporte que remodelam o tecido e moldam o ambiente imunológico. Um subtipo particular, chamado CAFs miofibroblásticos, apresentou níveis especialmente altos de INHBA. Mapas detalhados de comunicação sugeriram que fibroblastos ricos em INHBA conversam intensamente com células imunes e com as células tumorais, ajudando a criar um nicho imunossupressor e semelhante a uma cicatriz ao redor do câncer. Esse microambiente parece favorecer o crescimento tumoral e pode reduzir a eficácia de algumas formas de imunoterapia.
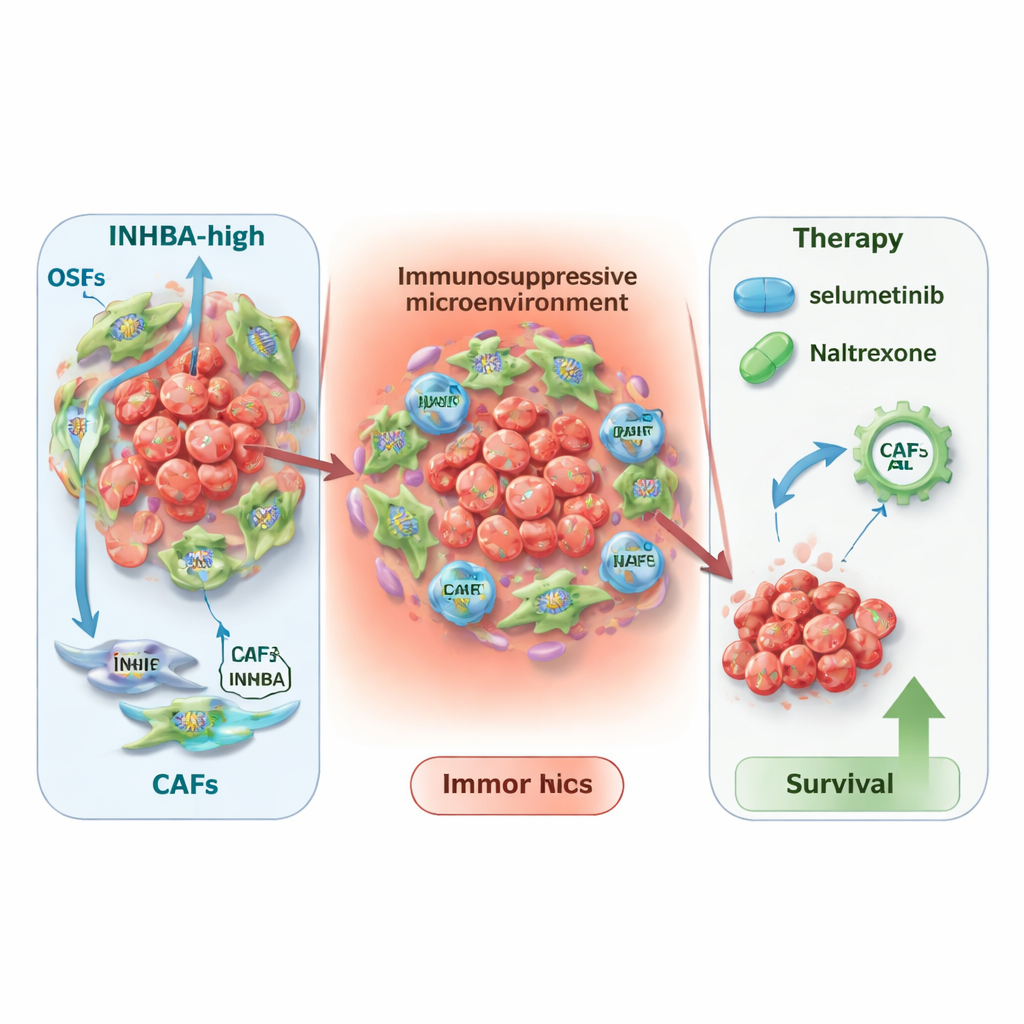
Novos ângulos de tratamento e impacto mais amplo
Sabendo que o INHBA marca um ambiente tumoral mais perigoso, os pesquisadores investigaram como isso poderia orientar a terapia. Em pacientes que receberam imunoterapia, níveis baixos de INHBA estiveram ligados a melhores desfechos com medicamentos comuns que visam PD‑L1 ou CTLA4, enquanto níveis altos de INHBA pareciam prever maior benefício de abordagens com células CAR‑T. Ao minerar dois grandes bancos de dados de resposta a medicamentos, também identificaram dois fármacos existentes — selumetinibe e naltrexona — como particularmente promissores em tumores com alto INHBA. Modelagem computacional mostrou que ambos os medicamentos poderiam se ligar fortemente à proteína INHBA, sugerindo um efeito direto. Finalmente, uma análise pan‑câncer revelou que INHBA está elevado e associado a pior sobrevida em muitos outros tipos de tumor, indicando que sua importância se estende além do câncer de boca.
O que isso significa para os pacientes
Em termos simples, este estudo identifica o INHBA como um gene “chave mestra” que ajuda tumores de boca letais a crescer, se espalhar e escapar do sistema imunológico, agindo em grande parte por meio de células de suporte especializadas em vez das células cancerosas sozinhas. Mensurar INHBA nos tumores poderia auxiliar médicos a identificar pacientes de alto risco, prever quem se beneficiará de diferentes tipos de imunoterapia e escolher drogas direcionadas que podem funcionar melhor nesse contexto. Como o INHBA desempenha um papel prejudicial semelhante em vários outros cânceres, terapias direcionadas a esse gene e aos fibroblastos parceiros poderiam, em última instância, beneficiar um amplo espectro de pacientes, aproximando o cuidado de um tratamento mais preciso e personalizado.
Citação: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Palavras-chave: carcinoma espinocelular oral, INHBA, microambiente tumoral, fibroblastos associados ao câncer, imunoterapia