Clear Sky Science · pt
Obinutuzumabe induz desestabilização lisossomal via inibição dependente de esfingomielina de TRPML2
Por que essa história de anticorpo importa
Para muitas pessoas com linfomas de células B, os modernos medicamentos à base de anticorpos transformaram um diagnóstico outrora invariavelmente fatal em uma doença tratável. No entanto, nem todos os anticorpos são iguais: alguns matam células cancerosas de forma mais potente e consistente do que outros. Este artigo investiga por que um desses fármacos, o obinutuzumabe, é melhor em matar diretamente células de linfoma do que seu predecessor rituximabe, focando em um culpado inesperado no interior da célula — os próprios centros de reciclagem celular, chamados lisossomos, e um delicado equilíbrio de lipídios e canais iônicos em suas membranas.
Do alvo na superfície à autodestruição interna
Tanto o rituximabe quanto o obinutuzumabe reconhecem o mesmo alvo nas células B, uma proteína chamada CD20. Mas os autores mostram que o obinutuzumabe é internalizado pela célula muito mais rápido e de forma mais eficiente. Uma vez ligado ao CD20 na superfície da célula cancerosa, os complexos anticorpo–receptores são puxados para dentro por um processo endocítico e entregues a compartimentos ácidos, incluindo os lisossomos. Lá, o obinutuzumabe desencadeia a permeabilização da membrana lisossomal: a membrana normalmente resistente torna‑se permeável, permitindo que enzimas digestivas, como catepsinas, vazem para o citosol e acionem vias de morte celular. Alterações no equilíbrio de sal e água desses compartimentos, que fazem os lisossomos inchar, amplificaram muito esse efeito letal.
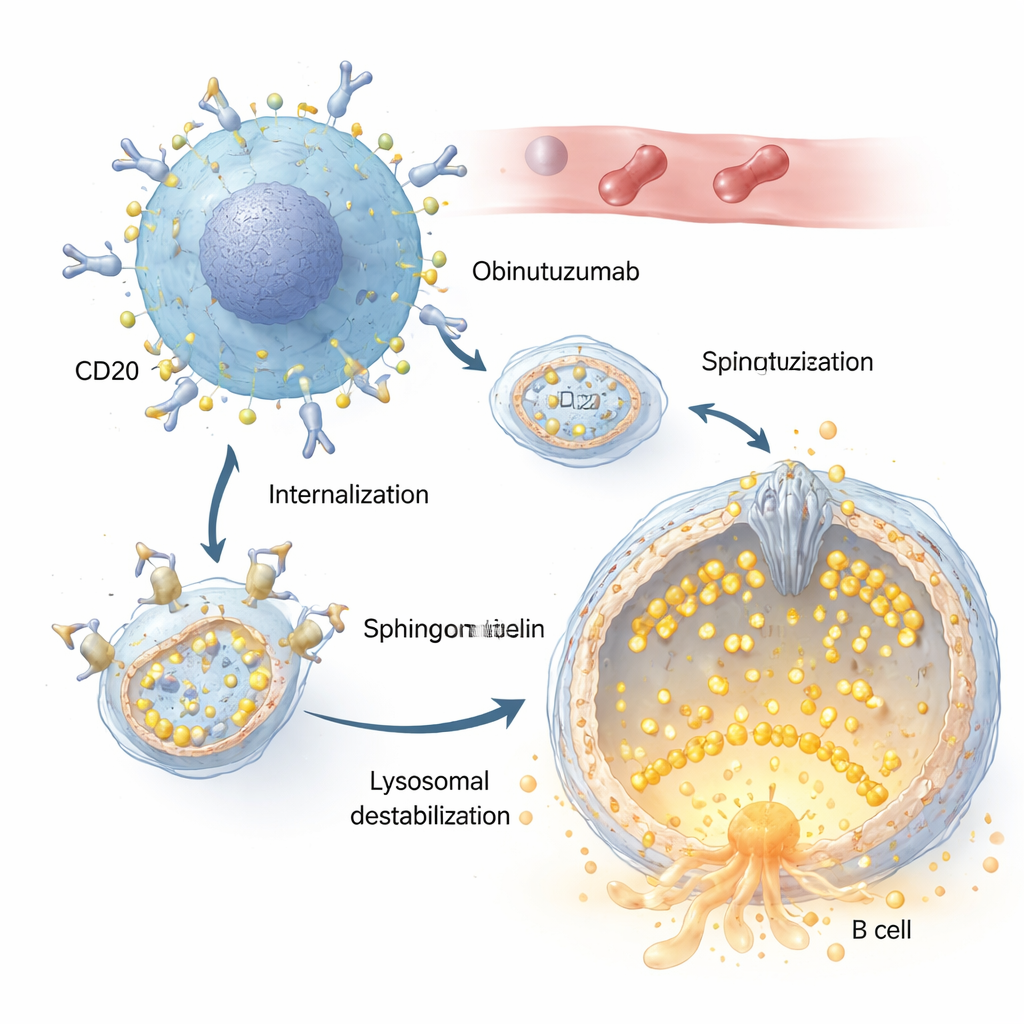
O papel de um minúsculo canal guardião
O elemento central dessa história é o TRPML2, um canal de cálcio embutido na membrana lisossomal. Em condições normais, o TRPML2 ajuda os lisossomos a lidar com estresse mecânico e osmótico liberando cálcio, o que sustenta a reparação da membrana, o tráfego intracelular e o controle de volume. Usando uma combinação de corantes fluorescentes de cálcio e versões do TRPML2 projetadas para detectar cálcio, os pesquisadores mostram que o obinutuzumabe fecha rapidamente esse canal: em minutos após o tratamento, um composto que normalmente ativa canais TRPML deixa de produzir o estouro de cálcio. Abordagens genéticas que reduzem os níveis de TRPML2, ou inibidores de pequenas moléculas que bloqueiam a atividade dos TRPML, tornam as células de linfoma mais vulneráveis ao obinutuzumabe, levando a mais vazamento lisossomal e maiores taxas de morte celular direta.
Como os lipídios da membrana desequilibram a balança
O estudo então investiga o que liga a captação do anticorpo ao fechamento do canal. A atenção se volta para a esfingomielina, um lipídio abundante nas membranas celulares e conhecido por interferir nos canais TRPML. Usando uma sonda fluorescente que se liga à esfingomielina, os autores constatam que vesículas contendo obinutuzumabe são ricas em esfingomielina quando alcançam compartimentos ácidos, muito mais do que vesículas com rituximabe. Quando as células são tratadas com esfingomielinase, uma enzima que corta a esfingomielina, a atividade de liberação de cálcio do TRPML2 é restaurada mesmo na presença do obinutuzumabe. Nestas condições, os lisossomos têm menos tendência a vazar e menos células morrem, o que sugere fortemente que o acúmulo de esfingomielina desativa o TRPML2 e prepara os lisossomos para rupturas.
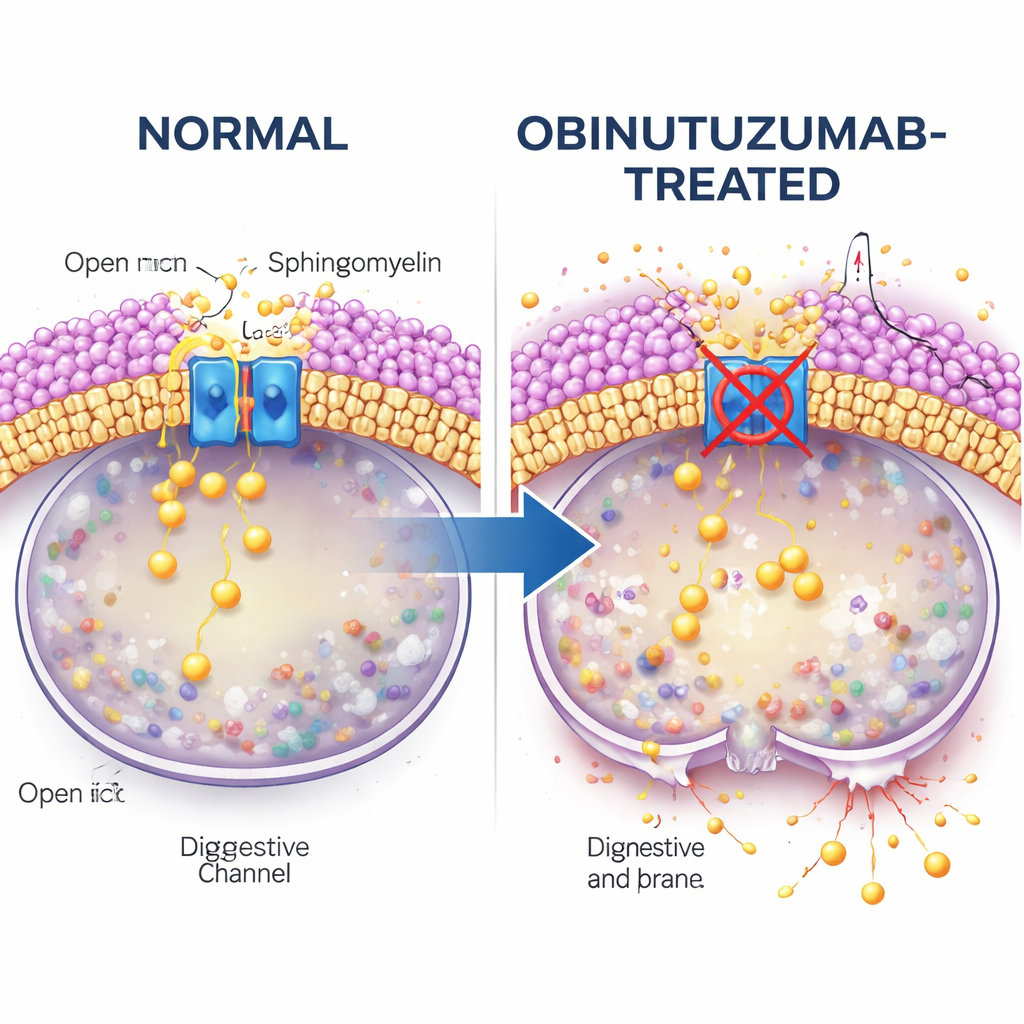
Rotas de tráfego e pontos de verificação do colesterol
A rota que o obinutuzumabe segue até o interior da célula também importa. Microscopia eletrônica e marcação do anticorpo sensível ao pH revelam que o obinutuzumabe sai da superfície celular e entra em vesículas intracelulares mais rapidamente do que o rituximabe. Quando os pesquisadores interferem em rotas específicas de captação, descobrem que bloquear uma forma de endocitose dependente de colesterol (com um composto chamado filipina) impede o obinutuzumabe de desligar o TRPML2 e reduz parcialmente o dano lisossomal e a morte celular. Outros inibidores de endocitose não produzem esse efeito protetor. Isso aponta para uma via especializada, rica em colesterol e esfingomielina, que entrega o obinutuzumabe aos lisossomos de modo a promover a inibição do TRPML2 e a subsequente desestabilização da membrana.
O que isso significa para tratamentos futuros contra o câncer
Em termos simples, este trabalho mostra que o obinutuzumabe mata linfomas de células B tão eficientemente porque força seus lisossomos a um estado frágil. Ao direcionar complexos anticorpo–CD20 para compartimentos ricos em esfingomielina, o fármaco desliga indiretamente um canal de cálcio protetor, o TRPML2. Sem essa salvaguarda, os lisossomos têm mais probabilidade de romper sob estresse, liberando enzimas corrosivas que desmontam a célula cancerosa por dentro. Entender esse eixo lipídio–canal iônico vai além de explicar por que o obinutuzumabe supera o rituximabe; também sugere novas estratégias para fortalecer terapias com anticorpos — por exemplo, combinando‑as com drogas que alterem esfingolipídios ou aumentem a atividade do TRPML2 para ajustar quando e como os lisossomos das células tumorais se autodestruirão.
Citação: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Palavras-chave: obinutuzumabe, linfoma de células B, lisossomo, esfingomielina, TRPML2