Clear Sky Science · pt
Engenharia de criogéis funcionalizados com polietilenimina–metal para melhor retenção, atividade e durabilidade a longo prazo da catalase
Por que manter enzimas no lugar é importante
O peróxido de hidrogênio é um subproduto químico comum em tudo, desde processamento de alimentos até tratamentos médicos, e as células vivas dependem da enzima catalase para degradá‑lo em água e oxigênio inofensivos. Na indústria, porém, a catalase costuma ser usada em forma livre e dissolvida, que perde atividade rapidamente, não pode ser recuperada com facilidade e precisa ser substituída frequentemente. Este estudo explora uma forma de "estacionar" a catalase dentro de um material semelhante a uma esponja para que ela permaneça ativa por mais tempo, seja reutilizável muitas vezes e opere de forma mais eficiente — tudo isso pode reduzir custos e tornar processos baseados em enzimas mais limpos e sustentáveis.

Construindo uma esponja inteligente
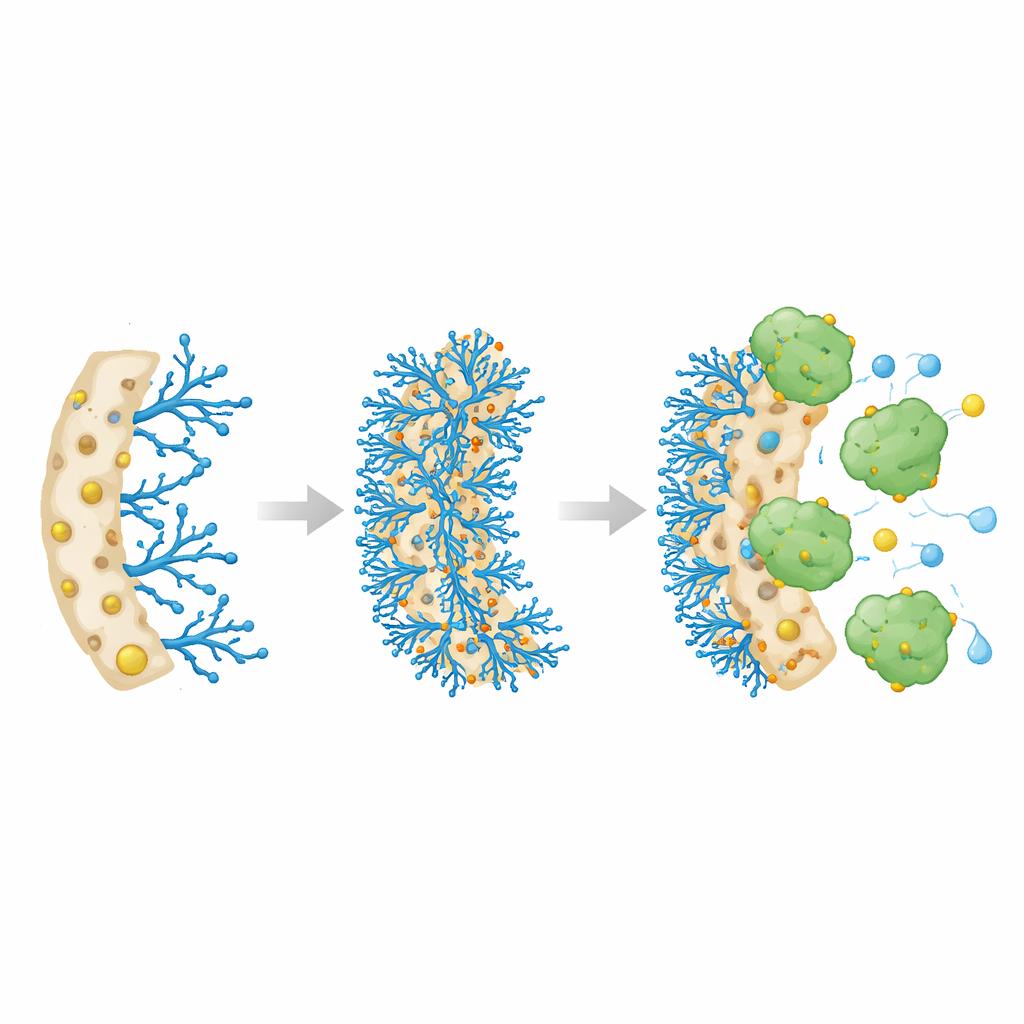
Os pesquisadores projetaram uma esponja polimérica especial, chamada criogel, formada por congelamento e descongelamento de uma mistura líquida de modo que os cristais de gelo esculpem grandes poros interconectados. Esses poros permitem que líquidos fluam livremente, como água passando por uma bucha, enquanto a estrutura sólida permanece resistente e elástica. A equipe usou um material base chamado Poli(HEMA-co-GMA) e, em seguida, graftou quimicamente sobre ele uma molécula ramificada rica em grupos de nitrogênio, a polietilenimina (PEI). Por fim, ligaram íons metálicos — cobre, níquel ou cobalto — a esses sítios de nitrogênio. A ideia era que os íons metálicos atuassem como pontos de ancoragem que atraíssem e mantivessem firmemente as moléculas de catalase no lugar, sem bloquear o fluxo de líquido através da esponja.
Ajustando o material para melhor desempenho
Para entender como cada etapa do projeto alterava o material, a equipe usou várias técnicas laboratoriais para sondar sua estrutura, química e estabilidade. Demonstraram que adicionar PEI e depois metais não colapsou a rede porosa, mas na verdade aumentou a capacidade da esponja de reter água, o que é bom para manter as enzimas em condições favoráveis e ativas. Entre os três metais, o cobre produziu o ambiente mais hidratado e bem organizado. Imagens de microscopia revelaram que o material original parecia grânulos compactos, enquanto as versões tratadas com PEI e metais abriram‑se em uma rede mais limpa e contínua de poros grandes. Medições do teor de metal confirmaram que o cobre se ligou com maior afinidade e em quantidades mais altas do que o níquel ou o cobalto, sugerindo que ele forneceria os pontos de ancoragem mais eficazes para a catalase.
Fixando a catalase no lugar
Quando a catalase foi introduzida nas diferentes esponjas contendo metal, todas as três capturaram rapidamente a enzima, mas a versão com cobre destacou‑se. Ela carregou a maior quantidade de catalase — cerca de 392 miligramas por grama de esponja seca — e atingiu um nível estacionário em aproximadamente oito horas. Em seguida, os pesquisadores examinaram quão bem a enzima imobilizada funcionava em comparação com a catalase livre em solução. Embora a velocidade máxima de reação por grama de enzima tenha diminuído um pouco, a catalase imobilizada mostrou uma atração aparente muito maior pelo seu substrato, o peróxido de hidrogênio. Em termos práticos, isso significa que a enzima ligada realizou seu trabalho de forma mais eficiente em níveis mais baixos de substrato, provavelmente porque o criogel poroso e hidratado com cobre concentrava o substrato perto da enzima e ajudava a manter sua conformação ativa.
Enzima que perdura
Uma das maiores vantagens de imobilizar enzimas é a promessa de reutilização e longa vida útil em prateleira. Aqui, a catalase ligada ao criogel à base de cobre mostrou‑se muito mais durável do que sua contraparte livre. Após 15 ciclos de uso repetidos, a enzima imobilizada ainda manteve cerca de um terço de sua atividade inicial, enquanto a catalase livre tipicamente seria descartada após um único uso. Em testes de armazenamento à temperatura de geladeira por 70 dias, a catalase imobilizada conservou mais de 60% de sua atividade, aproximadamente o dobro da enzima livre. A esponja também permitiu que a enzima fosse desprendida e recarregada várias vezes usando uma solução salina simples, mostrando que o próprio material pode ser reutilizado sem perda significativa de capacidade.
O que isso significa para o uso no mundo real
Para quem não é especialista, a conclusão principal é que os pesquisadores construíram uma espécie de "esponja de enzima" reutilizável que segura a catalase de forma firme, mas suave, ajudando‑a a trabalhar melhor em níveis químicos mais baixos e a durar muito mais em uso e armazenamento. Ao emparelhar um criogel altamente poroso com PEI e íons de cobre, eles criaram uma plataforma que combina alta carga de enzima, eficiência aprimorada e forte estabilidade de longo prazo. Materiais desse tipo poderiam ser integrados a sistemas industriais ou ambientais para degradar peróxido de hidrogênio e substâncias relacionadas de forma mais confiável e com menos desperdício, oferecendo um passo prático rumo a tecnologias enzimáticas mais verdes.
Citação: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Palavras-chave: imobilização de enzimas, catalase, criogel, polímeros funcionalizados com cobre, biocatálise