Clear Sky Science · pt
Carregamento crônico de NH4Cl melhora a tolerância à glicose sem alterar a sensibilidade à insulina em camundongos
Por que o equilíbrio ácido–base importa para o açúcar no sangue
Pessoas com doença renal crônica frequentemente desenvolvem uma condição chamada acidose metabólica, em que o sangue fica ligeiramente mais ácido do que o normal. Médicos normalmente veem isso como prejudicial, em parte porque episódios agudos de acidose são conhecidos por piorar o controle glicêmico. Este estudo inverte essa ideia: em camundongos, uma acidose branda e de longa duração na verdade melhorou a forma como o organismo lida com o açúcar, sem tornar o hormônio insulina mais ou menos eficaz. Entender essa surpresa pode, no futuro, ajudar a aprimorar tratamentos tanto para doença renal quanto para diabetes tipo 2.
Um desafio ácido de longo prazo em camundongos
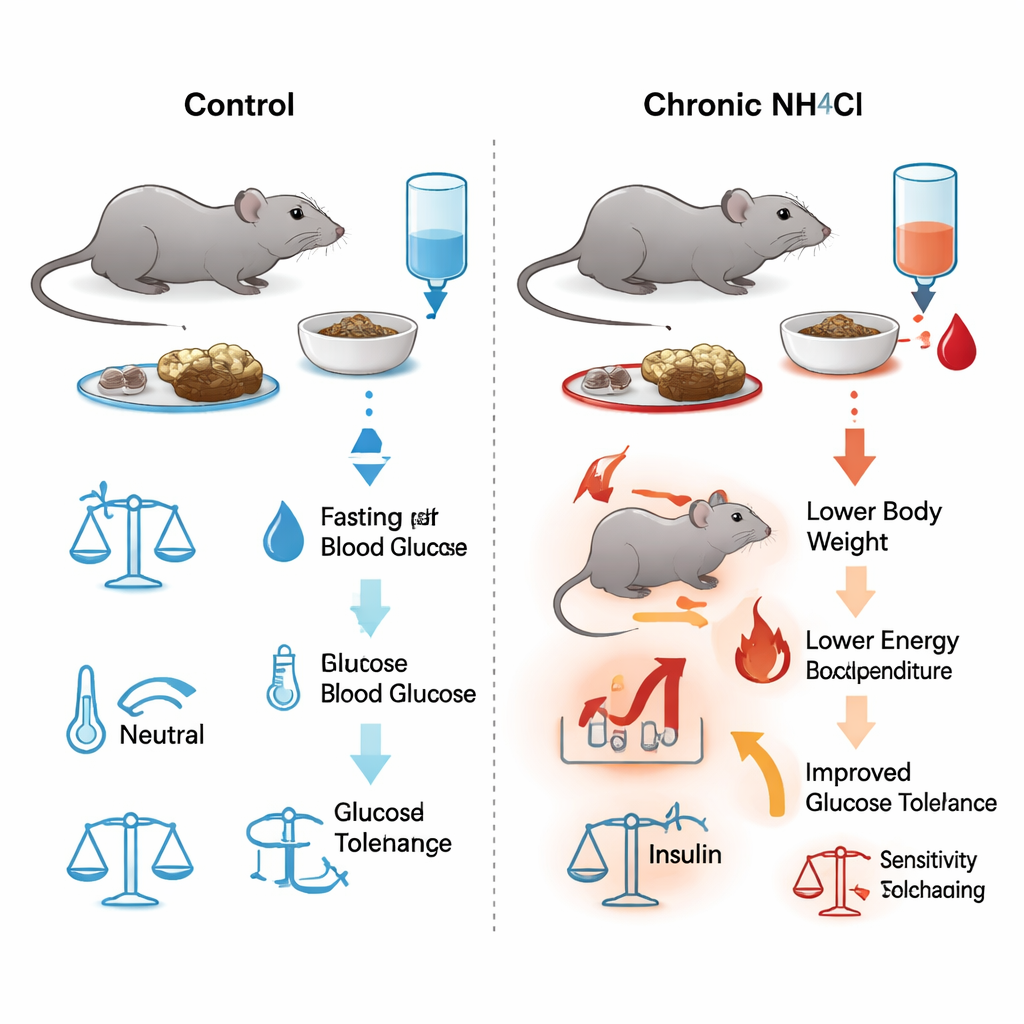
Os pesquisadores deram a camundongos machos água potável contendo cloreto de amônio, um sal que acidifica levemente o sangue, por até seis meses. Esse tratamento imita a carga ácida crônica observada na doença renal. Exames de sangue confirmaram uma acidose metabólica persistente e leve: pH e bicarbonato mais baixos, cloreto mais alto e, por outro lado, medidas relacionadas ao rim, como ureia e hematócrito, estáveis. Apesar de comerem e beberem tanto quanto ou mais que os camundongos não tratados, os animais submetidos à carga ácida pararam de ganhar peso após cerca de dois meses. Medições detalhadas em gaiolas metabólicas mostraram que esses camundongos queimavam mais energia no geral, tinham menos massa magra (rica em músculo) e carregavam relativamente mais gordura, indicando um custo metabólico de vida maior sob acidose crônica.
Melhor controle glicêmico sem mais ajuda da insulina
A equipe testou repetidamente quão bem os camundongos eliminavam o açúcar da corrente sanguínea ao injetar glicose e monitorar os níveis ao longo do tempo. Já na primeira semana após o início da bebida acidificante, os camundongos tratados reduziram sua glicemia mais rápido que os controles, e essa vantagem persistiu em muitos pontos ao longo de até 180 dias. A glicemia de jejum foi consistentemente menor no grupo acidótico. No entanto, quando os cientistas mediram a insulina no sangue durante esses testes, os níveis foram iguais em ambos os grupos. Testes separados em que os camundongos receberam insulina diretamente mostraram que a sensibilidade geral à insulina também não mudou. Em outras palavras, a acidose crônica melhorou a tolerância à glicose sem exigir que o pâncreas produzisse mais insulina ou que os tecidos respondessem com mais intensidade a ela.
Mudança de onde e como o açúcar é produzido e perdido
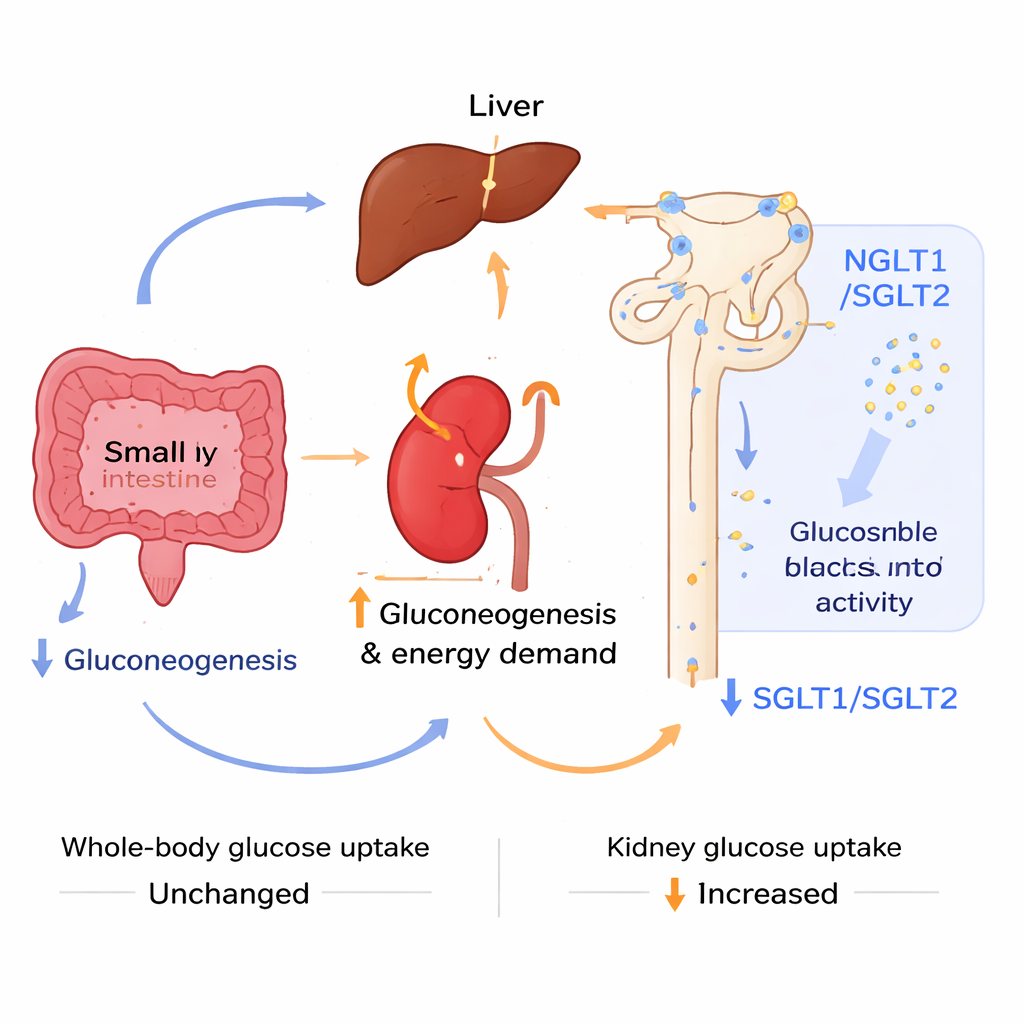
Para descobrir de onde vinha o controle glicêmico extra, os pesquisadores investigaram como diferentes órgãos produziam glicose. Eles usaram substâncias específicas — piruvato, alanina e glutamina — que alimentam vias de produção de glicose no fígado, rim e intestino. Com o tempo, o fígado e partes do intestino dos camundongos acidóticos tornaram-se menos ativos na produção de nova glicose, especialmente a partir de alanina e glutamina. Em contraste, o rim mostrou sinais de trabalhar mais: genes-chave envolvidos na produção de glicose e no suprimento de energia foram ativados, e imagens com um análogo radioativo da glicose revelaram maior captação de açúcar nos rins e na bexiga, embora a captação total pelo corpo permanecesse inalterada. Ao mesmo tempo, mais glicose foi perdida na urina após uma carga de açúcar, porque os principais transportadores sódio–glicose do rim, que normalmente recuperam a glicose filtrada, estavam reduzidos tanto no nível de RNA quanto de proteína. Essa combinação — menos açúcar produzido por fígado e intestino, mais açúcar consumido e excretado pelo rim — ajudou a manter os níveis sanguíneos sob controle.
Mudanças profundas dentro das células renais
Instantâneos da atividade gênica nos rins durante os primeiros dois meses de tratamento mostraram uma ampla remodelação da maquinaria celular. Vias envolvidas no transporte de partículas carregadas (ânions), recuperação de bicarbonato e funcionamento de mitocôndrias e fosforilação oxidativa — os principais geradores de energia da célula — foram reforçadas. Genes ligados ao metabolismo de glicose e lipídios também se alteraram para cima, enquanto algumas vias imunes e de desintoxicação, incluindo partes do sistema complemento e da família citocromo P450, foram suprimidas. Esses padrões são compatíveis com um rim que está trabalhando mais para excretar ácido, consumindo mais combustível e, ao mesmo tempo, reprogramando como lida com glicídios e lipídios para atender à demanda energética extra.
O que isso significa para pessoas com problemas renais e glicêmicos
Em resumo, uma acidose metabólica leve e de longa duração em camundongos não prejudicou o controle glicêmico — na verdade, o melhorou — ao reduzir a produção de glicose no fígado e no intestino, diminuir a reabsorção de glicose no rim e aumentar o uso de energia pelo próprio rim. A insulina em si não teve um papel maior do que o habitual. Isso não significa que a acidose seja benéfica ou que pacientes devam permanecer acidóticos; a acidose continua a ter muitos efeitos nocivos. Mas os achados revelam que o organismo pode se adaptar de maneiras inesperadas e destacam o rim como um regulador poderoso da glicemia. Trabalhos futuros podem ser capazes de aproveitar alguns desses mecanismos renais — como o aumento da perda urinária de glicose e a alteração da produção de glicose — sem expor os pacientes aos riscos da acidose crônica.
Citação: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Palavras-chave: acidose metabólica, tolerância à glicose, função renal, gluconeogênese, risco de diabetes tipo 2