Clear Sky Science · pt
Modelagem de célula inteira prevê estratégias alternativas de alocação de proteoma no arqueano Methanococcus maripaludis
Por que pequenos produtores de metano importam
Methanococcus maripaludis é um arqueano microscópico que ajuda a transformar químicos simples como dióxido de carbono e formiato em metano, um componente importante do gás natural. Entender como esse microrganismo distribui seus recursos internos — especialmente suas proteínas — pode revelar regras gerais da vida sob limitação de energia e orientar esforços para aproveitá‑lo como uma fábrica biológica de metano ou como plataforma para química sustentável.
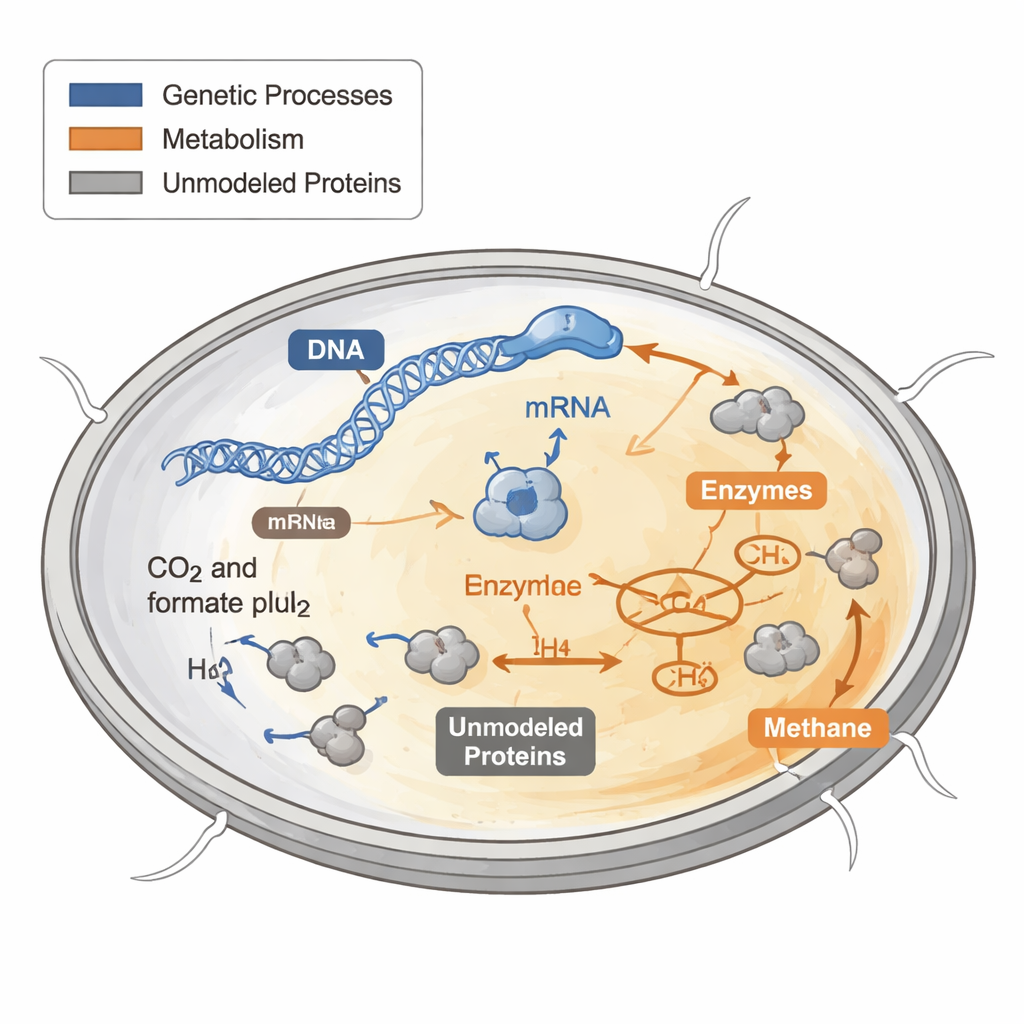
Como as células gastam seu orçamento de proteínas
Cada célula precisa decidir como gastar seu limitado “orçamento” de proteínas. Algumas proteínas constroem novas partes celulares, outras capturam energia e outras realizam tarefas de manutenção. Modelos computacionais anteriores do metabolismo tratavam essas proteínas como se fossem gratuitas e ilimitadas, o que funciona mal quando se tenta prever crescimento em condições adversas ou pobres em nutrientes. Em bactérias e leveduras, experimentos mostraram que células de crescimento rápido dedicam uma fatia maior do orçamento proteico aos ribossomos, as máquinas moleculares que sintetizam novas proteínas, enquanto células de crescimento lento deslocam recursos para outras funções.
Um arqueano que quebra as regras
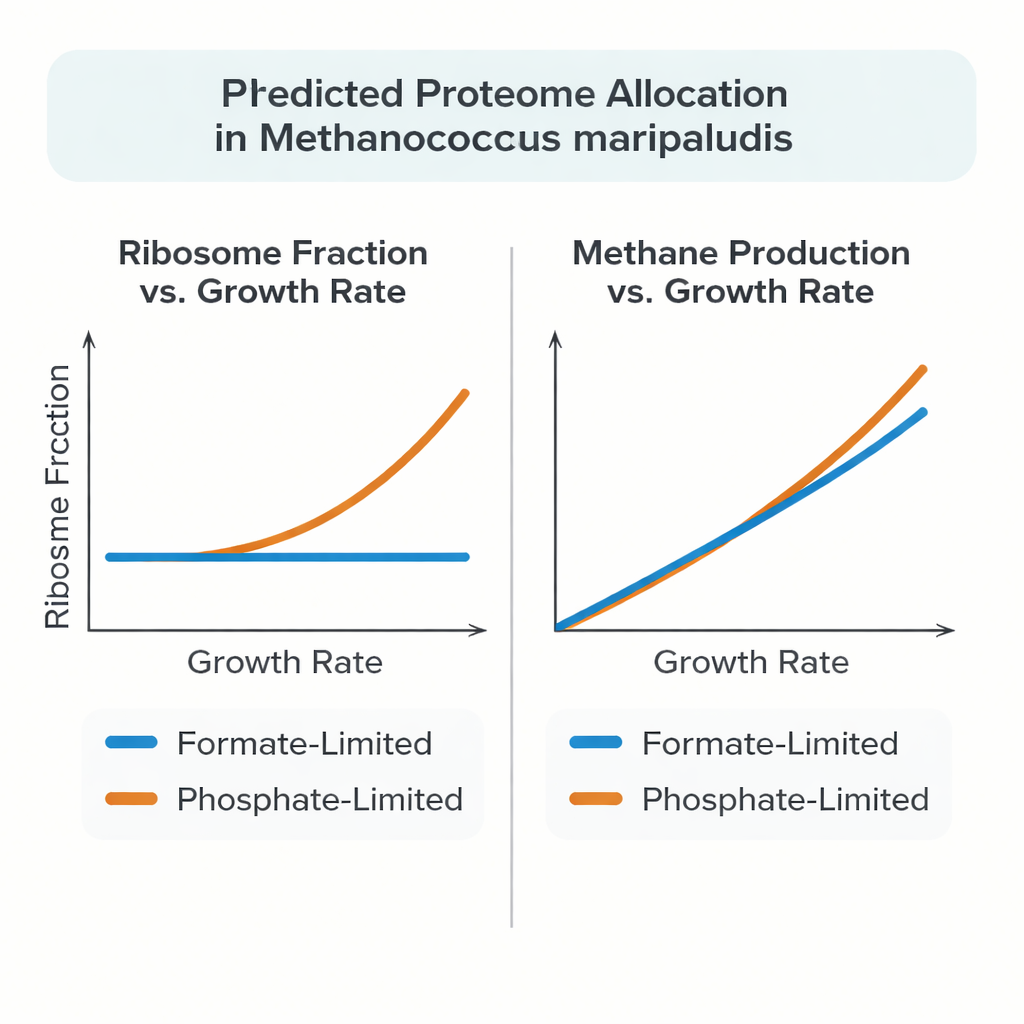
Experimentos recentes revelaram que M. maripaludis nem sempre segue esse padrão. Quando cresce usando formiato como fonte tanto de carbono quanto de energia, a fração do orçamento proteico investida em ribossomos permanece quase constante à medida que o crescimento diminui. Sob limitação de fosfato, no entanto, o arqueano comporta‑se de forma mais convencional: a fração de ribossomos aumenta com a taxa de crescimento, semelhante a Escherichia coli e leveduras. Para explicar esse comportamento incomum, os autores construíram um modelo detalhado no estilo “célula inteira” que conecta o metabolismo ao processo custoso de fabricar e montar proteínas e RNA, em vez de tratar proteínas como simples taxas de reação abstratas.
Construindo um modelo no estilo célula inteira
Os pesquisadores partiram de um mapa metabólico existente de M. maripaludis e sobrepuseram milhares de reações adicionais que descrevem a expressão gênica: copiar DNA em RNA, carregar RNAs de transferência, montar ribossomos e complexos enzimáticos, e diluir esses componentes durante a divisão celular. Eles coletaram limites de velocidade enzimática em bancos de dados bioquímicos e na literatura, e estimaram quanto da massa proteica é composta por proteínas “não modeladas” que não estão diretamente ligadas às reações do mapa. Em seguida, impuseram restrições globais que limitam a massa total de proteína e RNA, vinculam taxas de reação à quantidade de enzima disponível e amarram a produção de proteína à capacidade dos ribossomos. Com essas restrições, o modelo precisa escolher como alocar um orçamento proteico fixo para sustentar o crescimento.
O que as simulações revelaram
Quando testado contra experimentos de quimostato de alta qualidade, o modelo reproduziu com precisão as massas medidas de proteína e RNA, as taxas de produção de metano e os rendimentos de crescimento ao longo de uma faixa de taxas de crescimento lentas. Sob limitação de formiato, a célula simulada naturalmente passou a manter uma fração de proteína ribossomal quase constante conforme o crescimento variava, espelhando os dados experimentais. Sob limitação de fosfato, o modelo igualou o aumento observado na fração de ribossomos somente quando os ribossomos puderam trabalhar mais rápido em baixas taxas de crescimento, consistente com medições que mostram mais ribossomos ativamente engajados na síntese de proteínas. O modelo também sugeriu que uma parcela substancial da proteína em M. maripaludis não é estritamente necessária para o crescimento mínimo, e que carbono e energia em excesso podem ser armazenados ou desviados para outras moléculas grandes, como glicogênio ou aminoácidos livres, dependendo de qual nutriente está limitando.
Sondando mutantes e limites de crescimento
Como o modelo contabiliza explicitamente o custo proteico de cada via, ele pode prever não apenas se mutantes genéticos crescem, mas quão bem crescem em relação ao tipo selvagem. Os autores simularam linhagens sem diferentes enzimas de processamento de hidrogênio e compararam a aptidão prevista com medições laboratoriais em várias condições de crescimento, incluindo presença ou ausência de hidrogênio e monóxido de carbono. Em muitos casos, o modelo capturou se os mutantes podiam crescer e produziu estimativas razoáveis de suas taxas de crescimento relativas, melhorando modelos anteriores que só podiam dar respostas sim/não. A mesma estrutura foi usada para estimar taxas de crescimento máximas possíveis em condições de batelada para diferentes combinações de substratos.
O que isso significa para a ciência e a tecnologia
Em termos práticos, este estudo mostra que M. maripaludis usa uma estratégia alternativa para orçar sua força de trabalho proteica, mantendo suas “fábricas” de proteína funcionando com uma parcela estável do orçamento em algumas condições em vez de reduzi‑las à medida que o crescimento desacelera. Ao incorporar esse comportamento em um modelo detalhado e orientado por dados, o trabalho fornece um campo de testes para explorar como microrganismos limitados por energia equilibram crescimento, manutenção e armazenamento. Para pesquisa aplicada, o modelo oferece um roteiro para engenhar esse arqueano para produzir mais metano ou outros produtos, identificando quais enzimas e vias são mais dispendiosas em termos de investimento proteico. Mais amplamente, ele estende a poderosa modelagem no estilo célula inteira além de bactérias e leveduras para o domínio arqueal, ajudando a preencher a lacuna entre detalhes moleculares e o comportamento em grande escala de comunidades microbianas envolvidas em clima, energia e biotecnologia industrial.
Citação: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Palavras-chave: Methanococcus maripaludis, alocação do proteoma, modelagem de célula inteira, metanogênese, metabolismo de archaea