Clear Sky Science · pt
Estratégias computacionais para desvendar insights de inibidores conhecidos para otimização adicional de candidatos: Um estudo de caso em análogos de Celecoxib
Por que pequenas mudanças em analgésicos importam
Os analgésicos modernos não apenas aliviam dores; eles ajustam a química do corpo de maneiras muito precisas. O celecoxib, um anti‑inflamatório popular, tem como alvo uma enzima envolvida na dor e no inchaço, poupando em grande parte uma enzima irmã que protege o estômago. Ainda assim, dezenas de parentes químicos próximos do celecoxib se comportam de maneira muito diferente no organismo. Este estudo usa modelagem computacional para fazer uma pergunta aparentemente simples, com grandes implicações para medicamentos mais seguros: quanto importa uma única pequena alteração em uma molécula?
A enzima que ativa a dor
Quando um tecido é lesionado ou inflamado, o corpo libera uma molécula gordurosa chamada ácido araquidônico. Uma enzima chamada COX‑2 converte essa molécula em prostaglandinas, que desencadeiam dor, febre e inchaço. Uma enzima relacionada, COX‑1, ajuda a proteger o revestimento do estômago e as plaquetas. Analgésicos mais antigos, como o ibuprofeno, atingem ambas as enzimas, aliviando a dor mas frequentemente irritando o trato gastrointestinal. O celecoxib foi projetado para encaixar-se em um bolso ligeiramente maior encontrado principalmente na COX‑2, bloqueando sinais de dor enquanto preserva grande parte da função protetora da COX‑1. Entender a forma detalhada desse bolso, e como as moléculas de droga se acomodam dentro dele, é central para projetar novos medicamentos que sejam ao mesmo tempo potentes e seguros.
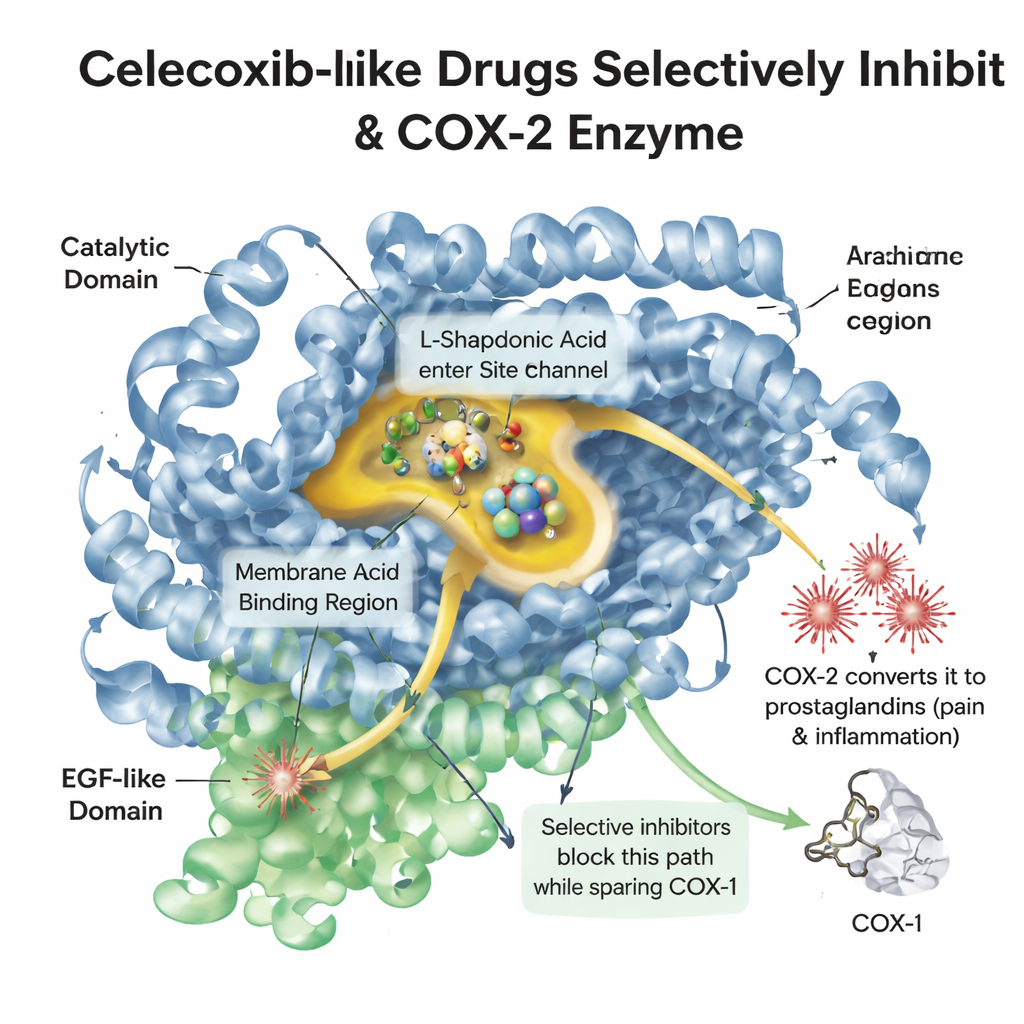
Uma biblioteca digital de drogas semelhantes
Os pesquisadores reuniram um conjunto de 375 moléculas que compartilham a estrutura básica de três anéis do celecoxib, mas diferem em pequenos detalhes, como a troca de um único átomo ou grupo lateral. Eles coletaram essas estruturas e suas forças medidas de bloqueio da COX‑2 a partir de um banco de dados público de fármacos. Usando software químico, geraram modelos 3D de cada molécula, calcularam quase 2.000 descritores numéricos de suas formas e propriedades, e então as acoplaram a uma estrutura de alta resolução da enzima COX‑2. No docking, um computador encaixa uma molécula no bolso da enzima de várias maneiras e atribui uma pontuação àqueles conformações que melhor se ajustam.
O que realmente controla potência e seletividade
A equipe concentrou-se em três regiões-chave do celecoxib. “Site‑1” é um anel que fica em uma região apolar do bolso; “Site‑2” é um anel com uma cauda rica em flúor; e “Site‑3” é um anel que carrega um grupo sulfonamida que forma ligações de hidrogênio fortes. A análise mostrou que o Site‑1 prefere grupos pequenos e não polares que preservem contatos hidrofóbicos; tornar essa região mais hidrofílica, por exemplo adicionando um –OH ou um grupo ácido, normalmente enfraquecia a droga. No Site‑2, pequenos grupos eletronegativos como o flúor frequentemente aumentavam a potência ao melhorar interações em um bolso apertado, enquanto caudas mais volumosas ou polares tendiam a prejudicar a atividade. No Site‑3, o nitrogênio da sulfonamida, capaz de doar uma ligação de hidrogênio, era crucial; substituí‑lo por uma versão sem capacidade de ligação reduzia de forma perceptível a afinidade.
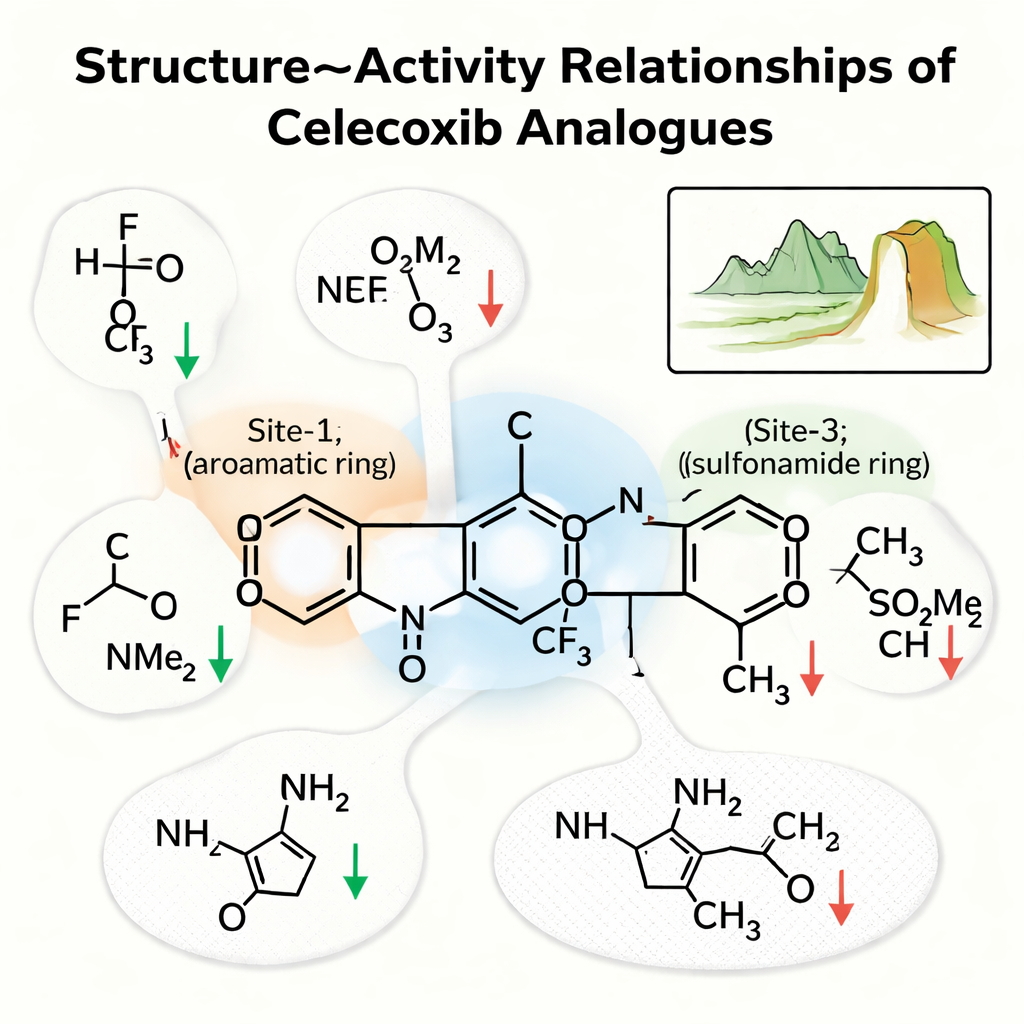
Penhascos na paisagem química
Para ir além de tendências simples, os autores construíram uma “paisagem estrutura–atividade”, que pergunta quanto a potência da droga salta quando a estrutura muda apenas um pouco. Nessa visão, a maioria dos compostos semelhantes ao celecoxib está sobre colinas suaves: ajustá‑los — por exemplo, deslocando um halogênio ou adicionando um pequeno grupo flexível — aumenta ou diminui a potência de maneiras previsíveis. Mas alguns pares formam “penhascos de atividade” acentuados, onde uma mudança minúscula, como trocar um grupo metil por um trifluorometil ou adicionar um único átomo de flúor, causa um ganho ou perda dramática de atividade. O estudo também realizou simulações completas de dinâmica molecular — filmes virtuais dos complexos droga‑enzima em movimento — que confirmaram que os melhores análogos permanecem estáveis no bolso por centenas de nanosegundos.
Guiando a próxima geração de analgésicos mais seguros
Para um leitor não especialista, a mensagem principal é que, no desenho de fármacos, os pequenos detalhes importam enormemente. Dois compostos que parecem quase idênticos no papel podem diferir em mil vezes na força com que bloqueiam a COX‑2, simplesmente porque um átomo extra melhora o encaixe em um bolso microscópico ou interrompe um contato chave. Ao mapear sistematicamente quais alterações ajudam ou prejudicam cada um dos três sítios-chave do celecoxib, e ao destacar os “penhascos” perigosos onde pequenos ajustes têm efeitos desproporcionais, este trabalho computacional oferece um roteiro para químicos. Indica caminhos para novos anti‑inflamatórios que mantenham a eficácia analgésica do celecoxib ao mesmo tempo que aumentam segurança e seletividade.
Citação: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Palavras-chave: inibidores de COX-2, análogos de celecoxib, anti-inflamatórios, projeto computacional de fármacos, relação estrutura-atividade