Clear Sky Science · pt
Avaliação preliminar da biodistribuição e do direcionamento da sonda molecular fluorescente Cy7-SYL3C em um modelo murino de câncer colorretal EpCAM-positivo
Por que isso importa para a detecção do câncer
O câncer colorretal é uma das principais causas de morte por câncer no mundo, em parte porque muitos tumores são detectados tardiamente. A principal ferramenta de rastreio atual, a colonoscopia, é eficaz, mas invasiva e desconfortável, por isso muitas pessoas a evitam. Este estudo explora um novo tipo de “traçador inteligente” luminoso que, no futuro, poderia ajudar médicos a ver tumores intestinais mais cedo e com mais clareza, usando luz em vez de um bisturi ou um longo tubo.
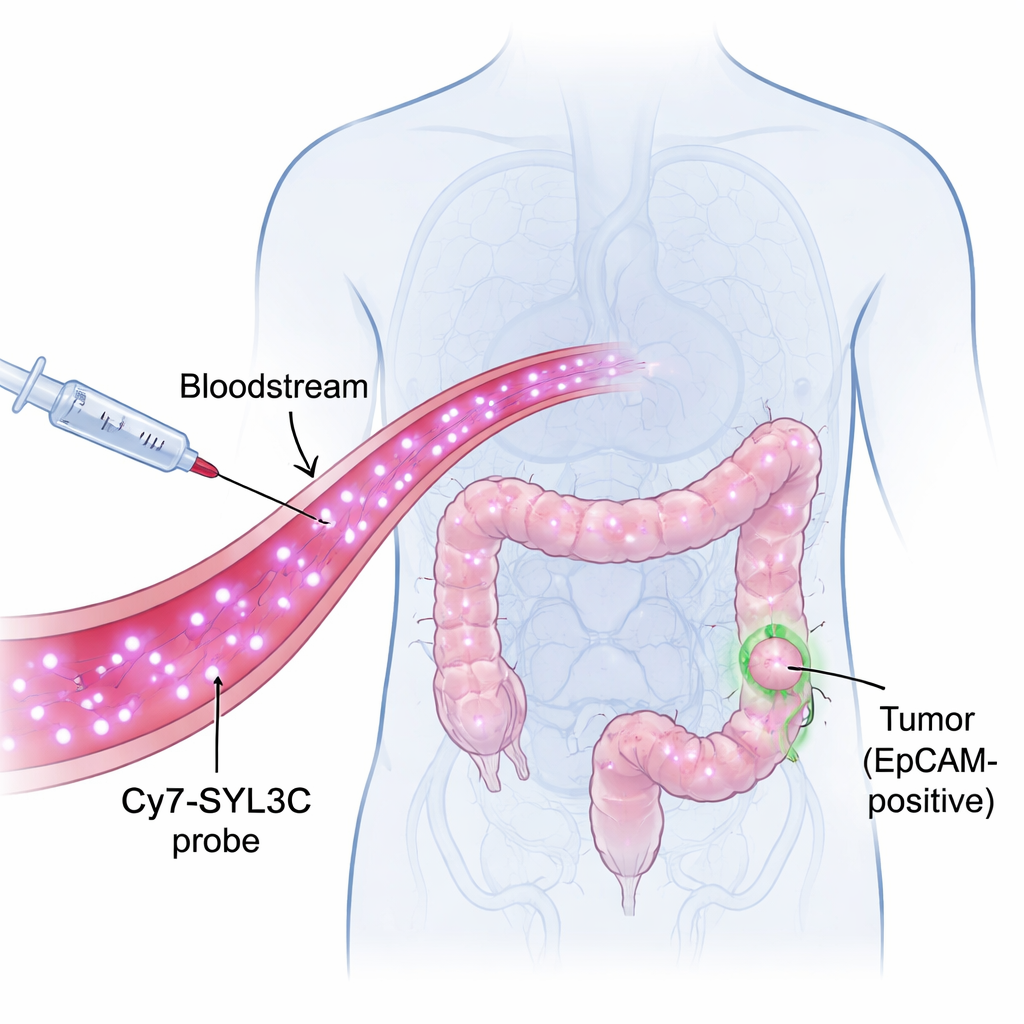
Uma etiqueta luminosa que reconhece células tumorais
Os pesquisadores concentraram-se em uma molécula chamada EpCAM, que se encontra na superfície de muitas células de câncer colorretal, mas é rara em tecidos saudáveis. Eles construíram uma sonda chamada Cy7-SYL3C ao ligar um corante no infravermelho próximo (Cy7) a uma curta sequência de DNA chamada aptâmero (SYL3C) que pode reconhecer EpCAM como uma chave encaixa numa fechadura. A luz no infravermelho próximo é invisível ao olho, mas pode penetrar vários milímetros no tecido, permitindo que câmeras captem sinais de dentro do corpo com alto contraste. A ideia é simples: injetar Cy7-SYL3C na corrente sanguínea, deixá-lo procurar células tumorais ricas em EpCAM e, em seguida, usar uma câmera especial para fazer essas células brilharem contra um fundo mais escuro.
Testando segurança e estabilidade no laboratório
Antes de testar a sonda em animais vivos, a equipe verificou se ela era estável e segura. Misturaram Cy7-SYL3C com soro sanguíneo de camundongos e bovinos e constataram que a maior parte da sonda permaneceu intacta por pelo menos oito horas, tempo suficiente para imageamento durante um procedimento médico. Em seguida, expuseram células humanas de câncer colorretal e células normais do cólon a diferentes concentrações da sonda. O crescimento celular permaneceu essencialmente inalterado e, quando a sonda foi misturada a glóbulos vermelhos, ela não os fez hemolisar. Esses testes sugerem que Cy7-SYL3C é quimicamente estável e pouco agressivo às células — requisitos chave para qualquer agente de imagem que possa ser usado em pacientes.
Para onde a sonda vai no corpo
Os cientistas acompanharam então o trajeto de Cy7-SYL3C em camundongos saudáveis usando um sistema de imageamento para pequenos animais. Logo após a injeção, o sinal mais forte apareceu no fígado e nos rins, órgãos que filtram e eliminam substâncias do sangue. O sinal no fígado atingiu o pico por volta de uma hora e depois diminuiu, enquanto os rins continuaram a brilhar por mais tempo, indicando a urina como via principal de eliminação da sonda. Após dois dias, restava apenas uma pequena fração do sinal original, e o exame microscópico dos principais órgãos não mostrou danos teciduais óbvios. Isso significa que a sonda é eliminada de forma relativamente rápida e não causa danos visíveis aos órgãos vitais neste estudo de curto prazo.
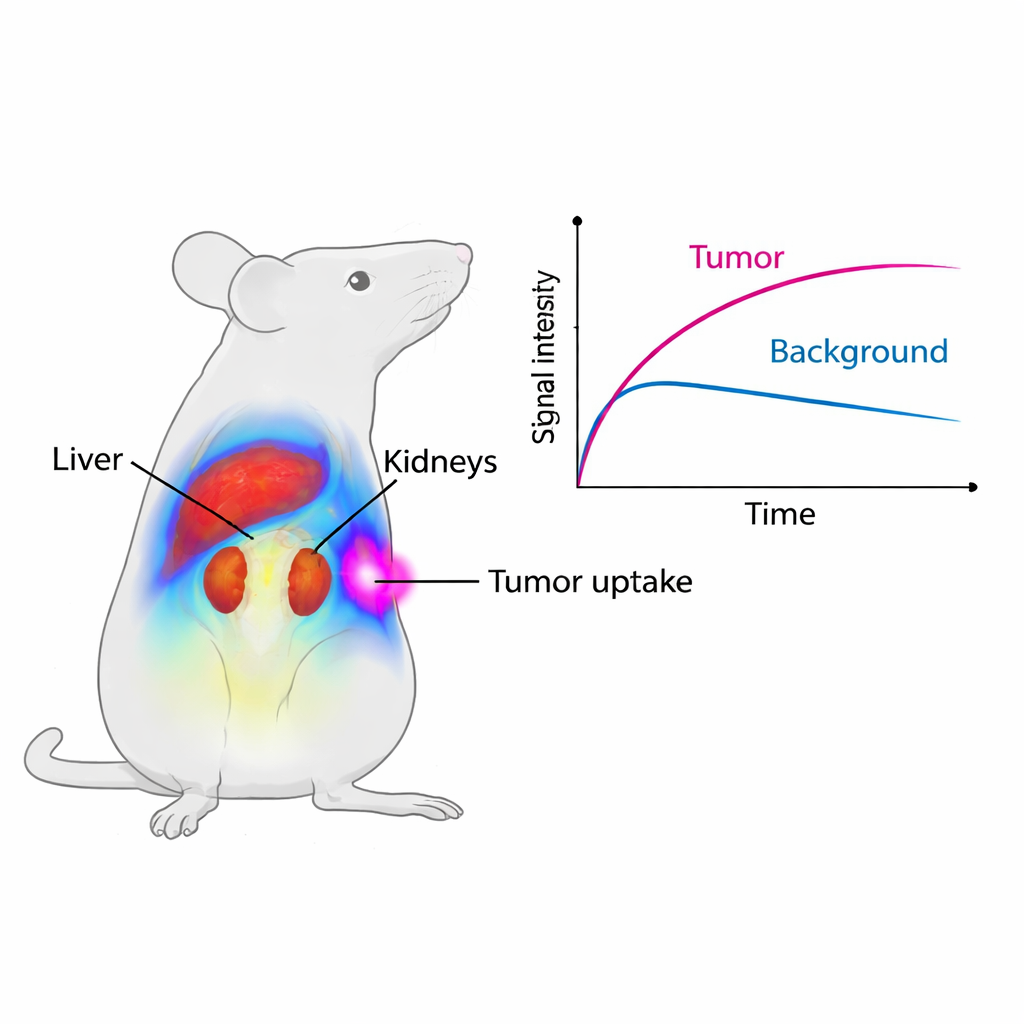
Focalizando tumores colorretais
Para verificar se Cy7-SYL3C realmente se dirige ao câncer, a equipe usou camundongos implantados com tumores humanos colorretais que expressam EpCAM. Em apenas cinco minutos após a injeção, os tumores começaram a brilhar no sistema de imageamento. Nas primeiras quatro horas, o sinal médio nos tumores foi quase duas vezes mais forte do que em camundongos cujos tumores haviam sido “pré-bloqueados” com um excesso de SYL3C não marcado, que ocupou temporariamente os sítios de EpCAM e impediu a sonda luminosa de se ligar. A razão entre o sinal tumoral e o músculo próximo ultrapassou um e atingiu pico por volta de oito horas, o que significa que os tumores ficaram claramente mais brilhantes que o entorno durante uma janela útil para imageamento. Estudos microscópicos detalhados confirmaram que a sonda fluorescente se sobrepunha à marcação de EpCAM nas células tumorais, enquanto órgãos normais apresentaram pouco ou nenhum EpCAM.
Como isso pode orientar futuras cirurgias e diagnósticos
Para um leitor não especialista, a mensagem principal é que Cy7-SYL3C age como um corante inteligente que procura células de câncer colorretal e depois é em grande parte eliminado pelos rins. Parece estável, pouco agressivo às células e capaz de fazer tumores brilharem rapidamente e por várias horas, o que poderia ajudar cirurgiões a verem melhor as bordas do tumor em tempo real ou auxiliar radiologistas a identificar áreas suspeitas durante procedimentos minimamente invasivos. Embora esses resultados venham de experimentos iniciais em camundongos e mais trabalho seja necessário antes do uso em humanos, o estudo estabelece uma base importante para uma nova classe de traçadores baseados em luz que podem tornar a detecção e a cirurgia do câncer colorretal mais precisas e menos invasivas.
Citação: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Palavras-chave: imagem do câncer colorretal, fluorescência no infravermelho próximo, direcionamento EpCAM, Sonda aptâmero, orientação cirúrgica de tumores