Clear Sky Science · pt
Estratégia multidimensional permite diversidade metabolômica escalável em fermentações microbianas
Por que pequenos ajustes na “fábrica” importam para novos remédios
Muitos dos medicamentos atuais vêm de substâncias naturais produzidas por bactérias e fungos. Mas transformar um candidato promissor em laboratório num verdadeiro lead farmacológico frequentemente falha em uma etapa surpreendentemente prosaica: cultivar o mesmo microrganismo em um vaso diferente ou em maior escala. Este estudo faz uma pergunta simples, porém crucial — como manter a produção química de um microrganismo estável e diversificada ao transferi‑lo de pequenas placas de teste para frascos maiores e biorreatores? A resposta pode acelerar a busca pela próxima geração de antibióticos e outras terapias.
Três maneiras de cultivar o mesmo microrganismo
Os pesquisadores concentraram‑se em uma bactéria do solo, Streptomyces griseochromogenes, conhecida por produzir muitos “metabólitos secundários” — pequenas moléculas com potencial farmacológico. Eles compararam três sistemas de cultivo comuns usados em descoberta inicial: frascos agitados com baffes, microplacas de 48 poços em formato “flower” e um biorreator tipo tanque agitado. Em cada sistema mediram crescimento, morfologia e estrutura celular e, fundamentalmente, o padrão de sinais químicos detectados por espectrometria de massa, usado aqui como uma impressão digital do metaboloma secretado pela bactéria. Primeiro aplicaram uma regra clássica de engenharia: manter a disponibilidade de oxigênio igual entre os sistemas e esperar comportamento semelhante. Em vez disso, descobriram que curvas de crescimento, formas celulares e impressões químicas divergiam fortemente entre os vasos.
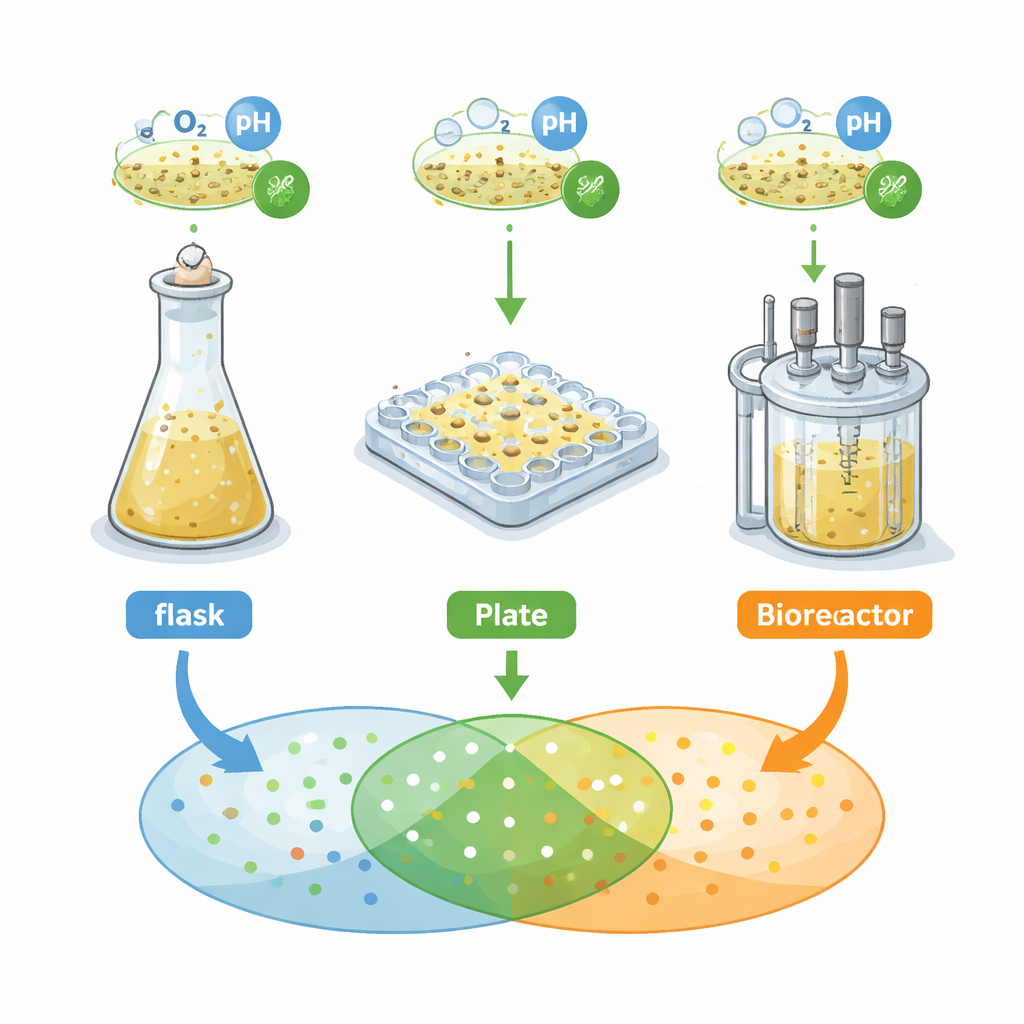
Quando uma regra não basta
Igualar apenas o oxigênio produziu “pegadas metabólicas” muito diferentes — os conjuntos de sinais de massa correspondentes a moléculas individuais. Apenas cerca de 18% dessas feições foram compartilhadas entre os três sistemas. As microplacas geraram muito mais sinais distintos do que os frascos ou o biorreator. A equipe então testou outra abordagem unidimensional, alterando ou a quantidade de etanol no meio (uma pequena molécula que pode induzir maior produção de metabólitos) ou a velocidade de agitação, que altera quanto oxigênio entra na cultura. Esses ajustes de uma dimensão melhoraram modestamente a sobreposição das pegadas químicas, mas apenas em mais ~18% ou algo próximo. Em outras palavras, receitas simples como “aumente o oxigênio” ou “adicione mais etanol” não garantem que um metabólito visto num poço minúsculo aparecerá de forma confiável em um fermentador maior.
Como a forma celular orienta a diversidade química
Para entender o que realmente importa, os autores reuniram dados de 80 cultivos diferentes e usaram um método estatístico que identifica fatores ocultos que moldam os resultados. Essa análise destacou dois temas principais: o próprio sistema de cultivo e a morfologia das células — se as bactérias cresciam como pelotas compactas, tapetes miceliais frouxos ou filamentos finamente dispersos. Condições que produziam morfologias semelhantes tendiam a produzir pegadas metabólicas mais parecidas e facilitavam a “escalagem” de moléculas de sistemas pequenos para o tanque agitado. Ao selecionar deliberadamente conjuntos de condições que geravam formas celulares comparáveis nos três sistemas, os pesquisadores aumentaram a sobreposição de feições químicas em cerca de 50% em comparação com a simples equalização de oxigênio.
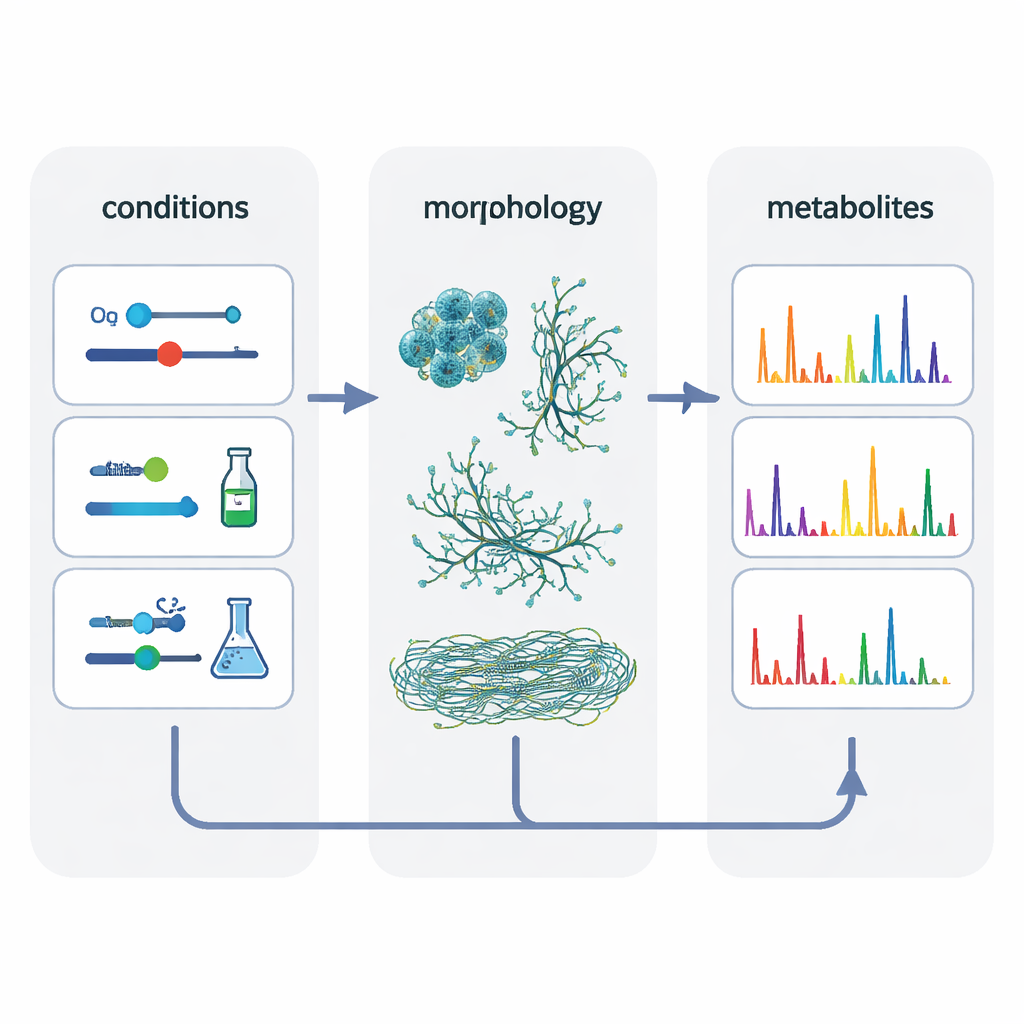
Famílias químicas ocultas e moléculas específicas de cada sistema
Além de contagens simples de sinais, a equipe construiu redes moleculares que agruparam feições de massa relacionadas em famílias de metabólitos estruturalmente semelhantes. Famílias grandes frequentemente continham ao menos um membro encontrado em todos os sistemas de cultivo, sugerindo uma química central resistente a mudanças de escala. Mas muitas famílias menores — e algumas moléculas individuais — apareceram apenas em um tipo de vaso. As microplacas de poliestireno, em particular, produziram a variedade mais rica de compostos, incluindo muitas variantes de sideróforos quelantes de ferro chamados desferrioxaminas e vários peptídeos não ribossomais. Os autores sugerem que estresses sutis nessas placas, como níveis mais altos de espécies reativas de oxigênio, podem induzir as bactérias a diversificar sua química, enquanto o biorreator bem misturado favorece um conjunto menor de estruturas “centrais”.
O que isso significa para descobrir novos produtos naturais
Para as equipes de descoberta de fármacos, a mensagem é clara: você não pode confiar em uma única regra de engenharia ou em uma condição “ótima” se quer tanto diversidade química rica quanto escalabilidade confiável. Em vez disso, é preciso uma estratégia multidimensional que considere tipo de vaso, transferência de oxigênio, aditivos como etanol e, importantemente, monitoramento em tempo real da morfologia celular. Usar microplacas que mimetizem características chave de biorreatores e ajustar condições para produzir formas de crescimento semelhantes pode aumentar muito a probabilidade de que moléculas promissoras descobertas em microlitros reapareçam quando cultivadas em litros. Essa abordagem ajuda a transformar hits iniciais frágeis em candidatos robustos e reprodutíveis, aumentando as chances de que novos produtos naturais completem a jornada do banco de laboratório até o armário de remédios.
Citação: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Palavras-chave: descoberta de produtos naturais, fermentação de Streptomyces, metabolômica, ampliação em biorreator, metabólitos secundários