Clear Sky Science · pt
Alvo sinérgico do eixo ARID2–MYC por pomalidomida e panobinostate supera resistência intrínseca a IMiDs no mieloma múltiplo
Por que esta pesquisa importa para pacientes
O mieloma múltiplo é um câncer das células produtoras de anticorpos na medula óssea que se tornou mais tratável, mas ainda raramente é curável. Muitos pacientes acabam deixando de responder aos medicamentos padrão, deixando os médicos com menos opções. Este estudo investiga por que a combinação de dois tipos já existentes de medicamentos — os chamados IMiDs, como a pomalidomida, e drogas que afetam o empacotamento do DNA chamadas inibidores de histona deacetilase (HDAC), como o panobinostate — pode atuar de forma cooperativa para matar células de mieloma, mesmo quando o câncer já é resistente apenas aos IMiDs. Compreender essa cooperação ao nível molecular pode orientar combinações terapêuticas melhores e ajudar mais pacientes a se beneficiarem de fármacos que já temos.
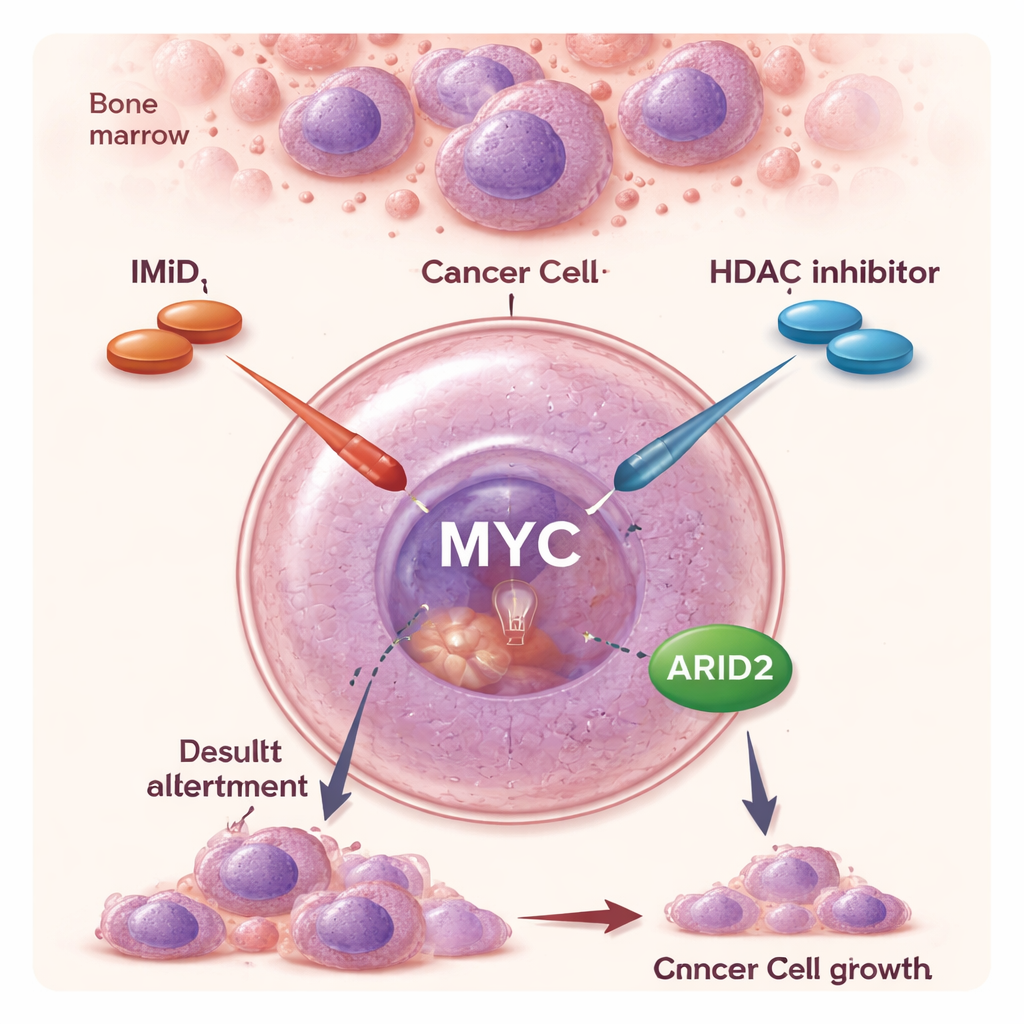
DuAS classes antigas de drogas, uma nova parceria
Nas últimas duas décadas, os IMiDs e outras drogas direcionadas ampliaram muito a sobrevida de pessoas com mieloma múltiplo. Os IMiDs atuam de forma incomum: em vez de simplesmente bloquear uma proteína, eles causam que certas proteínas sejam marcadas para destruição, efetivamente eliminando‑as da célula. Ao fazer isso, enfraquecem sinais de sobrevivência essenciais dos quais as células de mieloma dependem. Inibidores de HDAC como o panobinostate agem de maneira diferente: afrouxam o empacotamento do DNA, reconfigurando de forma ampla quais genes são ativados ou silenciados. Como agentes isolados, os inibidores de HDAC têm efeitos modestos e podem causar efeitos colaterais, mas ensaios clínicos sugeriram que combiná‑los com IMiDs produz uma resposta anticâncer muito mais forte, inclusive em pacientes cuja doença não responde mais aos IMiDs sozinhos. A razão molecular dessa sinergia, entretanto, permanecia obscura.
Um ponto de pressão comum: reduzir o MYC
Os pesquisadores testaram de forma sistemática combinações de vários IMiDs com diferentes inibidores de HDAC em um painel de linhas celulares de mieloma, usando um sistema de pontuação padronizado para medir quanto mais potentes eram as combinações em relação a cada droga isoladamente. Eles descobriram que pomalidomida mais panobinostate mostrou sinergia particularmente forte na maioria dos modelos celulares, e que esse efeito dependia de uma proteína chamada cereblon, que os IMiDs usam para direcionar suas “vítimas” proteicas à degradação. Ao analisar a atividade gênica global, a equipe descobriu que o panobinostate e um inibidor de HDAC de ação ampla relacionado desligavam fortemente o MYC, um gene mestre de crescimento frequentemente descrito como um “motor oncogênico” nas células cancerígenas, e que os IMiDs exerciam pressão adicional sobre esse mesmo ponto. Quando os cientistas forçaram as células de mieloma a continuar produzindo MYC a partir de uma fonte insensível ao medicamento, o efeito potente da dupla de medicamentos desapareceu em grande parte, demonstrando que o silenciamento do MYC é central para a cooperação entre eles.
Quebrando a resistência por uma rota alternativa
Algumas células de mieloma são intrinsecamente resistentes aos IMiDs: mesmo que os alvos iniciais esperados sejam destruídos, o MYC e outros sinais de sobrevivência não são corretamente silenciados, de modo que as células continuam a proliferar. Em um desses modelos resistentes, a via padrão dos IMiDs que liga os alvos iniciais ao MYC estava “desacoplada”. A equipe investigou se uma rota alternativa ainda poderia conectar os IMiDs ao MYC. Eles se concentraram no ARID2, um componente de uma grande máquina de remodelamento do DNA chamada complexo SWI/SNF. Trabalhos anteriores mostraram que a pomalidomida pode marcar o ARID2 para destruição e que isso ajuda a reduzir o MYC. Em células resistentes, a pomalidomida isolada reduziu o ARID2 apenas modestamente, em parte porque a célula aumentou sua produção de ARID2 em resposta. Quando o panobinostate foi adicionado, ele suprimiu o próprio gene ARID2, superando esse circuito de retroalimentação. Juntos, os dois medicamentos reduziram fortemente a proteína ARID2 e, em seguida, o MYC, levando a uma morte celular anticâncer potente mesmo em linhagens resistentes a IMiDs.
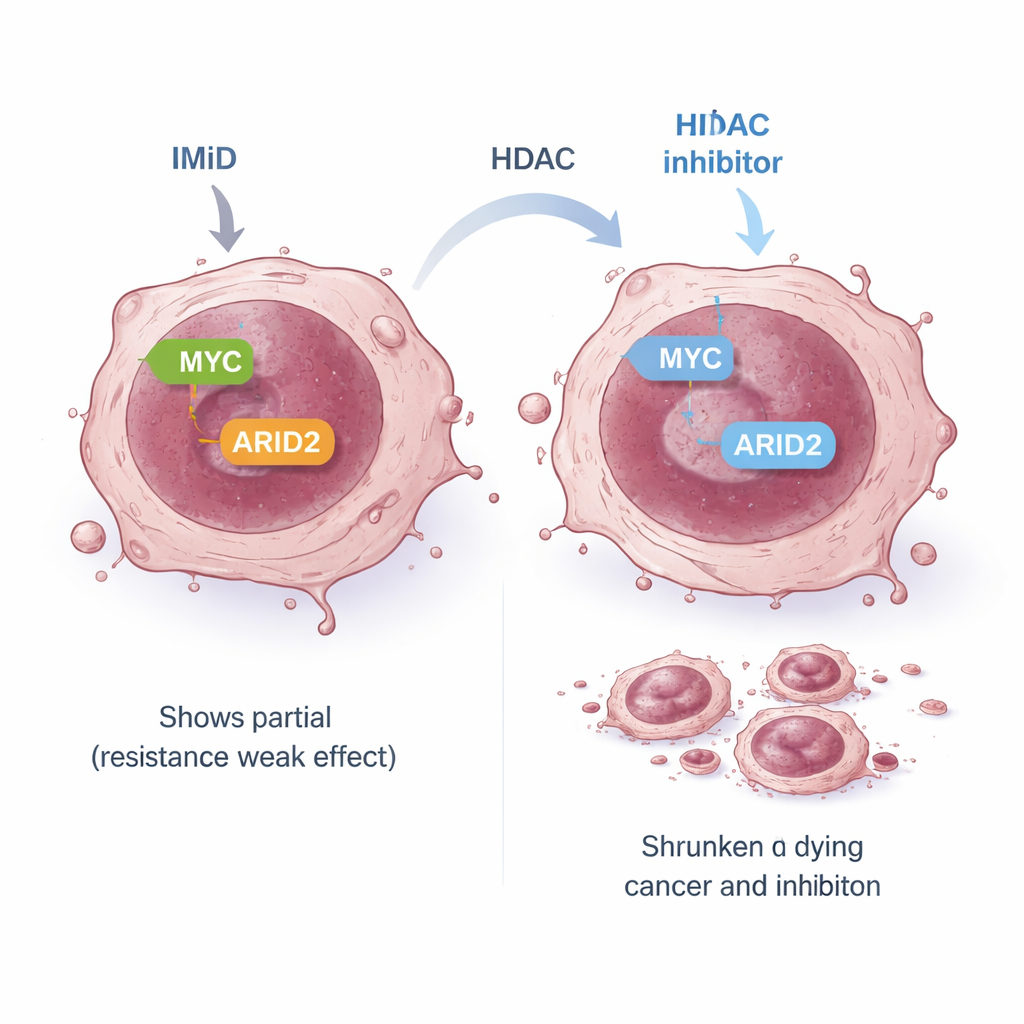
Expondo uma vulnerabilidade mais ampla nas células cancerígenas
Como o ARID2 é apenas um membro do complexo SWI/SNF, os autores perguntaram‑se se o complexo inteiro poderia ser um ponto fraco terapêutico. Eles descobriram que os inibidores de HDAC reduzem os níveis de vários componentes do SWI/SNF, e que uma droga de pequena molécula separada, projetada para bloquear os motores centrais do complexo (BRG1/BRM), sozinha pode desacelerar o crescimento das células de mieloma e reduzir o MYC. Importante: esse inibidor do SWI/SNF também atuou de forma sinérgica com pomalidomida e panobinostate, e uma combinação de três drogas levou ARID2 e MYC a níveis ainda mais baixos enquanto suprimiu fortemente a proliferação celular. Ao investigar quais enzimas HDAC específicas estavam envolvidas, os pesquisadores destacaram a HDAC1 como uma peça-chave que ajuda a sustentar a via ARID2–MYC, enquanto outras HDACs parecem influenciar o MYC por rotas paralelas.
O que isso significa para o tratamento futuro do mieloma
Para não especialistas, a mensagem central é que as células de mieloma parecem depender de um “centro de controle de crescimento” compartilhado centrado no MYC, e que existe mais de uma estrada levando a esse centro. A terapia padrão com IMiDs atinge principalmente uma estrada; em alguns cânceres resistentes, essa estrada está bloqueada, de modo que o MYC permanece ativo. Este estudo mostra que uma rota alternativa — passando pelo ARID2 e pelo complexo SWI/SNF — ainda permanece aberta, e que usar panobinostate juntamente com pomalidomida pode fechá‑la. Ao combinar deliberadamente fármacos que pressionam o MYC a partir de múltiplas direções, os clínicos podem ser capazes de superar algumas formas de resistência intrínseca aos medicamentos enquanto potencialmente usam doses menores de cada medicamento. Embora sejam necessários mais estudos pré‑clínicos e clínicos, as descobertas fornecem um roteiro mais claro para projetar combinações inteligentes e baseadas em mecanismos para pacientes com mieloma múltiplo de difícil tratamento.
Citação: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Palavras-chave: mieloma múltiplo, resistência a medicamentos, pomalidomida, panobinostate, MYC