Clear Sky Science · pt
Modificações alteradas em histonas nos intestinos de Aedes aegypti após exposição ao vírus da febre do Vale do Rift
Por que os genes do mosquito importam para a saúde humana
A febre do Vale do Rift é um vírus que adoecesce animais e pessoas em partes da África, e é transmitido por mosquitos. Para conter surtos, os cientistas precisam entender não apenas o vírus em si, mas também como os mosquitos respondem ao ingerir sangue infectado. Este estudo investiga o interior do intestino do mosquito em um nível incomum de detalhe, perguntando como o vírus induz mudanças na embalagem do DNA do mosquito para ativar ou desativar genes críticos — alterações que podem influenciar se o inseto se torna um transmissor eficaz ou ineficaz da doença.
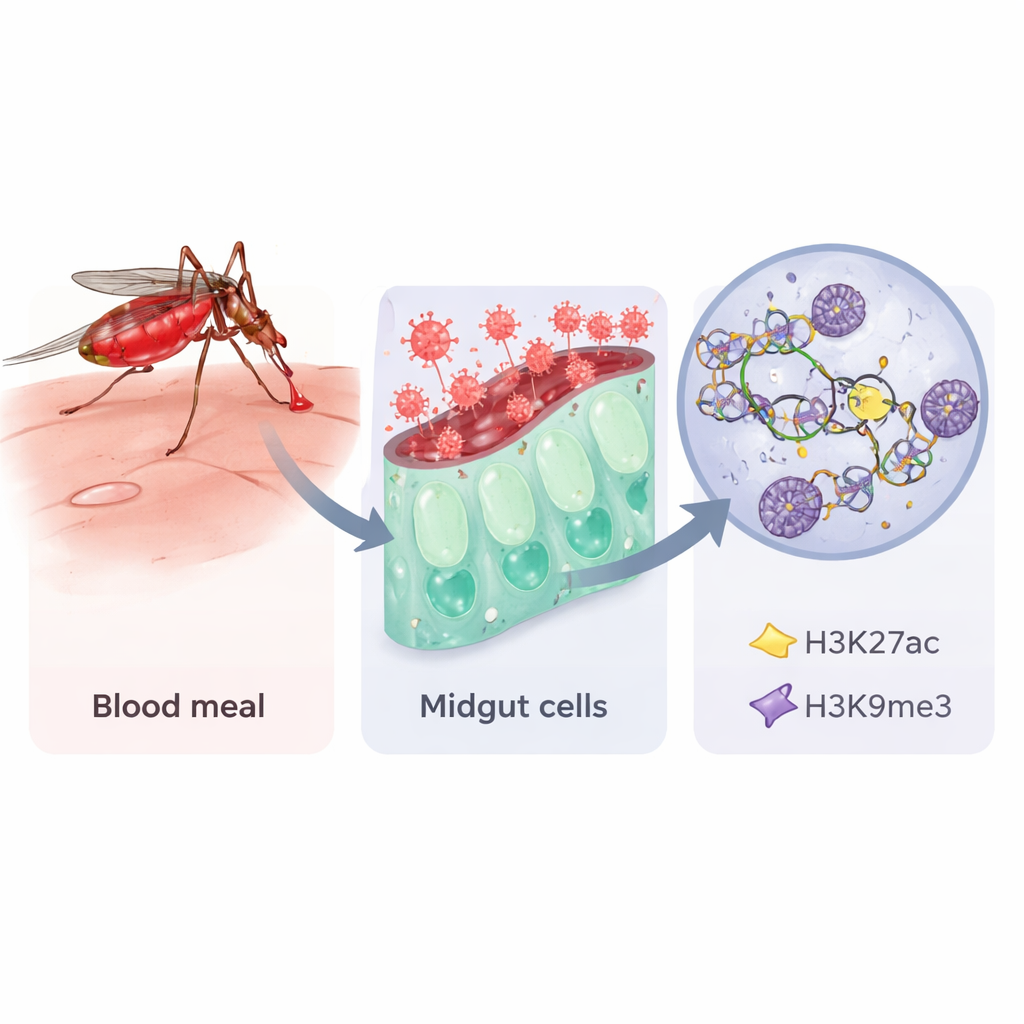
Abrindo o livro do DNA do mosquito
Como nos humanos, os mosquitos não mudam as letras do seu DNA quando encontram uma infecção, mas podem alterar o grau de compactação desse DNA. Os autores focaram em duas marcações químicas nas proteínas histonas, que funcionam como carretéis para o DNA. Uma marca, chamada H3K27ac, costuma indicar trechos de DNA abertos e ativos; a outra, H3K9me3, está associada a regiões silenciadas. Usando um método sensível conhecido como CUT&RUN, combinado com sequenciamento de RNA, a equipe examinou essas marcas e a atividade gênica nos intestinos de Aedes aegypti após três tipos de alimentação: açúcar simples, uma refeição de sangue normal ou sangue contendo uma estirpe vacinal do vírus da febre do Vale do Rift. Os intestinos foram amostrados um, três e sete dias após a alimentação para captar estágios iniciais, intermediários e tardios da infecção.
Como uma simples refeição de sangue reprograma o intestino
Uma refeição de sangue por si só, mesmo sem o vírus, provocou mudanças amplas na atividade gênica do intestino. Milhares de genes mudaram sua atividade um dia após a alimentação, especialmente aqueles envolvidos na digestão de proteínas, no manejo de energia e na construção de novos componentes celulares. Muitos desses genes estavam próximos de regiões marcadas por H3K27ac, consistente com a ideia de que o sangue desencadeia a abertura de bairros específicos do DNA necessários para a digestão e a produção de ovos. Nos dias seguintes, à medida que o sangue era digerido, o padrão evoluiu: a maquinaria produtora de energia permaneceu ativa e, mais tarde, genes envolvidos na organização dos cromossomos e no ciclo celular foram afetados. Os mosquitos alimentados com açúcar, em contraste, exibiram padrões mais estáveis, sugerindo que não tomar uma refeição de sangue pode levar a uma paisagem de DNA diferente, possivelmente relacionada ao envelhecimento.
Quando o vírus encontra as defesas do intestino
Adicionar o vírus da febre do Vale do Rift ao sangue mudou o quadro. No início, um e três dias após a alimentação, os intestinos de mosquitos expostos ao vírus aumentaram a expressão de genes ligados à defesa imune e ao sinalizador celular, além das mudanças causadas apenas pelo sangue. Ao mesmo tempo, as relações usuais entre as marcas das histonas e os genes vizinhos tornaram‑se mais complexas. No terceiro dia em particular, muitas regiões marcadas pela H3K9me3, normalmente repressiva, perderam essa marca, e centenas de genes próximos ficaram mais ativos, incluindo aqueles envolvidos no controle de outros genes, na transdução de sinais intracelulares e no gerenciamento da forma e polaridade celular. Aos sete dias, quando cerca da metade dos mosquitos carregava vírus infeccioso, a atividade gênica geral nos intestinos expostos caiu, genes relacionados à imunidade foram reduzidos e as marcas ativadoras H3K27ac estavam amplamente depletadas em comparação com os controles alimentados apenas com sangue.
Pistas de artifícios virais e defesas do mosquito
Ao correlacionar atividade gênica com mudanças histônicas próximas, os pesquisadores identificaram um pequeno conjunto de genes cujo comportamento é especialmente sugestivo. Alguns genes que ajudam a organizar estruturas de membrana ou a mover materiais dentro das células ganharam atividade enquanto suas marcas ativadoras locais diminuíam, tornando‑se candidatos a auxiliar o vírus na montagem ou no transporte intracelular. Outros, como genes relacionados à desintoxicação de moléculas reativas ou ao reconhecimento de patógenos, mostraram padrões compatíveis com funções antivirais. Um gene de destaque, que carrega um domínio proteico conhecido de fatores antivirais humanos, aumentou seu RNA enquanto perdia tanto marcas ativadoras quanto repressivas nas histonas, sugerindo forte pressão regulatória durante a infecção. O estudo também realçou uma via de polaridade celular, chamada smoothened/hedgehog, cujos componentes foram atenuados tardiamente na infecção, em consonância com evidências de que muitos vírus preferem células altamente polarizadas.
O que isso significa para controlar doenças transmitidas por mosquitos
Para um público não especializado, a mensagem principal é que as células do intestino do mosquito não aceitam a invasão viral passivamente. Em vez disso, elas remodelam rapidamente a forma como seu DNA é embalado, primeiro para impulsionar a digestão e a reprodução após uma refeição de sangue e depois para montar — ou às vezes relaxar — defesas contra o vírus da febre do Vale do Rift. Duas marcas de histonas, H3K27ac e H3K9me3, mudam de maneiras complexas durante esse cabo de guerra, influenciando quais genes podem responder. Embora apenas uma fração das mudanças gênicas tenha sido vinculada diretamente a essas marcas, o trabalho mostra que sinais epigenéticos são uma camada importante da resposta do mosquito à infecção. A longo prazo, entender esses interruptores pode ajudar cientistas a projetar novas estratégias para tornar os mosquitos menos capazes de transportar vírus, adicionando mais uma ferramenta à luta contra doenças emergentes transmitidas por mosquitos.
Citação: Ogg, H.A., Mikol, Z.M., King, D.C. et al. Altered histone modifications in Aedes aegypti midguts following Rift Valley fever virus exposure. Sci Rep 16, 6605 (2026). https://doi.org/10.1038/s41598-026-37729-y
Palavras-chave: vírus da febre do Vale do Rift, Aedes aegypti, epigenética de mosquitos, modificações de histonas, competência vetorial