Clear Sky Science · pt
Mecanismo e divergência evolutiva de uma nova hidrolase de polietileno vinílico oxidado em Stenotrophomonas rhizophila QL-P4
Por que um plástico “verde” comum ainda persiste na natureza
O álcool polivinílico, ou PVA, aparece em tudo, desde cápsulas de detergente para roupas até revestimentos têxteis e papel. Frequentemente é comercializado como ambientalmente amigável porque, em princípio, microrganismos podem degradá‑lo. No entanto, em rios, solos e oceanos reais esse material semelhante a plástico se decompõe muito lentamente e pode persistir por décadas como fragmentos de micro e nanoplástico. Este estudo examina de perto uma das ferramentas da natureza para enfrentar o PVA: uma enzima recém‑descoberta de uma bactéria do solo capaz de fragmentar esse polímero persistente em pedaços menores e mais seguros.
Um pequeno ajudante do solo com uma grande missão
Pesquisadores isolaram anteriormente uma bactéria chamada Stenotrophomonas rhizophila QL‑P4 de solo de montanha na China e descobriram que ela pode crescer usando PVA como fonte de alimento. No trabalho novo, focaram em um único gene suspeito, chamado BAY15_0160, que parecia codificar uma enzima capaz de cortar PVA oxidado. Ao deletar cuidadosamente esse gene, reintroduzi‑lo e forçar a superexpressão dele na bactéria, mostraram que BAY15_0160 é essencial para a degradação eficiente do PVA. Quando o gene foi removido, o microrganismo perdeu cerca de 40% de sua capacidade de consumir PVA; restaurar o gene recuperou o desempenho, confirmando que seu produto é um componente chave na via de degradação.
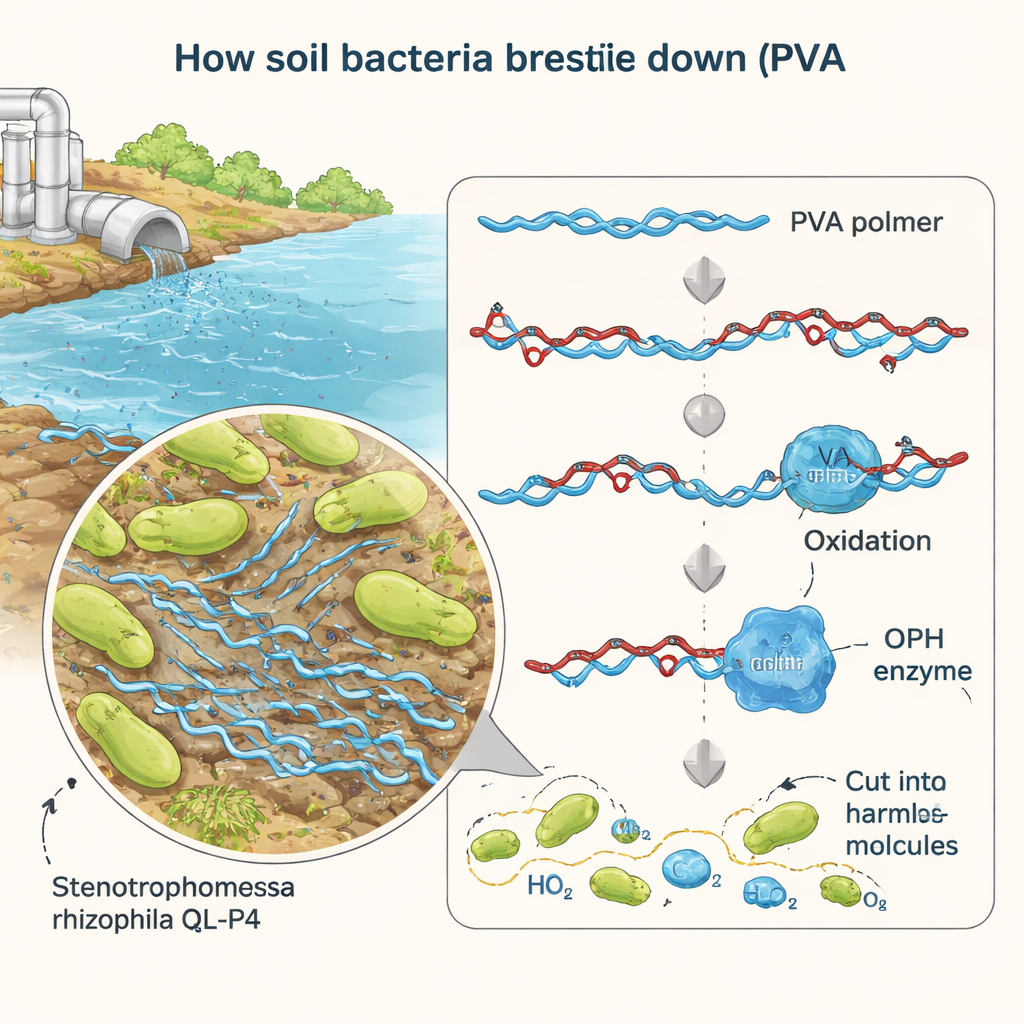
Medindo como a enzima realiza seu trabalho
Para estudar a enzima em detalhe, a equipe a produziu em grandes quantidades usando cepas laboratoriais de Escherichia coli. Eles purificaram a proteína, que se revelou de cerca de 35 quilodaltons, e testaram sua atividade sob diferentes condições. Usando uma molécula‑teste simples que libera um corante amarelo quando é cortada, acompanharam a velocidade da reação em várias temperaturas e níveis de acidez. A enzima foi mais ativa em torno da temperatura ambiente (30 °C) e em pH neutro, semelhante ao de muitas águas naturais. Nessas condições suaves, mostrou alta eficiência catalítica, o que significa que cada molécula da enzima pode processar muitas moléculas de substrato por segundo — notícia encorajadora para aplicações práticas de limpeza ambiental.
Observando de perto as tesouras moleculares
Enzimas são as pequenas máquinas da natureza, e sua forma determina o que podem fazer. Os pesquisadores usaram programas de predição de última geração, RoseTTAFold e AlphaFold, para construir modelos tridimensionais da enzima que corta PVA, agora reconhecida como uma nova hidrolase de PVA oxidado, ou OPH. Ambas as ferramentas concordaram que a enzima possui o encaixe clássico de “hidrolase alfa/beta” encontrado em muitas tesouras biológicas. Em seu núcleo há um motivo curto — frequentemente escrito como Gly–X–Ser–X–Gly — que ajuda a posicionar um trio de aminoácidos (serina, aspartato e histidina) para atacar ligações químicas. Simulações computacionais mostraram fragmentos de PVA oxidado acomodando‑se nesse sulco, com a serina chave provavelmente fazendo o primeiro corte na cadeia.
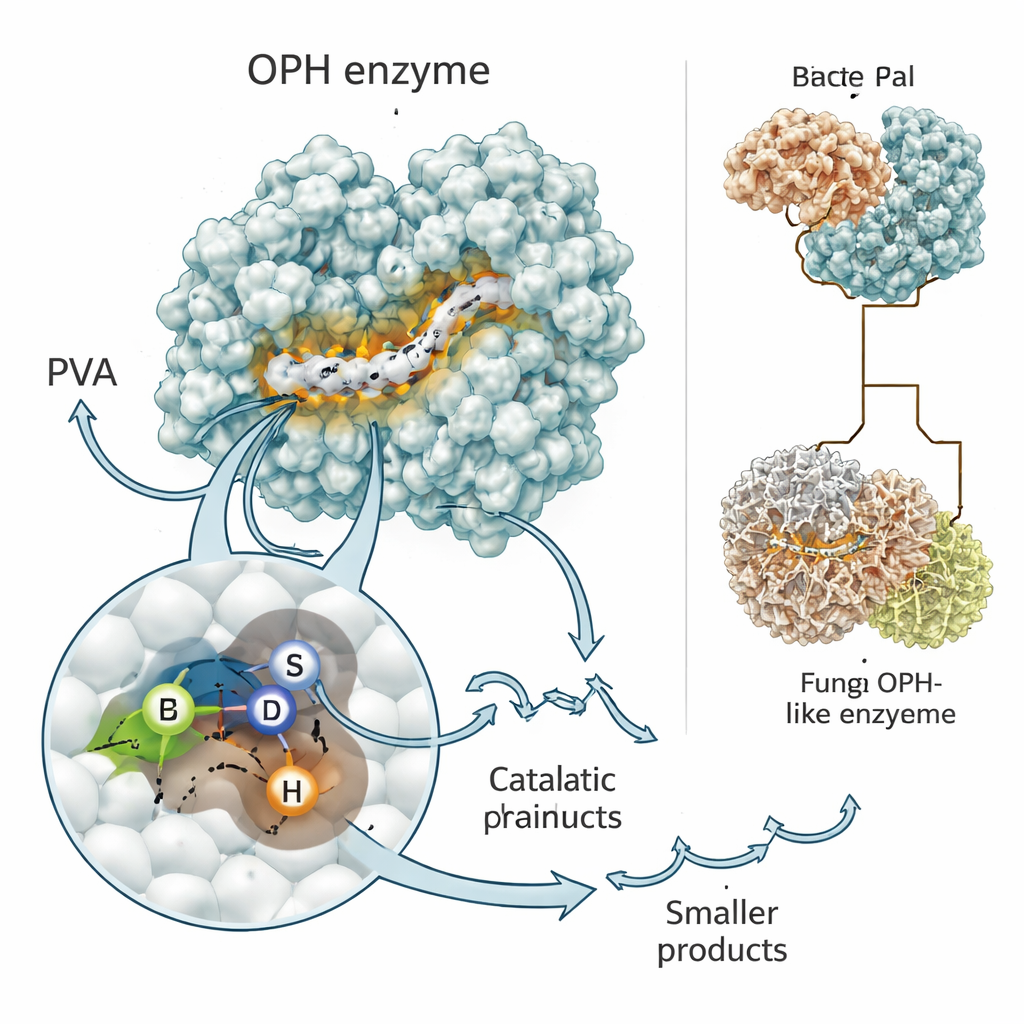
Sinais, chaves e reviravoltas evolutivas
A equipe também explorou quais partes da enzima são absolutamente necessárias para seu funcionamento na bactéria. Uma região próxima à frente da proteína age como um código postal, direcionando a enzima para fora da célula, onde o polímero PVA realmente se encontra. Outra região contém o motivo ativo que apreende e cliva as ligações carbono–carbono do plástico. Quando os cientistas construíram versões do gene sem o segmento sinalizador ou sem o motivo do sítio ativo, a bactéria ainda produziu RNA a partir do gene, mas não conseguiu mais digerir o PVA de forma eficiente. Ao examinar muitas bactérias e fungos, encontraram parentes dessa enzima que compartilham a mesma região central de “corte”, mas diferem em partes adicionais, incluindo uma versão fúngica marcante que funde o domínio de corte a um transportador incorporado, sugerindo uma estratégia de importar‑e‑digerir ainda mais eficiente em ambientes extremos, como rochas antárticas.
O que isso significa para a limpeza da poluição por plástico
Para não especialistas, a mensagem principal é que os cientistas estão aprendendo como alguns micróbios naturalmente degradam um plástico supostamente biodegradável que, de outra forma, permanece por tempo demais no ambiente. Este estudo identifica uma única enzima, OPH de S. rhizophila QL‑P4, como uma poderosa tesoura molecular que opera em condições suaves e atua em uma etapa crucial da degradação do PVA. Ao entender sua estrutura, condições de trabalho e parentes evolutivos, os pesquisadores podem começar a projetar cepas microbianas melhores ou misturas de enzimas adaptadas para estações de tratamento de águas residuais, efluentes industriais ou solos contaminados. A longo prazo, esses conhecimentos nos aproximam de soluções práticas baseadas em biologia para gerenciar resíduos plásticos, em vez de deixá‑los se acumular no ambiente.
Citação: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Palavras-chave: álcool polivinílico, biodegradação, poluição por plástico, enzimas microbianas, biorremediação