Clear Sky Science · pt
Dieta rica em gorduras remodela as redes regulatórias de genes na área pré-ótica
Por que seu cérebro importa no diabetes
A maioria das pessoas pensa no diabetes como um problema do pâncreas e da glicemia, mas o cérebro também está profundamente envolvido. Este estudo investiga como uma dieta rica em gorduras e um tratamento experimental potente alteram a atividade gênica em uma pequena, porém importante, região cerebral chamada área pré-ótica. Ao mapear quais células cerebrais “reconfiguram” sua atividade quando o diabetes entra em remissão, os pesquisadores esperam apontar caminhos para novas terapias que explorem a capacidade do próprio cérebro de ajudar a controlar a glicose sanguínea.
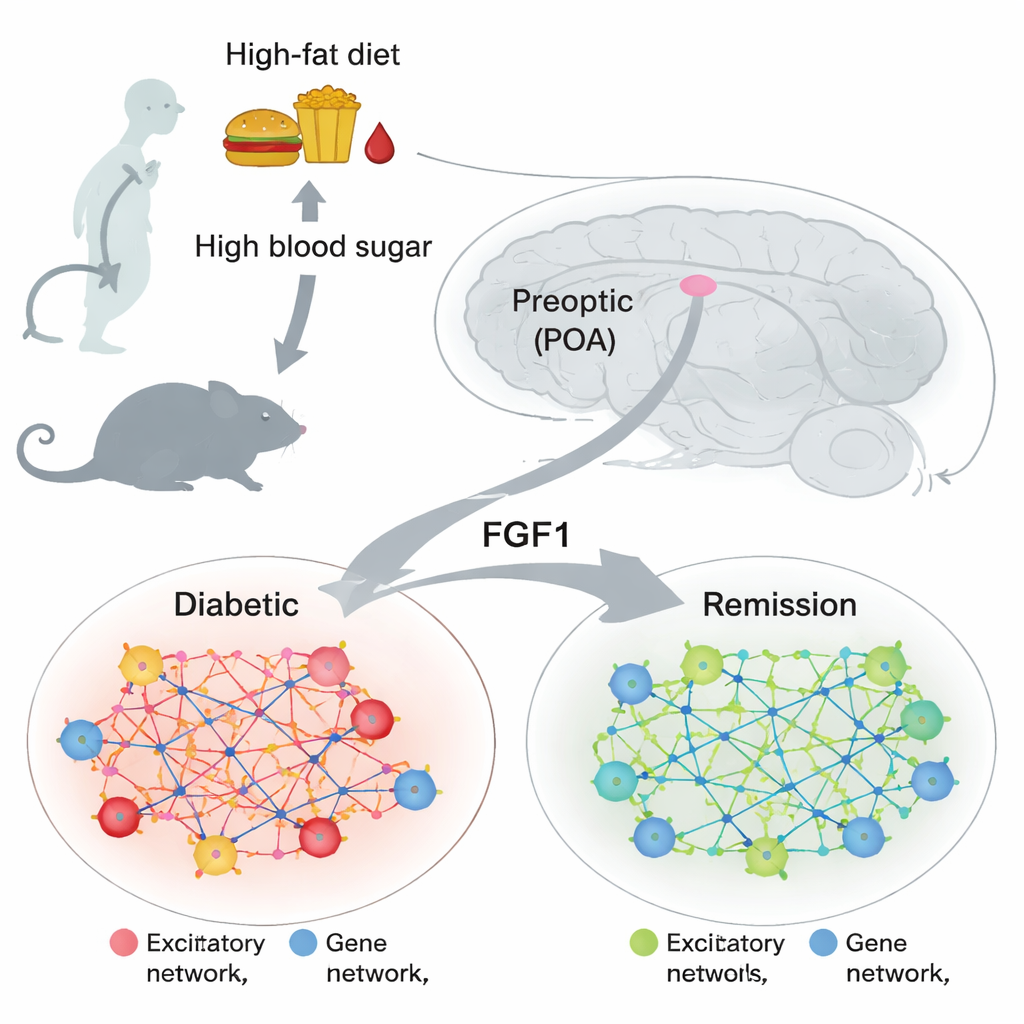
Um pequeno centro cerebral com grande influência metabólica
A área pré-ótica situa-se na frente do hipotálamo, uma parte do cérebro que regula temperatura corporal, sono, alimentação e sinais hormonais. Trabalhos anteriores mostraram que células nessa região podem influenciar como o corpo lida com a glicose e responde ao calor, mas seu papel no diabetes era pouco compreendido. Ao mesmo tempo, outros estudos descobriram que uma única dose de uma proteína chamada fator de crescimento de fibroblastos 1 (FGF1), administrada no cérebro, pode levar camundongos obesos e diabéticos a uma remissão duradoura. Isso levantou uma questão-chave: quais células cerebrais e programas gênicos mudam quando a glicemia normaliza, e mudanças semelhantes aparecem na área pré-ótica?
Lendo a atividade gênica célula a célula
Para responder, a equipe recorreu ao sequenciamento de RNA de célula única, uma técnica que mede quais genes estão ativados em milhares de células individuais ao mesmo tempo. Eles reanalisaram um conjunto de dados existente de camundongos cuja diabetes entrou em remissão após tratamento com FGF1, focando em neurônios do hipotálamo. Usando ferramentas estatísticas, identificaram grupos de genes que aumentavam ou diminuíam em conjunto à medida que os animais transitavam do estado diabético para a remissão. Esses “módulos de remissão” funcionam como impressões digitais da recuperação: em vez de acompanhar um gene por vez, capturam mudanças coordenadas em muitos genes dentro de tipos neuronais específicos.
Dieta rica em gorduras, células cerebrais e redução do uso de energia
Os pesquisadores então compararam esses módulos de remissão com a atividade gênica em outro conjunto de dados que amostrava células da área pré-ótica de camundongos normais. Primeiro, separaram os neurônios em duas classes amplas: células excitatórias, que tendem a aumentar a atividade em seus circuitos, e células inibitórias, que a reduzem. Em camundongos diabéticos tratados com FGF1, ambos os tipos neuronais apresentaram amplas reduções em genes ligados à produção de energia — especialmente aqueles envolvidos em fosforilação oxidativa, respiração celular e na maquinaria mitocondrial que alimenta células ativas. Nos neurônios excitatórios, um grande módulo gênico “turquesa” associado ao uso de energia e à atividade sináptica foi fortemente suprimido na remissão, sugerindo que essas células se tornam menos exigentes metabolicamente quando a glicemia é controlada.
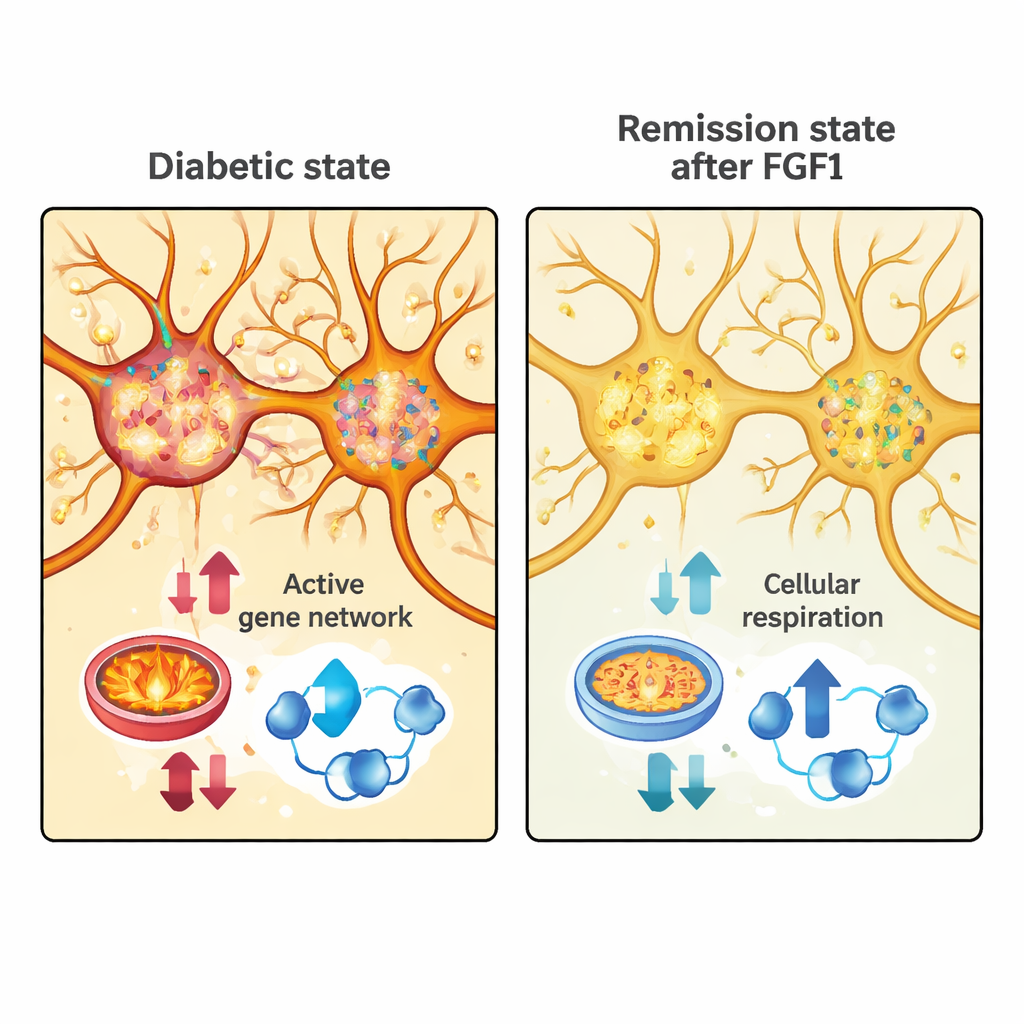
Rastreando assinaturas de remissão a grupos neuronais específicos
Em seguida, a equipe perguntou se esses padrões gênicos relacionados à remissão correspondiam a populações celulares particulares na área pré-ótica. Ao mesclar computacionalmente os dois conjuntos de dados, descobriram que alguns aglomerados de neurônios pré-óticos expressavam muitos dos mesmos genes que mudavam com a remissão induzida por FGF1. Eles destacaram vários genes — como Trpc4, Dgkg e Ryr3 — que estavam no cruzamento dessas análises. Utilizando um método de microscopia altamente sensível chamado RNAscope, mostraram que esses genes são de fato expressos em zonas distintas da área pré-ótica do camundongo, majoritariamente em sub-regiões dorsais. Isso os valida como marcadores reais de grupos neuronais específicos que podem participar da resposta cerebral à doença metabólica.
O que isso significa para tratamentos futuros do diabetes
Para não especialistas, a conclusão é que o diabetes não é apenas um problema de glicemia — é também um problema de redes cerebrais. O estudo demonstra que, quando o diabetes entra em remissão em camundongos, certos neurônios pré-óticos mudam para um estado de menor consumo energético e alteram sua atividade gênica de maneira coordenada. Ao definir esses módulos de remissão e vinculá-los a tipos celulares concretos e genes marcador, o trabalho fornece um roteiro para experimentos futuros: pesquisadores agora podem direcionar esses neurônios específicos para testar como eles influenciam o controle da glicose, a obesidade e complicações relacionadas. A longo prazo, um melhor entendimento desses circuitos cerebrais pode inspirar tratamentos que complementem ou até contornem órgãos com falha no corpo, aproveitando o controle intrínseco do cérebro sobre o metabolismo.
Citação: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Palavras-chave: cérebro e diabetes, área pré-ótica, dieta rica em gorduras, redes gênicas, remissão por FGF1