Clear Sky Science · pt
Identificação no transcriptoma completo de variantes deletérias em genes candidatos ligados à paratuberculose bovina
Genes ocultos por trás de uma doença bovina onerosa
A paratuberculose bovina, também conhecida como doença de Johne, corrói silenciosamente a saúde e a produtividade de rebanhos leiteiros ao redor do mundo, custando aos produtores centenas de milhões de dólares por ano e suscitando preocupações sobre ligações com transtornos intestinais humanos. Este estudo investiga o “capô” genético de vacas Holandesas para responder a uma pergunta simples, porém crucial: quais diferenças em seus genes podem ajudar alguns animais a resistir a essa infecção enquanto outros sucumbem? Ao ler o RNA — as cópias funcionais dos genes — no sangue e no tecido intestinal, os pesquisadores rastrearam como mudanças sutis no DNA em genes-chave do sistema imune podem direcionar o curso da doença.
Por que essa doença bovina importa
A paratuberculose é causada pela bactéria Mycobacterium avium subespécie paratuberculosis (MAP). As vacas tipicamente se infectam cedo na vida, mas os sinais costumam aparecer anos depois. Nas fases silenciosa e subclínica, os animais parecem saudáveis, mas podem eliminar baixos níveis de bactérias e produzir menos leite. Nas fases clínicas, desenvolvem diarreia crônica, perda de peso severa e quedas expressivas na produção de leite. As taxas de infecção ao nível do rebanho podem exceder 50% em muitas regiões, incluindo partes da Europa e da América do Norte, criando um desafio econômico e de bem‑estar animal. Como a bactéria também pode atuar como um gatilho ambiental para doenças inflamatórias humanas, como a doença de Crohn, cresce a pressão para melhorar as estratégias de controle em bovinos.
Lendo o genoma funcional
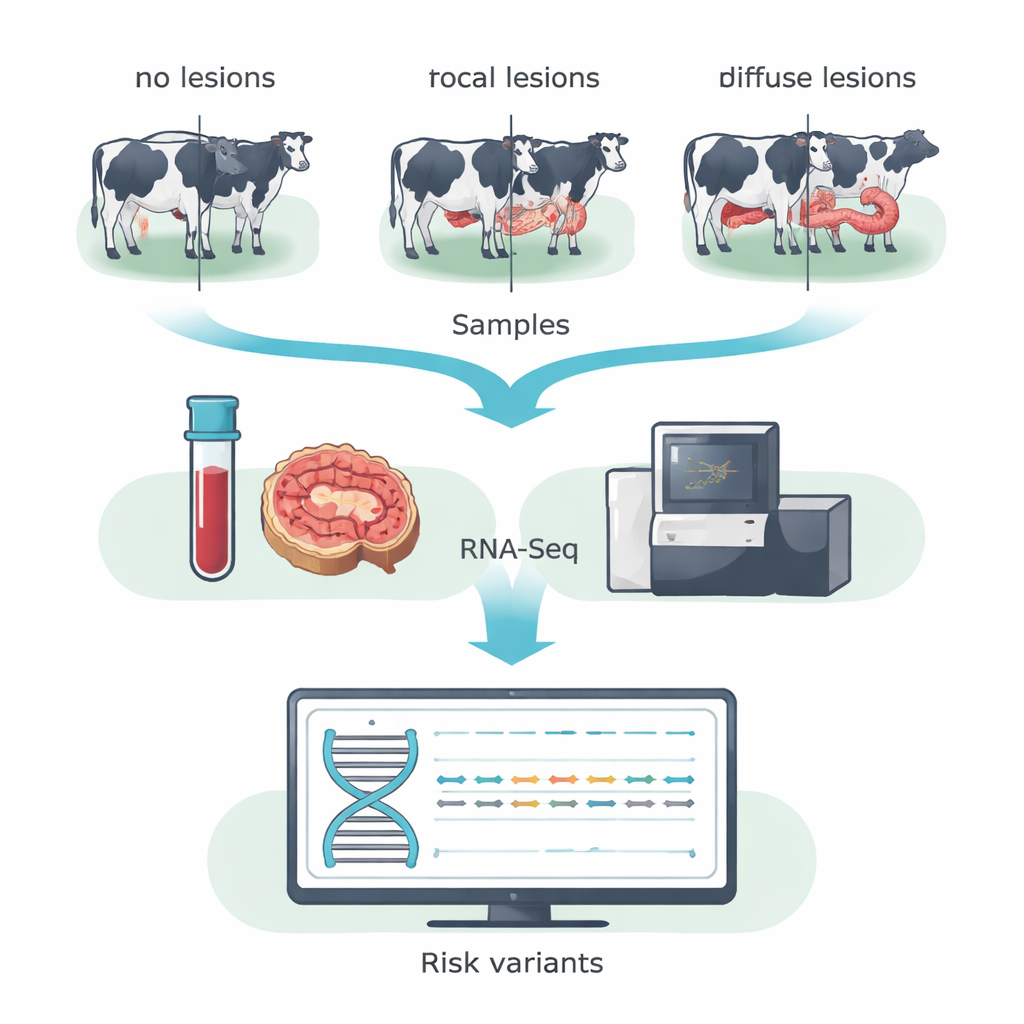
Em vez de vasculhar toda a sequência de DNA, a equipe usou sequenciamento de RNA (RNA‑Seq) para focar nos genes que estão realmente ativos no animal. Eles coletaram sangue e amostras da válvula ileocecal — uma região intestinal fortemente afetada pelo MAP — de 14 vacas Holandesas em um rebanho leiteiro espanhol. Com base no exame microscópico dos tecidos intestinais, as vacas foram agrupadas em três categorias: animais sem lesões detectáveis, animais com pequenas lesões localizadas (focais) típicas de infecção subclínica prolongada, e animais com lesões severas e difusas associadas à doença clínica. Ao mesclar dados de sangue e intestino dentro de cada grupo, os pesquisadores aumentaram sua capacidade de detectar mudanças de uma letra no DNA em genes expressos, conhecidas como SNPs codificantes.
Encontrando mudanças nocivas em genes imunes chave
De centenas de milhares de variantes, a equipe concentrou‑se naquelas que alteram a sequência proteica e são preditas como capazes de prejudicar a função da proteína — as chamadas variantes deletérias. Aplicaram filtros rigorosos para garantir alta confiança e usaram ferramentas de predição estabelecidas para sinalizar alterações de risco. Esse processo de seleção revelou 31 variantes desse tipo únicas em vacas sem lesões, 15 únicas em vacas com lesões focais e 31 únicas em vacas com lesões difusas. Muitas delas recairam sobre genes que orientam como as células imunes reconhecem e eliminam infecções, regulam a morte celular e gerenciam o metabolismo. Um destaque foi a família de genes BOLA, a versão bovina do complexo principal de histocompatibilidade classe II, que ajuda as células imunes a apresentar fragmentos bacterianos às células T. Diferentes variantes potencialmente nocivas em BOLA foram encontradas nos três grupos de vacas, sugerindo que versões específicas de BOLA podem inclinar os animais para resistência, controle da infecção ou inflamação lesiva.
Das variantes de DNA às vias de doença
Para entender o que essas mudanças genéticas podem significar na prática, os pesquisadores examinaram quais vias biológicas estavam enriquecidas em cada grupo. Vacas sem lesões mostraram variantes alteradas em genes ligados ao processamento de antígenos, tráfego de vesículas e equilíbrio imune intestinal, incluindo BOLA, AP3B1 e CHGA. Essas alterações podem promover a digestão eficiente de bactérias dentro das células imunes e um ambiente intestinal estável que limita danos. Nas vacas com lesões focais, variantes nocivas se concentraram em genes (ORMDL3 e KANK2) que atenuam a morte celular programada e regulam o metabolismo celular, potencialmente ajudando o hospedeiro a manter baixos os números bacterianos durante uma fase subclínica prolongada. Nas vacas com lesões difusas, os genes afetados apontaram para vias imunes hiperativas, como diferenciação de células Th1/Th2 e apresentação de antígenos, junto com transporte de bile e rotas de resposta a fármacos. Aqui, genes alterados da família BOLA podem impulsionar uma reação inflamatória forte, por vezes autolesiva, ecoando padrões observados em muitas doenças autoimunes e inflamatórias humanas.
Pistas para criar rebanhos mais resilientes
Além de esclarecer como diferentes variantes genéticas moldam a resposta imune ao MAP, o estudo também vinculou essas alterações de risco a regiões conhecidas do genoma bovino associadas a características de saúde, incluindo suscetibilidade à paratuberculose e outras infecções. Embora esses resultados ainda exijam validação em rebanhos maiores e não possam ser usados isoladamente como marcadores diagnósticos, oferecem um catálogo promissor de variantes e genes candidatos. Em termos simples, o trabalho sugere que algumas vacas carregam versões de genes que as ajudam a controlar silenciosamente a infecção, enquanto outras carregam versões que favorecem inflamação descontrolada e doença grave. No futuro, tais informações poderão apoiar programas de seleção e testes genéticos que deslocem os rebanhos rumo a maior resistência natural, reduzindo tanto perdas econômicas quanto a necessidade de medidas intensivas de controle de doenças.
Citação: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Palavras-chave: paratuberculose bovina, genética da doença de Johne, imunidade em bovinos leiteiros, sequenciamento de RNA, cruzamento para resistência a doenças