Clear Sky Science · pt
Sinalização de interferon tipo I define uma nova assinatura de doença em queratinócitos humanos com xeroderma pigmentosum C
Por que a luz solar pode ser tão perigosa para algumas pessoas
Para a maioria de nós, a luz solar significa calor e vitamina D. Mas para pessoas com uma condição genética rara chamada xeroderma pigmentoso C (XP‑C), até mesmo a luz do dia moderada pode causar danos severos à pele e um risco extremo de câncer de pele. Este estudo vai além do bem conhecido problema de reparo de DNA no XP‑C e revela uma camada oculta de sinalização tipo imunológica hiperativa dentro das células da pele, oferecendo novas pistas sobre por que a pele dessas pessoas é tão vulnerável e inflamada após a exposição ao sol.
Quando o reparo de DNA falha na pele
Nossas células da pele reparam constantemente os danos ao DNA causados pelos raios ultravioleta B (UVB) do sol. Uma proteína chamada XPC é um dos primeiros “sensores” que detecta lesões induzidas por UV e aciona uma grande equipe de reparo. No XP‑C, mutações no gene XPC prejudicam essa etapa de alerta inicial, de modo que os danos por UV se acumulam em vez de serem corrigidos. Pacientes com XP‑C desenvolvem cânceres de pele milhares de vezes mais frequentemente do que a população em geral e precisam evitar a luz solar rigorosamente. Embora esse defeito no reparo de DNA seja bem conhecido, como ele reconfigura os sistemas de comunicação internos das células — especialmente aqueles que controlam a inflamação — tem sido muito menos claro.
Investigando sinais celulares ao longo do tempo
Para abordar esse problema, os pesquisadores modificaram queratinócitos humanos — as principais células da camada externa da pele — para que ficassem totalmente sem XPC, e os compararam com células normais idênticas em todos os outros aspectos. Eles expuseram ambos os tipos celulares a um nível de UVB cuidadosamente escolhido, semelhante a uma dose de queimadura solar moderada. Em seguida, examinaram as células em duas etapas. Uma hora após a irradiação, mediram a atividade de muitas enzimas chamadas tirosina quinases de proteína, que ligam e desligam sinais adicionando pequenas marcas de fosfato. Vinte e quatro horas depois, usaram espectrometria de massa avançada para obter um panorama amplo de milhares de proteínas e ver quais aumentavam ou diminuíam em abundância. Essa abordagem em duas etapas permitiu acompanhar tanto os primeiros “sinais de alarme” quanto as respostas “a jusante” posteriores dentro das células.
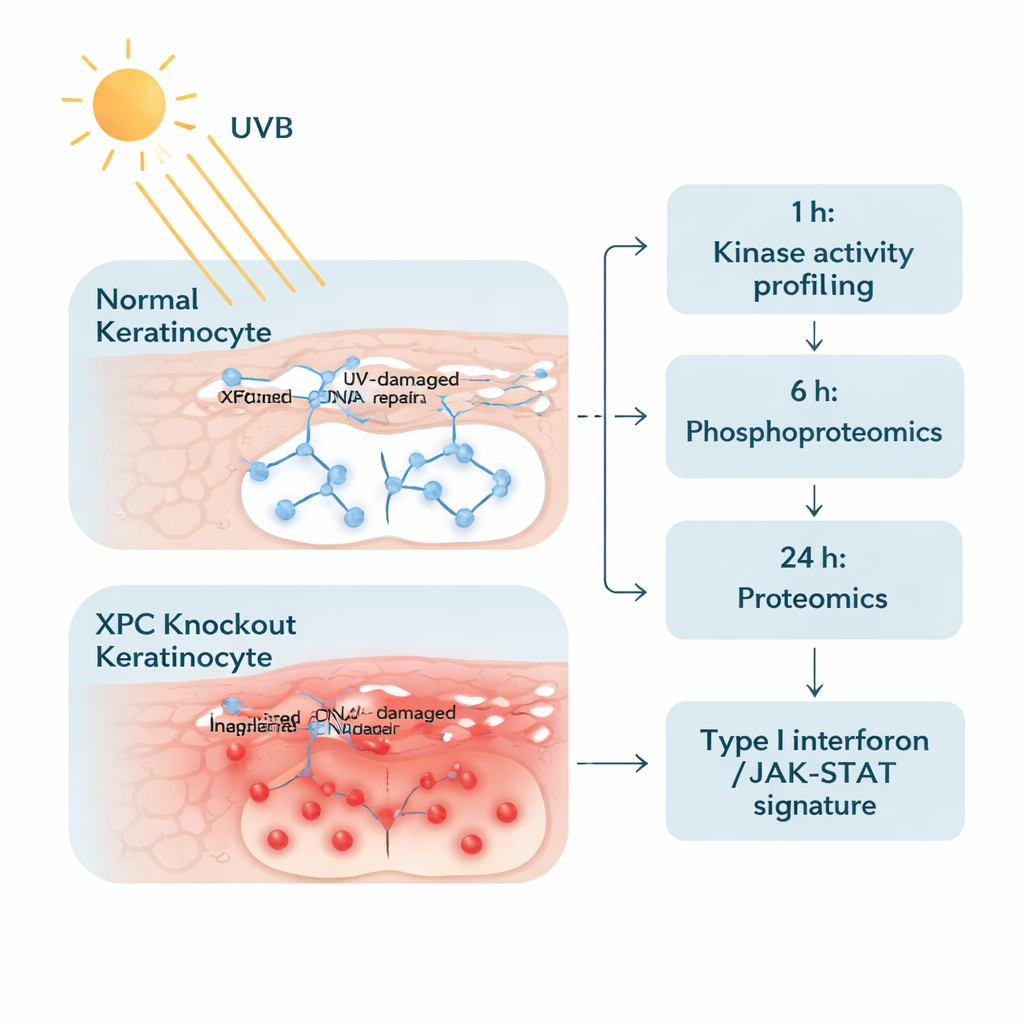
Uma via inflamatória se acende
A triagem inicial das quinases revelou que queratinócitos deficientes em XPC respondem ao UVB com uma onda de fosforilação em mais de uma centena de sítios em comparação com células normais. Notavelmente, muitas dessas mudanças se agruparam na via de sinalização JAK/STAT — uma rota de comunicação central normalmente usada por mensageiros imunológicos como os interferons. Marcadores ligados a JAK1, JAK2, JAK3, TYK2 e proteínas STAT estavam mais ativos nas células XP‑C, mesmo antes do UVB, e foram ainda mais elevados após a irradiação. Isso sugere que as células estavam em um estado de “alta vigilância”, prontas para amplificar mensagens inflamatórias sempre que encontrassem estresse induzido por UV.
Genes de alarme no estilo interferon em células da pele
A pesquisa proteica mais ampla e posterior confirmou e ampliou esse quadro. Em células com nocaute de XPC, especialmente após UVB, centenas de proteínas foram alteradas, e um grande grupo correspondeu a genes normalmente ativados por interferons tipo I — os mesmos sinais antivirais que nosso corpo usa para combater infecções. Proteínas como MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 e IRF9, clássicos “genes estimulados por interferon”, estavam fortemente elevadas. Análises de redes e vias ligaram essas proteínas de volta à sinalização JAK/STAT e ao interferon tipo I como o tema dominante. Experimentos subsequentes de western blot confirmaram que proteínas STAT-chave estavam mais fosforiladas e que essas proteínas responsivas ao interferon eram produzidas em níveis muito mais altos nas células XP‑C do que em queratinócitos normais, tanto em repouso quanto, especialmente, após UVB.
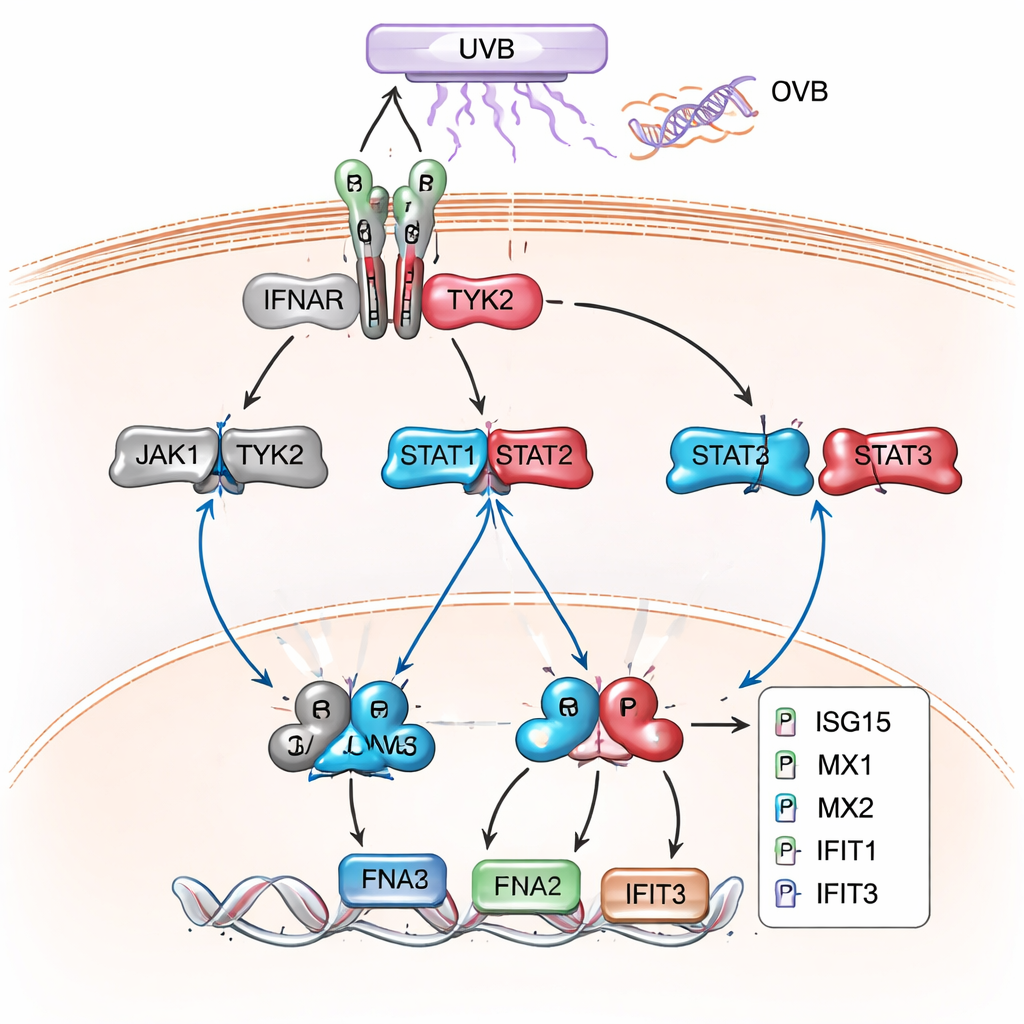
O que isso significa para pacientes e tratamentos futuros
Em conjunto, esses resultados mostram que o XP‑C não é apenas uma doença de reparo de DNA defeituoso; também se caracteriza por um estado inflamatório persistente, do tipo interferon, dentro das células da pele, conduzido pela via JAK/STAT e intensificado pela luz UV. Para um leigo, isso significa que queratinócitos XP‑C se comportam como se estivessem constantemente combatendo uma infecção invisível sempre que veem luz solar, sobrepondo inflamação crônica ao dano de DNA não reparado. Embora o estudo não avalie tratamentos diretamente, ele levanta a possibilidade de que drogas cuidadosamente ajustadas que atinjam JAK/STAT ou circuitos inflamatórios relacionados possam um dia ajudar a reduzir o dano desencadeado por UV no XP‑C e talvez em outras condições inflamatórias da pele que compartilhem essa assinatura molecular.
Citação: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Palavras-chave: xeroderma pigmentoso, câncer de pele, reparo de DNA, sinalização de interferon, via JAK STAT