Clear Sky Science · pt
Reservatórios na membrana plasmática de APOL1 resistem à degradação rápida da proteína
Por que o “desaparecimento” de uma proteína renal importa
Uma grande parcela das formas graves de doença renal em pessoas de ascendência africana recente foi atribuída a duas variantes de um único gene, APOL1. Ainda assim, os cientistas têm dificuldade para explicar exatamente como esse gene danifica as células renais sem prejudicar a maioria dos portadores. Este estudo faz uma pergunta aparentemente simples, com implicações importantes: uma vez sintetizada dentro das células, por quanto tempo a proteína APOL1 permanece e onde é mais estável? As respostas revelam uma personalidade surpreendentemente dupla — APOL1 é rapidamente destruída dentro das células, mas se mantém teimosamente estável quando incorporada na superfície externa da célula, uma pista que pode orientar terapias futuras.
Gene de risco com um lado duplo
O gene APOL1 ajuda a proteger os humanos contra certos parasitas, uma vantagem evolutiva que provavelmente explica por que suas variantes de risco, chamadas G1 e G2, são comuns em populações africanas. Infelizmente, pessoas que herdam duas cópias dessas variantes enfrentam um risco muito maior de distúrbios renais agrupados como doenças renais mediadas por APOL1. Trabalhos anteriores mostraram que, quando os níveis de APOL1 aumentam — frequentemente em resposta à inflamação — a proteína pode se tornar tóxica, especialmente nas delicadas células filtrantes do rim conhecidas como podócitos. Mas a maioria dos estudos concentrou-se no que ativa o APOL1. Muito menos se sabia sobre como as células o desligam novamente, por exemplo quebrando a proteína.
Rastreando uma proteína frágil dentro das células
Para explorar a estabilidade de APOL1, os pesquisadores projetaram linhagens celulares humanas para produzir versões marcadas por fluorescência de APOL1 e de seu parente mais próximo, APOL2. Isso permitiu observar quanto de cada proteína se acumulava ou desaparecia em diferentes condições, usando western blot, microscopia e citometria de fluxo. Eles bloquearam a principal maquinaria intracelular de degradação de proteínas, o proteassoma, e separadamente bloquearam a produção de novas proteínas. Quando os proteassomas foram inibidos, os níveis de APOL1 aumentaram rapidamente, mostrando que normalmente ela é degradada em alta velocidade. Quando a síntese proteica foi interrompida, os níveis de APOL1 caíram rapidamente. Em nítido contraste, APOL2 mal se alterou sob qualquer um dos tratamentos, revelando‑a como uma proteína muito mais estável. Importante, o alto turnover de APOL1 foi o mesmo para a versão normal (G0) e para as variantes de risco renal (G1 e G2), e se manteve em várias formas naturais de APOL1 que diferem em como se inserem nas membranas.
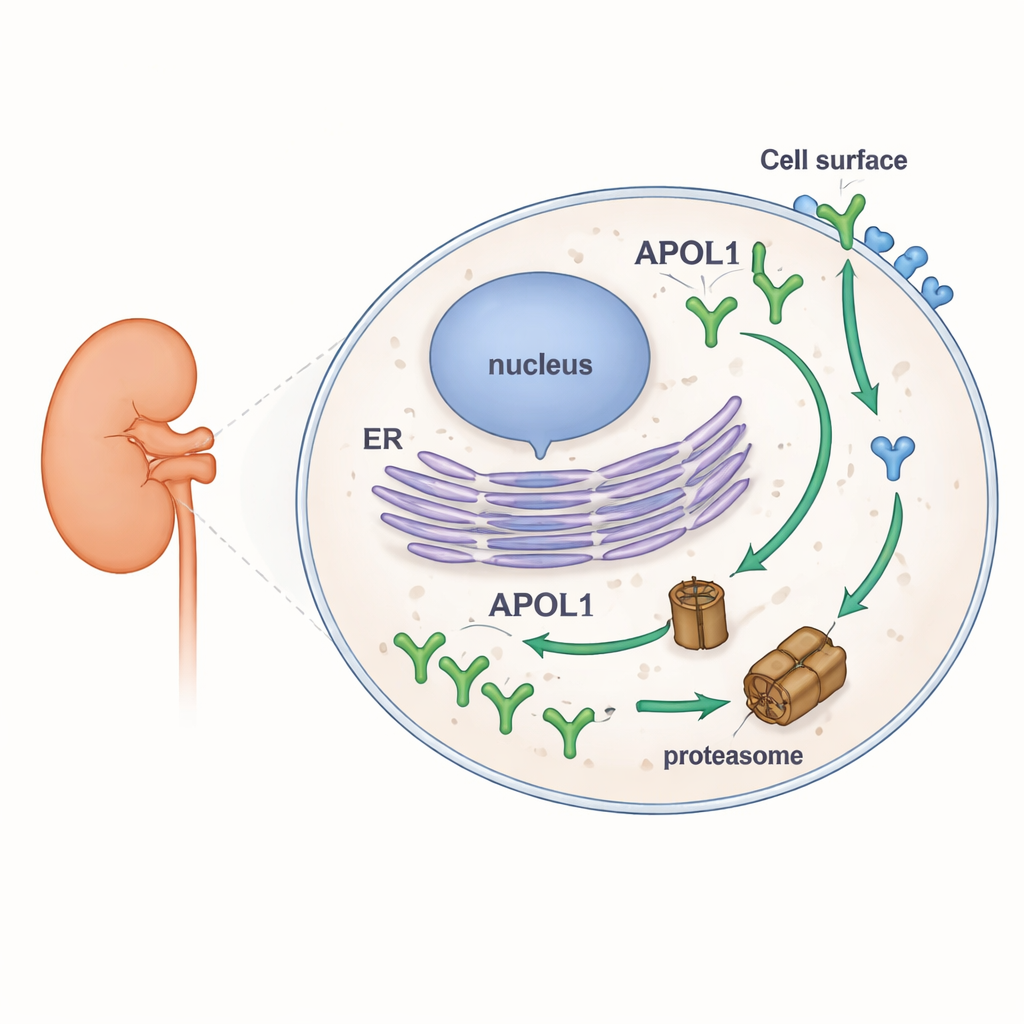
Pistas na sequência e a história de dois bairros
Mergulhando na estrutura da proteína, a equipe usou ferramentas computacionais para analisar APOL1 e APOL2 em busca de segmentos frouxos e não estruturados, conhecidos como regiões intrinsecamente desordenadas. Tais regiões frequentemente atuam como sinais de “coma-me” para o proteassoma. Eles identificaram duas regiões candidatas fortes em APOL1 que estavam amplamente ausentes em APOL2. Para testar se a extremidade frontal única de APOL1 contribui para sua fragilidade, criaram híbridos: um APOL1 encurtado sem seus primeiros 59 aminoácidos, e um quimera de APOL2 carregando esse segmento de APOL1. Adicionar a peça N‑terminal de APOL1 ao APOL2 fez com que o APOL2 se degradasse mais rapidamente, enquanto o APOL1 truncado permaneceu instável, sugerindo que mais de uma parte de APOL1 favorece a degradação rápida. Em conjunto, esses resultados associam os segmentos incomuns e flexíveis de APOL1 ao seu rápido turnover, sem vincular esse comportamento especificamente às variantes causadoras de doença.
Proteína resistente na superfície celular
A descoberta mais marcante surgiu quando os autores distinguiram entre APOL1 dentro da célula e APOL1 na superfície celular. Usando anticorpos que reconhecem apenas a porção de APOL1 exposta ao exterior, mediram os níveis de superfície separadamente dos níveis totais. Dentro da célula, APOL1 comportou‑se como esperado: acumulou‑se quando os proteassomas foram bloqueados e desapareceu rapidamente quando a nova síntese foi interrompida. A APOL1 de superfície, contudo, quase não se alterou em nenhuma das condições. Uma vez que as moléculas de APOL1 alcançavam a membrana plasmática, mostraram‑se altamente resistentes à degradação rápida. Além disso, embora as variantes de risco produzissem menos APOL1 total do que a versão normal, seus níveis de superfície foram semelhantes. Isso sugere que as variantes de risco e a APOL1 normal são removidas em taxas comparáveis dentro da célula, mas que os conjuntos incorporados à membrana — que se pensa formarem canais iônicos e direcionarem a toxicidade — são preservados em todas as variantes.
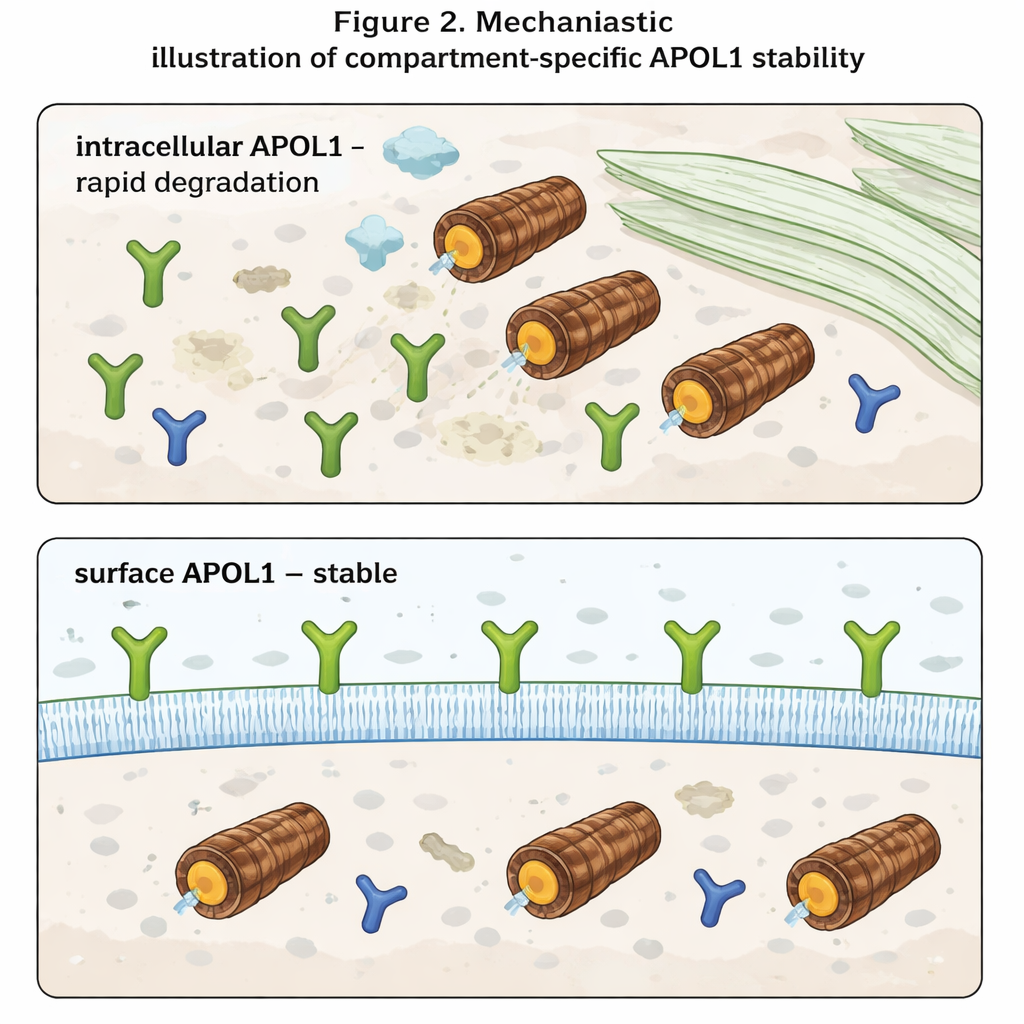
O que isso significa para tratamentos futuros
Para não especialistas, a lição principal é que APOL1 se comporta de maneira muito diferente dependendo de onde se encontra. Dentro da célula, é uma proteína de vida curta, rapidamente reconhecida e destruída. Na superfície celular, torna‑se de longa duração e relativamente protegida, mesmo quando a maquinaria de degradação da célula é alterada. Como a doença parece surgir quando canais de APOL1 na superfície perturbam o equilíbrio de íons como sódio e potássio, as terapias podem precisar focar menos nos níveis totais de APOL1 e mais em quanto dela atinge e persiste na membrana plasmática. Estratégias que reduzam o tráfego de APOL1 para a superfície ou que desestabilizem seletivamente o pool de superfície poderiam, em princípio, atenuar o dano renal sem bloquear completamente as funções imunológicas benéficas do gene.
Citação: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Palavras-chave: APOL1, doença renal, degradação de proteína, membrana plasmática, proteassoma