Clear Sky Science · pt
Caracterização in vitro do domínio catalítico da histona deacetilase humana 5
Por que pequenos interruptores na embalagem do DNA importam
Dentro de cada célula, nosso DNA está enrolado em torno de proteínas que funcionam como bobinas, ajudando a acomodar metros de material genético em um espaço microscópico. Se um gene é ativado ou silenciado muitas vezes depende de pequenas marcas químicas nessas proteínas-bobina. Este estudo focaliza um “interruptor” proteico em particular chamado HDAC5, que está associado a doenças cardíacas, distúrbios neurológicos, câncer e mais. Ao entender como o HDAC5 funciona em nível molecular, os pesquisadores esperam abrir caminho para medicamentos mais precisos e com menos efeitos colaterais.
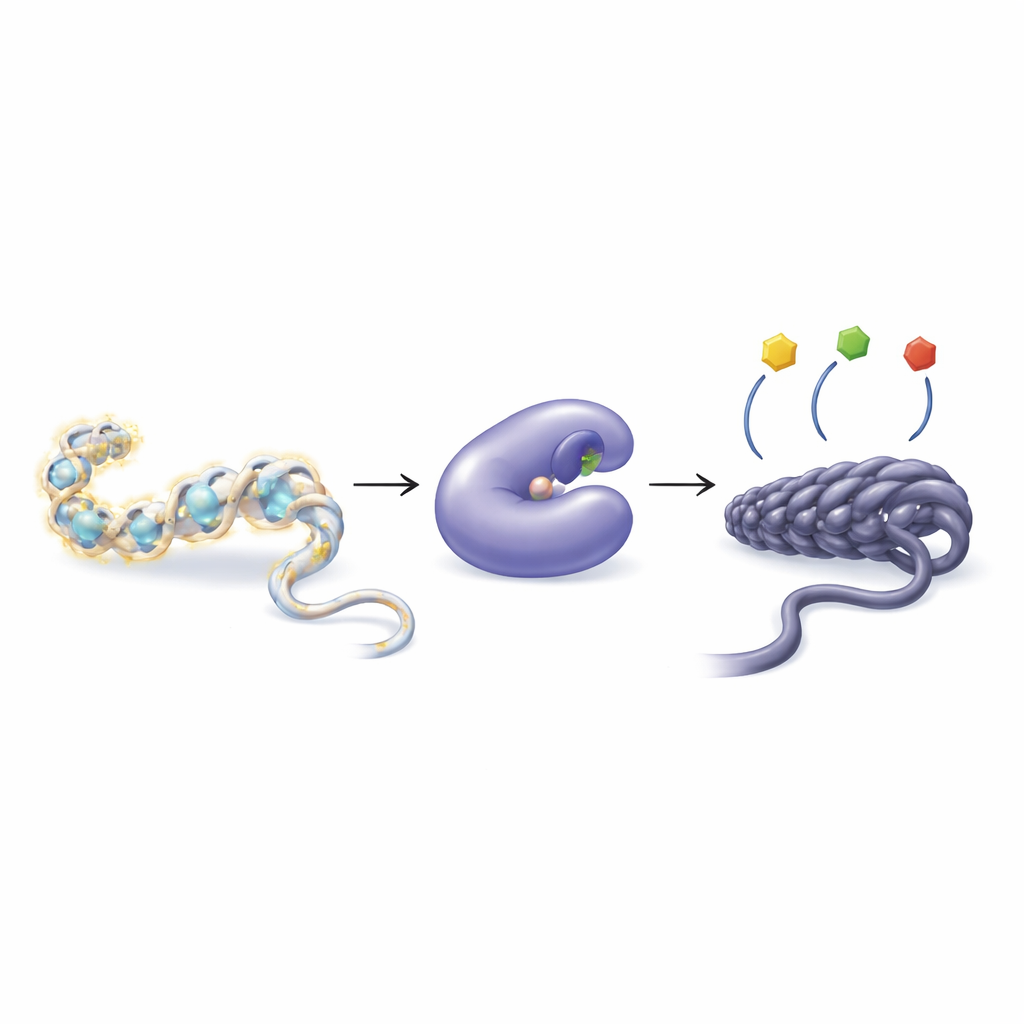
Como as células regulam genes com pequenas marcas químicas
Nosso DNA não flutua livremente, mas está enrolado em torno de proteínas chamadas histonas, formando uma estrutura conhecida como cromatina. As células podem adicionar ou remover pequenos grupos químicos, como grupos acetil, das caudas das histonas para afrouxar ou apertar a cromatina. Um empacotamento mais frouxo geralmente facilita a leitura dos genes; um empacotamento mais denso tende a silenciá-los. Dois grupos de enzimas gerenciam esse equilíbrio: as histona acetiltransferases adicionam grupos acetil, enquanto as histona deacetilases (HDACs) os removem. Quando esse balanço é perturbado, pode contribuir para uma ampla gama de doenças, incluindo câncer, problemas cardíacos, atrofia muscular e distúrbios imunológicos.
Por que o HDAC5 é um alvo promissor, mas complicado
As HDACs formam uma grande família de enzimas relacionadas, divididas em várias classes. Muitos dos medicamentos atualmente em uso clínico bloqueiam vários tipos de HDAC ao mesmo tempo, o que pode interromper funções normais importantes e causar efeitos colaterais intensos. As HDACs de classe IIa, incluindo o HDAC5, destacam-se por serem enriquecidas em tecidos específicos como cérebro, coração e músculo esquelético, e por se associarem a outras proteínas para regular redes gênicas chave. O HDAC5 frequentemente atua como uma ponte, trazendo uma parceira enzimática altamente ativa (HDAC3) até certos genes para que a cromatina seja condensada e esses genes silenciados. Devido a esses papéis focalizados, o HDAC5 é visto como um alvo atraente para fármacos mais seletivos, mas tem faltado dados bioquímicos detalhados e não havia estrutura de alta resolução de seu núcleo ativo, o que dificulta o desenho racional de drogas.
Reconstruindo o HDAC5 em um tubo de ensaio
Para abordar essa lacuna, os pesquisadores produziram apenas o núcleo catalítico do HDAC5 humano — a parte que realiza a reação química — em bactérias, purificaram-no e confirmaram que ele forma uma proteína estável e monomérica em solução. Em seguida, testaram seu desempenho sob diferentes níveis de sal e acidez. A atividade do HDAC5 permaneceu robusta em uma ampla faixa de salinidade e atingiu pico em condições levemente básicas, semelhantes às de muitas células. Usando moléculas fluorescentes especiais como substratos de teste, eles descobriram que a forma natural do HDAC5 reconhece apenas um tipo particular de substrato comumente usado para sondar enzimas da classe IIa. Guiados por trabalhos anteriores em HDACs relacionados, trocaram um único aminoácido (histidina) por uma tirosina em um ponto crítico. Surpreendentemente, essa mudança pequena permitiu que a versão mutante do HDAC5 processasse de forma eficiente ambos os tipos de substratos de teste, revelando como um único resíduo no sítio ativo direciona as preferências químicas da enzima.
Testando e comparando dois novos candidatos a fármacos
A equipe examinou a seguir duas moléculas experimentais que bloqueiam o HDAC5, conhecidas como NT160 e FFK24. Esses compostos usam um novo grupo quelante de zinco que evita parte da toxicidade e da baixa seletividade observadas em drogas antigas à base de hidroxamato. Ao medir como cada inibidor diminuía a atividade do HDAC5 em reações cuidadosamente controladas, os autores determinaram constantes de inibição extremamente baixas na faixa dos nanomolares, o que significa que ambos os compostos se ligam firmemente à enzima. O NT160 ligou-se consistentemente cerca de dez vezes mais fortemente que o FFK24. Para entender por quê, os pesquisadores usaram acoplamento por computador (docking) com uma estrutura do núcleo do HDAC5 prevista pelo AlphaFold. Ambos os inibidores compartilhavam uma região de cabeça comum que se alojava profundamente no bolso ativo e contatava o íon metálico, mas a “cauda” do NT160 formou contatos estabilizadores adicionais com aminoácidos específicos no bolso. Essas interações extras provavelmente explicam sua maior potência.
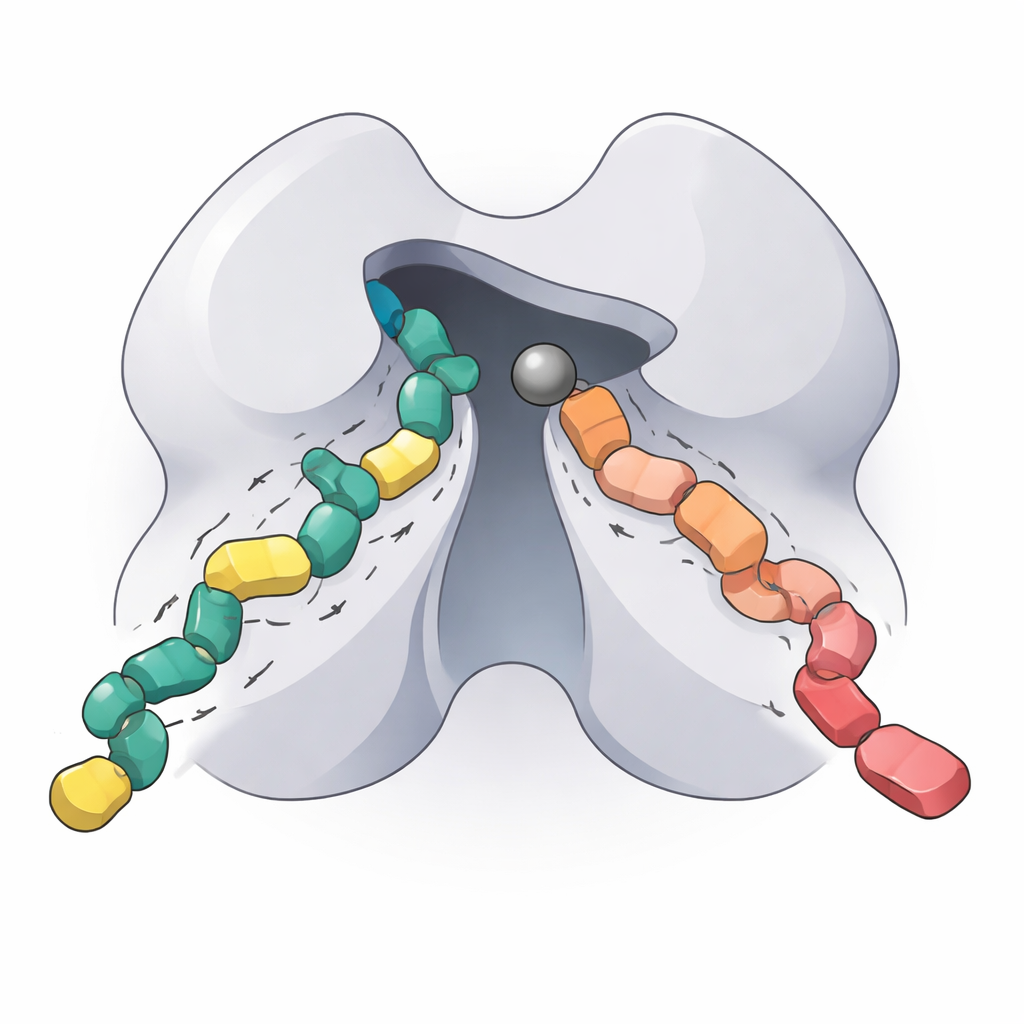
O que isso significa para futuras terapias direcionadas
Ao reconstituir o núcleo funcional do HDAC5, mapear suas condições ótimas de atuação, dissecar como uma única mudança de aminoácido altera seu comportamento e quantificar como dois inibidores de nova geração se ligam, este estudo fornece uma “impressão digital” bioquímica detalhada de uma enzima importante, porém antes pouco caracterizada. Para não especialistas, a conclusão principal é que o HDAC5 ajuda a controlar se certos genes estão ligados ou desligados, e que ajustar com precisão esse interruptor pode ser valioso no tratamento de doenças cardíacas, neurodegeneração, câncer e distúrbios imunológicos. Os novos insights e ferramentas apresentados aqui devem ajudar pesquisadores a projetar fármacos seletivos para HDAC5 e para a classe IIa que atuem onde são necessários, minimizando efeitos indesejados em outras partes do corpo.
Citação: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Palavras-chave: histona deacetilase 5, regulação epigenética, inibidores de HDAC, terapia alvo contra o câncer, estrutura da cromatina