Clear Sky Science · pt
Inativação de LIMK2 suprime a diferenciação de fibroblastos dérmicos induzida por estímulo mecânico e a resistência à apoptose
Por que algumas cicatrizes crescem fora de controle
A maioria dos cortes e feridas cirúrgicas deixa uma linha fina e plana. Mas em algumas pessoas o processo de cicatrização entra em hiperatividade, formando cicatrizes espessas e salientes chamadas cicatrizes hipertróficas ou queloides, que podem coçar, doer e limitar o movimento. Este estudo investiga por que células cutâneas comuns às vezes se tornam produtoras de cicatriz excessivas e aponta para um único interruptor molecular, chamado LIMK2, que pode ser reduzido para evitar que as cicatrizes cresçam descontroladamente.
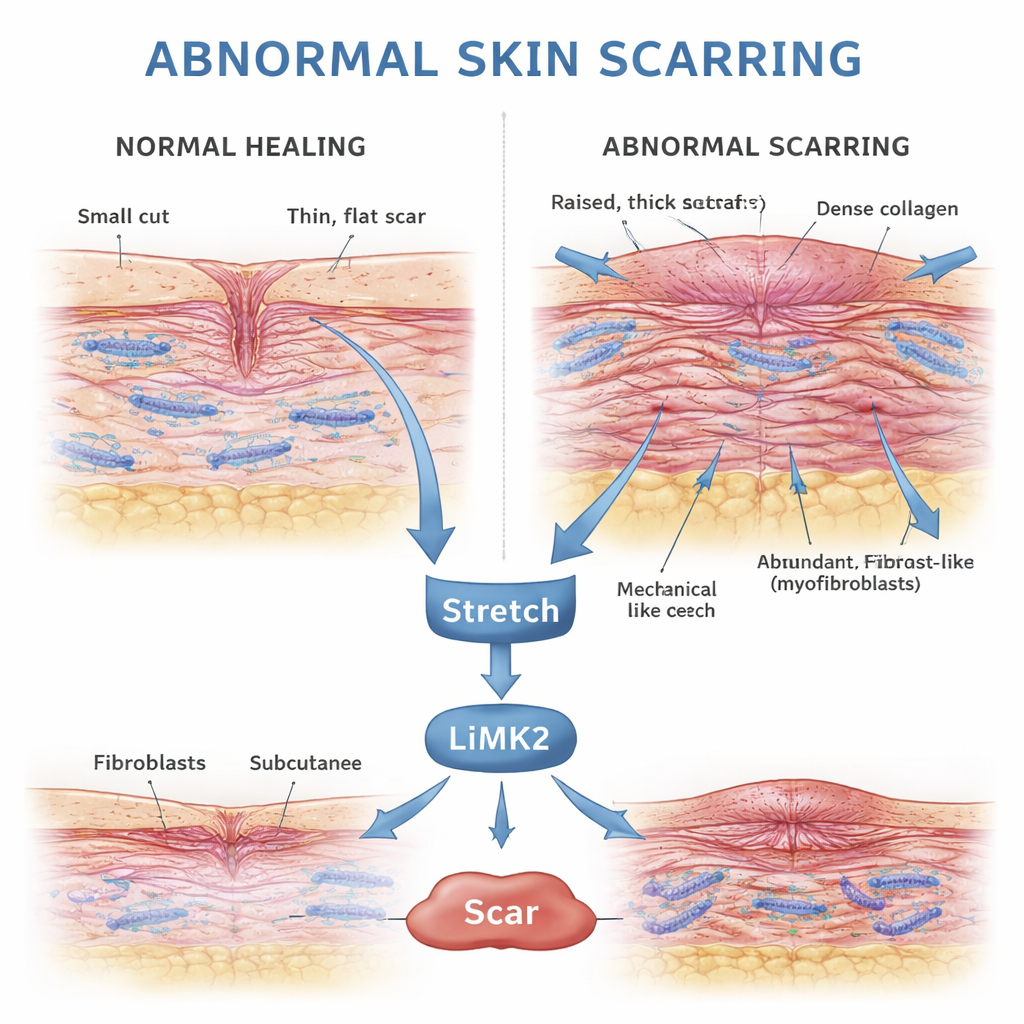
Como a pele normalmente cicatriza após uma lesão
Quando a pele é lesionada, o corpo inicia um programa de reparo cuidadosamente temporizado. Fibroblastos — células “operárias” na camada mais profunda da pele — migram para a ferida, multiplicam-se e depositam colágeno, a estrutura proteica do novo tecido. Muitos desses fibroblastos temporariamente se transformam em uma forma mais forte e contraída chamada miofibroblasto, que ajuda a aproximar as bordas da ferida. Uma vez que a superfície fecha e o tecido novo se estabiliza, esses miofibroblastos deveriam morrer por meio de um processo controlado conhecido como apoptose, deixando para trás uma cicatriz modesta e flexível.
Quando forças cotidianas pioram as cicatrizes
Cicatrizes anormais frequentemente aparecem onde a pele está constantemente esticada — sobre o tórax, ombros ou parte inferior do abdome. Essa observação levou pesquisadores a suspeitar que forças mecânicas, como tração e tensão sobre uma ferida em cicatrização, podem levar fibroblastos a permanecer ativos por tempo demais. Trabalhos anteriores mostraram que esticar essas células em laboratório aumenta uma proteína chamada α-SMA, um marcador de miofibroblastos, e ativa genes que ajudam as células a resistir à apoptose. O novo estudo foca em LIMK2, uma peça-chave de uma cadeia de sinalização mecânica dentro das células que conecta o estiramento físico a mudanças na estrutura interna formada por filamentos de actina.
Um interruptor-chave para células formadoras de cicatriz
Para testar o papel de LIMK2, os pesquisadores usaram fibroblastos dérmicos humanos de pele normal e de tecido queloide. Eles introduziram uma versão desativada de LIMK2 em algumas células, deixando outras inalteradas ou fornecendo uma versão sempre ativa como controles. Quando as células foram submetidas a estiramento mecânico, os fibroblastos normais responderam como esperado: aumento rápido de cofilina fosforilada e fibras de actina mais fortes, aumento de α-SMA, maior produção de colágeno e níveis mais altos de Bcl-2, uma proteína que protege contra a morte celular, juntamente com níveis reduzidos da proteína pró-morte BAX. Em contraste marcante, fibroblastos com LIMK2 inativo mal mudaram sob estiramento. Eles não aumentaram α-SMA, não elevaram Bcl-2 protetor nem reduziram BAX, e apresentaram menos colágeno. Essas células também contraíram géis de colágeno com menos força e se moveram mais lentamente em um ensaio que simula ferida, sugerindo menor capacidade de tração e habilidade reduzida de invadir o tecido ao redor.
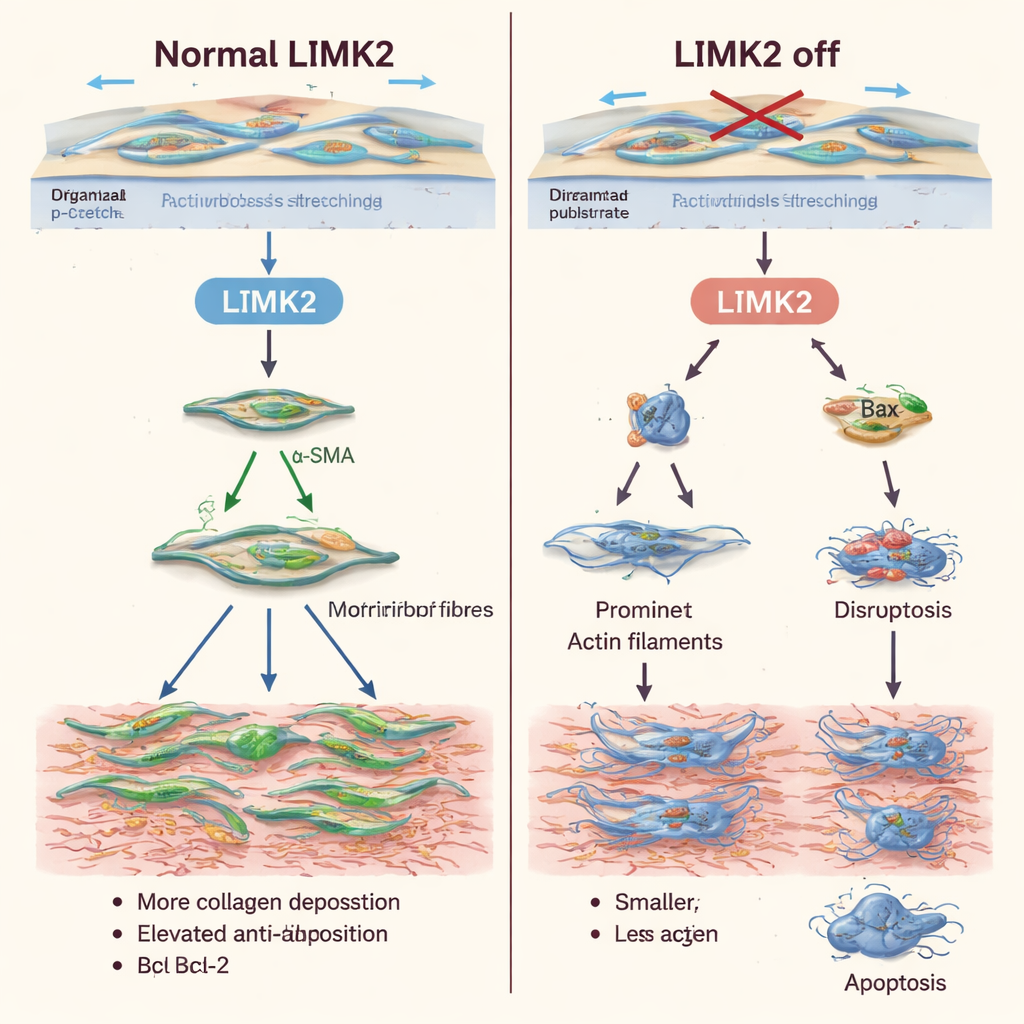
Tornando células de cicatriz persistentes mais fáceis de eliminar
Além de alterar o comportamento dos fibroblastos sob estiramento, desligar LIMK2 os tornou mais propensos a morrer e menos propensos a se multiplicar. Células com LIMK2 inativo mostraram níveis basais mais altos de apoptose, e o estiramento mecânico — normalmente um sinal de sobrevivência — deixou de protegê-las. Citometria de fluxo e marcação fluorescente confirmaram que mais células estavam em estágios iniciais ou tardios de morte programada. Ao mesmo tempo, contagens celulares e testes de marcação de DNA revelaram que essas células se dividiam muito menos do que o normal. Padrões semelhantes apareceram quando a equipe usou latrunculina A, uma droga que desorganiza filamentos de actina, apoiando a ideia de que LIMK2 atua principalmente controlando a estrutura interna da célula.
O que isso pode significar para tratamentos futuros de cicatrizes
As descobertas sugerem que LIMK2 se situa em uma encruzilhada onde forças mecânicas, sobrevivência celular e atividade de formação de cicatriz se intersectam. Quando LIMK2 está ativo, o estiramento empurra os fibroblastos para um estado miofibroblástico robusto e persistente: eles contraem com força, resistem à morte e produzem excesso de colágeno, tudo o que favorece cicatrizes espessas e salientes. Desligar LIMK2 reverte grande parte disso — os fibroblastos tornam-se menos contráteis, menos móveis, menos prolíficos e mais propensos a sofrer apoptose. Para os pacientes, isso aponta para um futuro em que cremes, injeções ou curativos que bloqueiem suavemente LIMK2 ou suas mudanças downstream na actina podem ajudar feridas de alto risco a cicatrizar com cicatrizes mais planas e confortáveis.
Citação: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Palavras-chave: cicatrizes queloides, cicatrização de feridas, fibroblastos, tensão mecânica, apoptose