Clear Sky Science · pt
Mudanças na atividade de EGFR após edição CRISPR/Cas9 do domínio de ligação ao EGF
Por que redirecionar um sinal do câncer importa
O câncer cervical frequentemente depende de um potente interruptor de crescimento chamado receptor do fator de crescimento epidérmico (EGFR). Muitos tumores apresentam quantidades enormes desses receptores, mas fármacos destinados a bloqueá‑los ajudaram apenas uma fração dos pacientes. Este estudo fez uma pergunta fundamental com grandes implicações terapêuticas: o que acontece se você remove a capacidade do EGFR de captar seu sinal de crescimento preferido, o fator de crescimento epidérmico (EGF), sem remover o receptor em si?
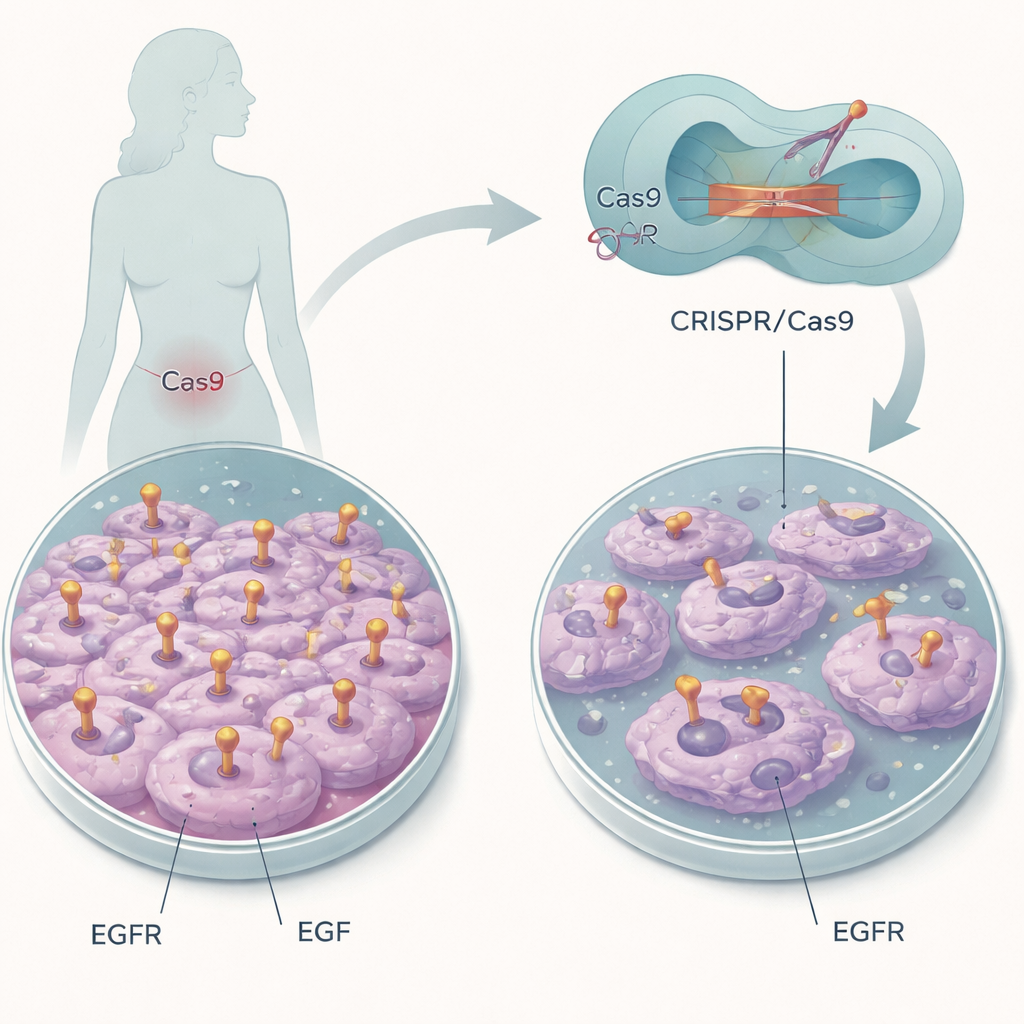
Desligando um “interruptor” molecular
Os pesquisadores focalizaram uma linha celular de câncer cervical que expressa grandes quantidades de EGFR estruturalmente normal. Em vez de destruir o gene, eles usaram a edição genômica CRISPR/Cas9 como um bisturi molecular para alterar apenas alguns aminoácidos no bolso de ligação ao EGF do EGFR. Duas posições em particular, chamadas L14 e Y45, ajudam o EGF a se acomodar no receptor. Ao substituir esses blocos construtores por outros, a equipe buscou manter o EGFR presente, porém cego ao EGF, permitindo isolar o papel dessa única interação no comportamento das células tumorais.
Construindo linhagens celulares tumorais desenhadas
Num primeiro passo, a equipe testou essas mutações em células usando plasmídeos que produzem transitoriamente EGFR normal ou modificado. EGF marcado com fluorescência revelou que todas as formas mutantes ligavam muito menos ligante do que o receptor normal, especialmente quando L14 e Y45 foram alterados juntos. Em seguida, os pesquisadores introduziram essas mudanças diretamente no genoma das células tumorais com CRISPR/Cas9, gerando vários novos clones celulares. Alguns carregavam uma mutação única; outros apresentavam a dupla mutação em uma cópia do EGFR e alterações inativadoras na outra. Modelagens computacionais das formas protéicas resultantes mostraram que essas alterações distorciam o sítio de ligação o suficiente para enfraquecer ou abolir a ancoragem do EGF, consistente com os testes de ligação.
Quando o receptor se move, mas as células sobrevivem
Imagens detalhadas revelaram que os receptores editados se comportavam de forma muito diferente dentro da célula. Em células tumorais não editadas, o EGFR fica na superfície celular, captura o EGF e então se desloca para o interior enquanto é quimicamente ativado por fosforilação. Em clones portadores da mutação dupla, a ligação ao EGF praticamente desapareceu e o EGFR não foi mais observado na membrana; em vez disso, a pequena quantidade de receptor remanescente se acumulou no interior celular. Mesmo uma única alteração em Y45 reduziu substancialmente a ligação e diminuiu os níveis totais de EGFR. Ainda assim, apesar dessa ruptura na via clássica EGF–EGFR, as células cancerosas permaneceram viáveis e continuaram a crescer em cultura com apenas alterações modestas em seus padrões do ciclo celular.
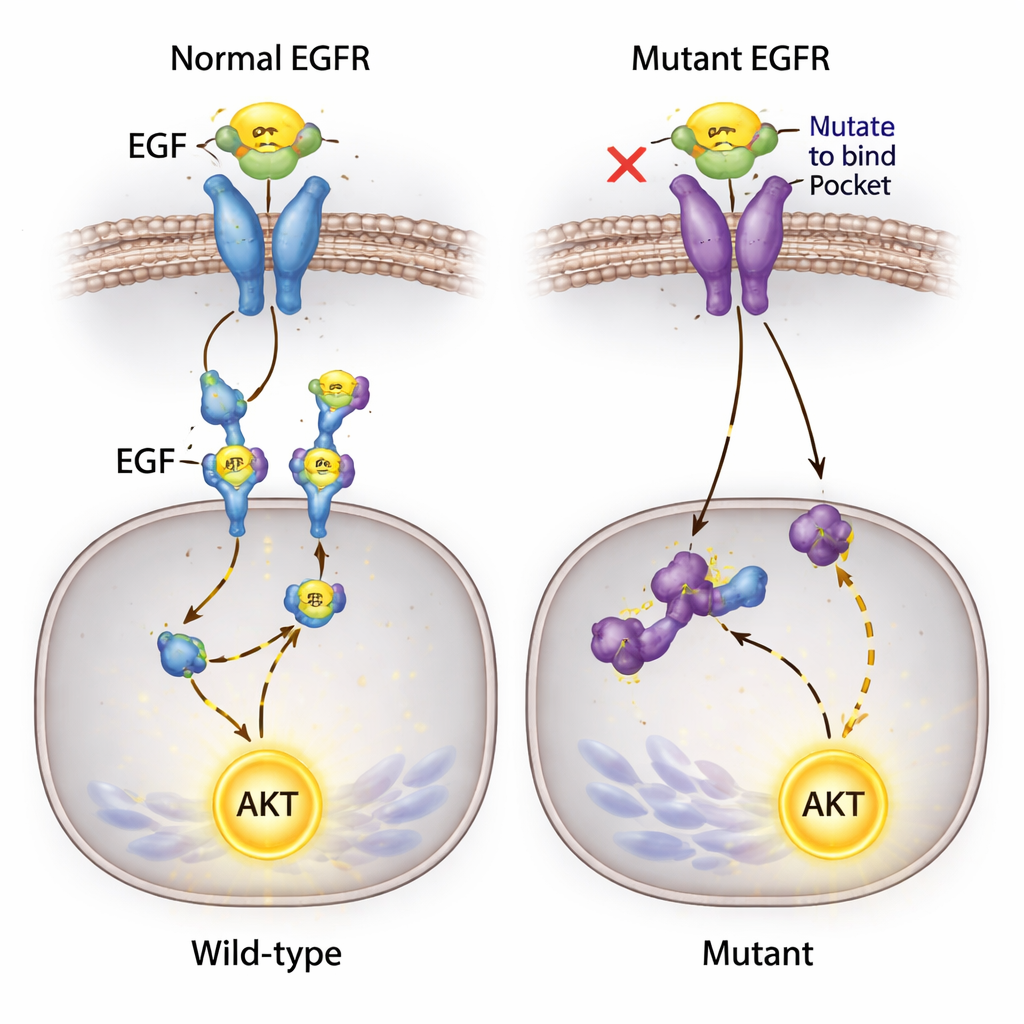
Um sinal inesperado que não desiste
Uma das descobertas mais surpreendentes envolveu a AKT, uma proteína chave que promove a sobrevivência celular e geralmente é ativada a jusante do EGFR. Os pesquisadores esperavam que bloquear a ligação EGF–EGFR silenciasse essa via. Em vez disso, quando adicionaram EGF ao meio, a AKT foi fortemente ativada em todas as linhagens celulares — incluindo aquelas em que o EGF não poderia mais se ligar ao EGFR e onde a fosforilação do receptor era indetectável. Como essas células carregam uma mutação conhecida em outro gene de sinalização, PIK3CA, a equipe suspeita que rotas alternativas podem permitir que o EGF alimente a ativação da AKT, possivelmente por meio de outras proteínas de superfície ou mutações de fundo, contornando o EGFR editado.
Alterações genéticas ocultas e terapias futuras
Para garantir que o CRISPR não estivesse causando edições não intencionais em larga escala, os cientistas sequenciaram os genomas completos das novas linhagens celulares. Confirmaram que as mutações desejadas no EGFR estavam presentes e não encontraram evidências de cortes nos locais fora do alvo previstos para as guias CRISPR. No entanto, detectaram muitas mutações espontâneas espalhadas pelo genoma, algumas das quais podem influenciar o comportamento das células. Isso ressalta que, mesmo quando o CRISPR atinge seu endereço intencional, o DNA naturalmente instável das células cancerosas pode complicar a interpretação dos resultados experimentais e o desenho de terapias gênicas precisas.
O que isso significa para os pacientes
Para um público leigo, a mensagem principal é que bloquear simplesmente o aperto de mão entre EGF e EGFR — mesmo de forma muito precisa ao nível atômico — não interrompe automaticamente os comandos de “crescer e sobreviver” das células cancerosas. O estudo mostra que as células tumorais podem redirecionar sinais chave, como a ativação da AKT, em torno de um receptor bloqueado, e que a própria edição por CRISPR precisa ser avaliada com cuidado em genomas tão instáveis. Essas linhas celulares engenheiradas agora fornecem um modelo laboratorial poderoso para procurar vias alternativas que sustentam tumores dependentes de EGFR, informação que poderá, em última instância, levar a tratamentos combinados que atinjam tanto o EGFR quanto seus cúmplices ocultos.
Citação: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Palavras-chave: EGFR, câncer cervical, CRISPR, sinalização EGF, via AKT