Clear Sky Science · pt
Conjugação de DNA em superfícies plásticas funcionalizadas para sequenciamento sequencial e iterativo de molécula única
Armazenando os dados de amanhã em fios minúsculos
Imagine fazer backup de suas fotos, livros ou registros científicos em uma forma que possa durar séculos e caber em um ponto menor que um grão de areia. O DNA — a mesma molécula que carrega nossos genes — surge como um forte candidato para armazenamento de dados ultra-denso e duradouro. Este artigo explora uma nova maneira de “estacionar” dados em DNA de forma segura no interior de tubos plásticos comuns de laboratório, e então lê‑los repetidas vezes sem destruir as moléculas originais.
Uma nova espécie de “pen drive” de dados
Os discos rígidos e memórias flash de hoje se desgastam, e armazenam muito menos informação por grama do que o DNA potencialmente pode. Pesquisadores já demonstraram como traduzir arquivos digitais em sequências das “letras” do DNA. Mas cada vez que essas fitas de DNA são copiadas ou sequenciadas, parte do material original é consumida, como tinta que desbota ao copiar uma página muitas vezes. Neste estudo, os autores transformaram o humilde tubo PCR de plástico — já padrão em laboratórios de biologia — em um dispositivo físico de armazenamento reutilizável. Eles ligaram quimicamente fitas de DNA que carregavam dados codificados à superfície interna do tubo, de modo que o DNA permanece fixo enquanto cópias são repetidamente produzidas e lidas. 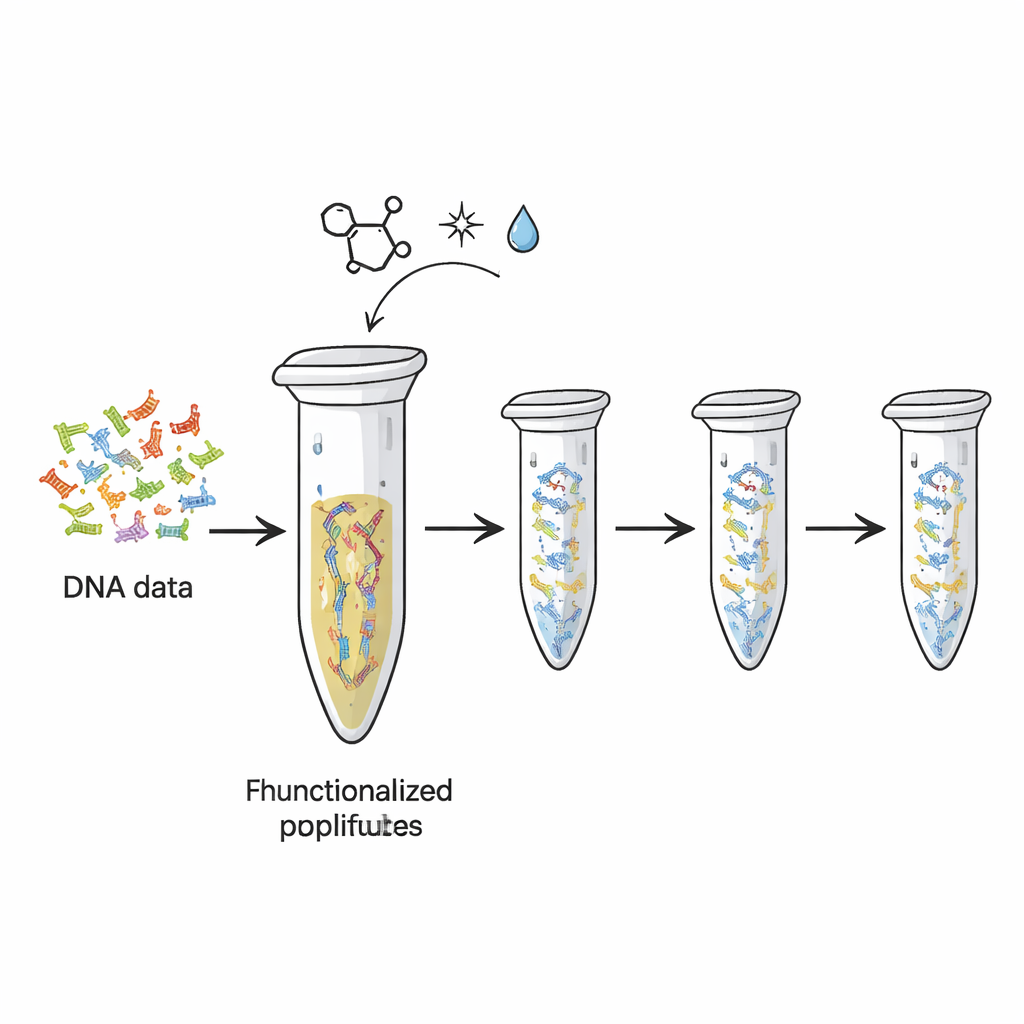
“Colando” DNA no plástico
A equipe recorreu a um tipo de ‘química click’ altamente específica — um conjunto de reações valorizadas por serem rápidas, confiáveis e suaves. Primeiro, adicionaram caudas químicas especiais às extremidades de fitas de DNA que representam diferentes “arquivos” de dados. Essas caudas, baseadas em uma molécula chamada TCO, foram projetadas para se ligar a grupos complementares (MTz) que haviam sido graftados na superfície plástica do tubo. Quando os dois se encontram, formam uma ligação covalente estável, efetivamente colando o DNA ao plástico. Testes com um fragmento de DNA controle mostraram que após incubação quase todo o DNA havia desaparecido da solução, indicando que agora estava imobilizado na parede do tubo. A plataforma podia reter da ordem de centenas de femtomoles de DNA, sugerindo capacidade suficiente para conjuntos de dados práticos.
Recuperando “arquivos” digitais sob demanda
Para verificar se esse DNA preso à superfície ainda se comportava como um arquivo utilizável, os pesquisadores codificaram texto e outros dados em um conjunto de cerca de 15.000 fitas curtas de DNA, agrupadas em 18 “grupos de arquivos”. Cada grupo podia ser copiado seletivamente usando seu próprio par de primers — pequenas sequências iniciais que direcionam a maquinaria de cópia aos alvos corretos. A equipe realizou repetidamente reações padrão de PCR no mesmo tubo, escolhendo a cada vez um grupo de arquivos diferente para amplificar. Após cada rodada, removiam o DNA copiado, limpavam o tubo com enzimas que digerem produtos remanescentes em solução e passavam para o próximo arquivo. O sequenciamento por nanoporo do material copiado mostrou que a maioria dos grupos de arquivos foi recuperada com alta precisão, e a contaminação cruzada de rodadas anteriores permaneceu extremamente baixa, tipicamente em torno de 1% ou menos.
Buscando uma forma mais suave de leitura
Havia, no entanto, um problema: ao repetirem o PCR no mesmo tubo até 18 vezes, a quantidade de DNA recuperada caiu de forma constante. O PCR depende de aquecimento e resfriamento rápidos, e os autores inferiram que as temperaturas repetidas e elevadas estavam danificando o DNA imobilizado ou sua conexão com o plástico, embora testes de controle sugerissem que o DNA não estava simplesmente sendo lavado para a solução. Para resolver isso, recorreram à amplificação por recombinase‑polimerase (RPA), um método mais recente que opera a uma única temperatura relativamente baixa, próxima à temperatura corporal. Usando RPA em tubos recém‑revestidos com DNA, novamente consultaram os 18 grupos de arquivos em sequência. Desta vez, os rendimentos foram elevados — cerca de 60 ng/µL — e não mostraram a mesma tendência de queda. O padrão de quais fitas eram favorecidas ou desfavorecidas durante a cópia também correspondeu de perto ao observado quando o DNA estava livre em solução. 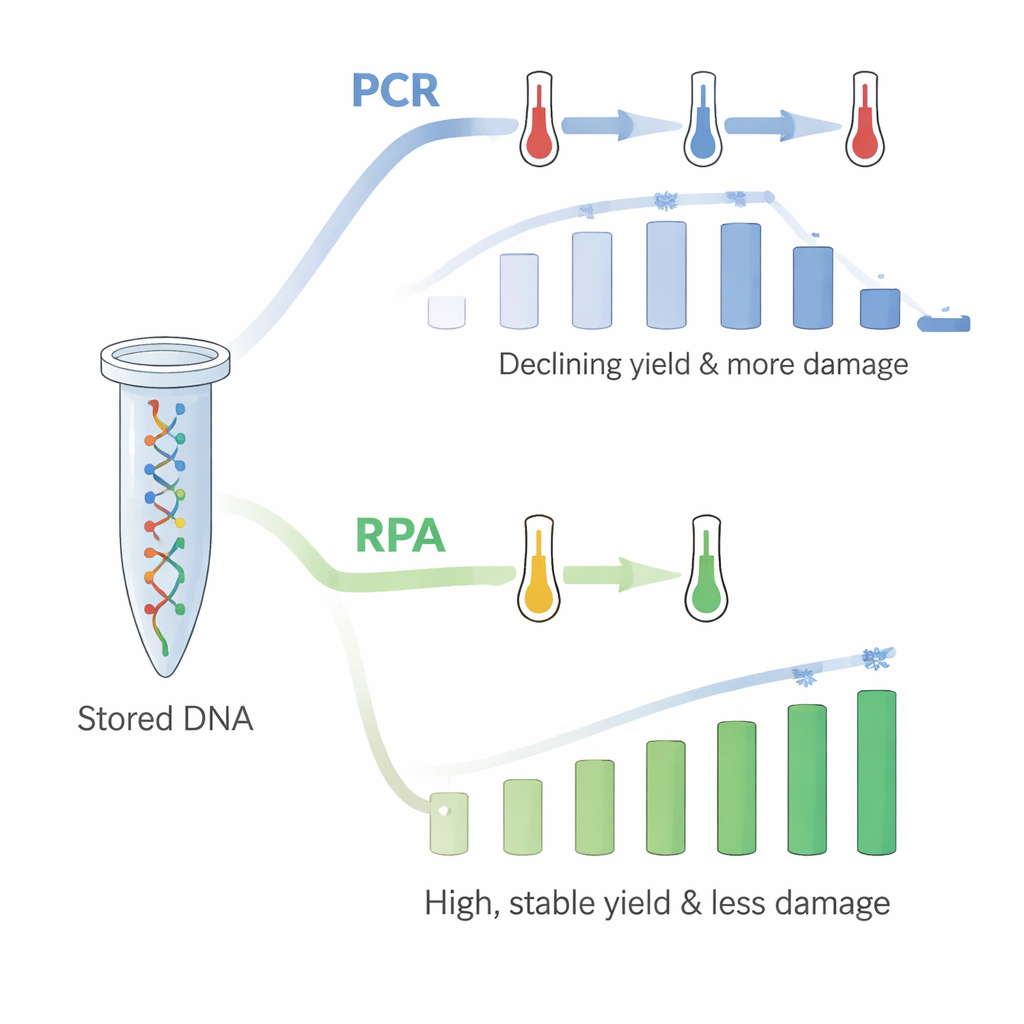
Rumo a uma memória de DNA portátil e duradoura
Ao combinar química click robusta com cópia de DNA a baixa temperatura, este trabalho aponta para uma maneira prática de transformar tubos plásticos simples em cartuchos reutilizáveis de dados em DNA. O DNA permanece fisicamente preso ao tubo, onde pode ser consultado repetidamente para arquivos específicos sem consumir as moléculas originais, especialmente ao usar o método mais suave de RPA. Para não especialistas, a mensagem principal é que o DNA não é apenas o código da vida — ele também pode atuar como um meio de armazenamento digital compacto e durável. Métodos como este nos aproximam de um futuro em que seus backups de longo prazo possam residir não em discos giratórios, mas em moléculas cuidadosamente projetadas repousando silenciosamente em uma prateleira de laboratório.
Citação: Roy, S., Ji, H.P. & Lau, B.T. DNA conjugation on functionalized plastic surfaces for sequential, iterative single molecule sequencing. Sci Rep 16, 6467 (2026). https://doi.org/10.1038/s41598-026-37575-y
Palavras-chave: armazenamento de dados em DNA, química click, conjugação em superfície plástica, amplificação por recombinase-polimerase, sequenciamento por nanoporo