Clear Sky Science · pt
Uma abordagem com ligase de biotina dividida revela proteínas associadas à alfa-sinucleína oligomérica durante a agregação
Por que proteínas aglomeradas no cérebro importam
Na doença de Parkinson e em condições relacionadas, uma proteína cerebral normalmente útil chamada alfa‑sinucleína pode se aglomerar em depósitos pegajosos conhecidos como corpos de Lewy. Esses depósitos surgem décadas antes dos sintomas e são uma característica definidora observada na autópsia, mas ainda não sabemos quais outras proteínas ajudam a empurrar a alfa‑sinucleína de um estado inofensivo para agregados perigosos. Este estudo usa uma engenhosa “etiqueta de proximidade” molecular para mapear quais proteínas ficam próximas à alfa‑sinucleína enquanto ela passa de moléculas isoladas para pequenos aglomerados, oferecendo novas pistas sobre como a doença começa e quais vias podem ser alvo para retardá‑la ou preveni‑la.
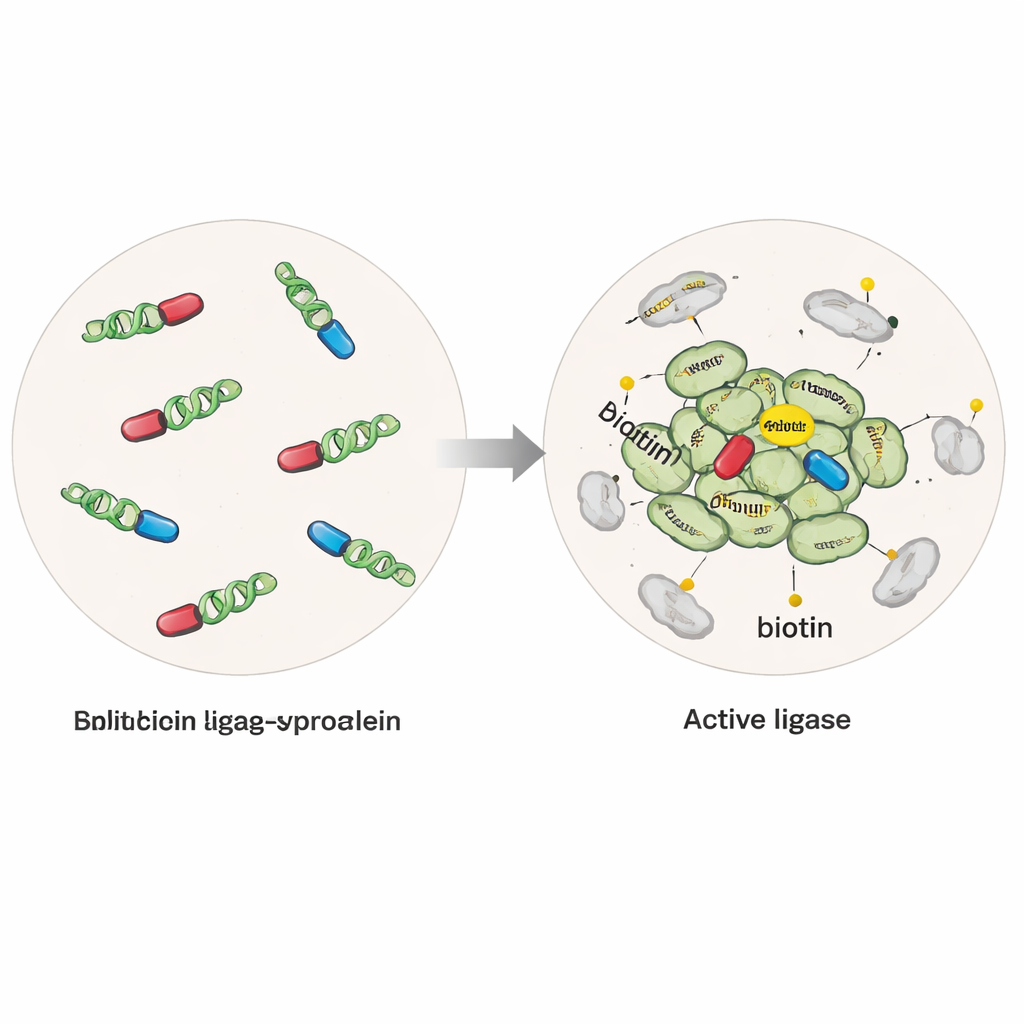
Uma “etiqueta” molecular que acende os vizinhos
Os pesquisadores modificaram células humanas para produzir alfa‑sinucleína fundida a uma enzima alterada que pode acrescentar uma pequena etiqueta de biotina a qualquer proteína dentro de alguns bilionésimos de metro. Em uma versão, a enzima estava intacta e ativa sempre que a alfa‑sinucleína estava presente, capturando proteínas próximas tanto de moléculas isoladas quanto de aglomerados. Em uma segunda versão “dividida”, mais seletiva, a enzima foi cortada em duas metades inativas, cada uma ligada a uma molécula separada de alfa‑sinucleína. Somente quando moléculas de alfa‑sinucleína se reuniam em multímeros ou oligômeros as metades se reuniam em uma enzima ativa, ligando a marcação especificamente ao redor desses agregados iniciais. Ao adicionar fibrilas purificadas de alfa‑sinucleína às células, a equipe também pôde induzir agregação semelhante à da doença e comparar estados normais versus patológicos.
Construindo um mapa de proteínas vizinhas
Depois de permitir tempo para a marcação, a equipe isolou todas as proteínas rotuladas com biotina e as identificou por espectrometria de massas, uma técnica que pesa e conta proteínas com alta precisão. Em todas as condições, encontraram 1.277 proteínas distintas e, após filtragem criteriosa, reduziram esse número para 581 que provavelmente estavam genuinamente próximas à alfa‑sinucleína. Comparando os sistemas com a enzima intacta e dividida, puderam distinguir proteínas que se associam principalmente a moléculas isoladas daquelas que preferem multímeros. Também compararam células com e sem adição de fibrilas para ver como o ambiente proteico local da alfa‑sinucleína muda quando a agregação é desencadeada.
Principais vias celulares atraídas para os aglomerados
O esboço do interatoma resultante aponta para vários temas biológicos importantes. Em condições normais, a alfa‑sinucleína multimérica estava próxima de muitas proteínas de tráfego de membrana e enzimas modificadoras de proteínas—consistente com seu papel proposto em ajudar os neurônios a manejar vesículas sinápticas e manter o controle de qualidade proteico. Várias enzimas que adicionam grupos fosfato, incluindo as quinases PAK4, RIPK2 e MAP4K4, foram enriquecidas perto dos multímeros saudáveis, mas pareciam perder contato quando os agregados se formavam, sugerindo que a ruptura dessas relações pode favorecer formas da proteína associadas à doença. A equipe também detectou proteínas ligadas à sinalização do fator de crescimento semelhante à insulina, apoiando conexões clínicas entre resistência à insulina e doença de Parkinson, e encontrou que a agregação recruta proteínas envolvidas na eliminação de proteínas danificadas, como a família de chaperonas 14‑3‑3 e componentes específicos das vias de degradação celular.
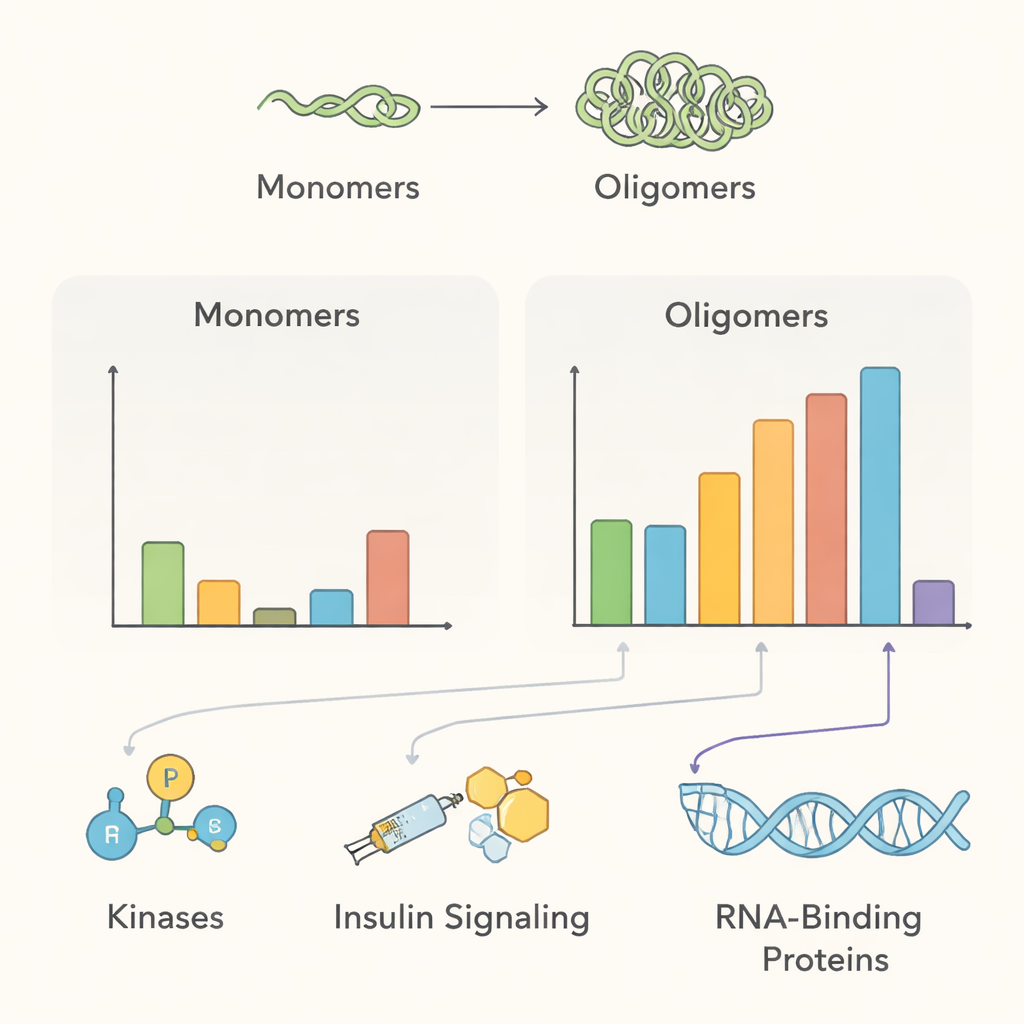
Pontes inesperadas para outros transtornos cerebrais
Além da doença de Parkinson, os dados destacam uma conexão surpreendente com a esclerose lateral amiotrófica (ELA) e a demência frontotemporal (DFT). Uma proteína de ligação ao RNA chamada FUS, que se deslocaliza e agrega nessas condições, apareceu próxima à alfa‑sinucleína multimérica tanto em condições normais quanto nas induzidas à agregação. Outras proteínas relacionadas ao RNA também mudaram sua proximidade conforme a alfa‑sinucleína agregava. Esses achados levantam a possibilidade de que pequenos complexos de alfa‑sinucleína possam prender proteínas responsáveis pelo processamento de RNA no lugar errado dentro das células, ligando potencialmente a biologia das doenças por corpos de Lewy à da ELA e DFT, embora interações físicas diretas ainda precisem ser verificadas.
O que isso significa para entender a doença
Para não especialistas, a principal conclusão é que este trabalho fornece uma “lista de contatos” em estágio inicial de proteínas que acompanham a alfa‑sinucleína à medida que ela passa de um ajudante normal a um aglomerado nocivo. O estudo sugere que a perda de certas relações protetoras—como com quinases específicas ou enzimas de controle de qualidade—pode ser tão importante quanto a aquisição de novos parceiros tóxicos. Embora os experimentos tenham sido realizados em um modelo celular simplificado e ainda não provem causa e efeito, eles destacam candidatos e vias concretas para testes futuros em neurônios e tecido cerebral. A longo prazo, mapear esses bairros proteicos em mudança pode orientar estratégias para restaurar interações protetoras, apoiar a sinalização relacionada à insulina ou impedir a captura de proteínas ligadoras de RNA, potencialmente diminuindo a progressão de mudanças moleculares sutis para doenças por corpos de Lewy plenamente desenvolvidas.
Citação: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Palavras-chave: alfa-sinucleína, doença de corpo de Lewy, agregação de proteínas, proteômica de proximidade, doença de Parkinson