Clear Sky Science · pt
Imobilização covalente da peroxidase de Lepidium draba em nanopartículas magnéticas revestidas com quitosana e sua aplicação na biossensoriamento de glicose
Por que ímãs minúsculos importam para o açúcar no sangue
Manter a glicemia sob controle é crítico para manejar o diabetes e prevenir danos a longo prazo ao coração, rins, olhos e nervos. Os testes de glicose atuais funcionam bem, mas as enzimas neles podem ser frágeis, de curta duração e difíceis de reutilizar, o que aumenta custos e resíduos. Este estudo explora uma maneira engenhosa de tornar uma enzima vegetal mais resistente e duradoura ao fixá‑la em microesferas magnéticas, abrindo caminho para testes de glicose mais rápidos, mais confiáveis e potencialmente mais baratos.
Uma ajuda vegetal inspirada na raiz‑forte
Muitos testes médicos dependem de enzimas — proteínas que aceleram reações químicas. Um coringa em laboratórios diagnósticos é a peroxidase de raiz‑forte, usada para transformar alterações químicas invisíveis em mudanças de cor claras, visíveis a olho nu. Os pesquisadores trabalharam com um parente próximo dessa enzima, chamada peroxidase de Lepidium draba, produzida em bactérias para possibilitar produção em larga escala. Sozinha, essa enzima livre é potente, mas delicada: perde atividade com calor, armazenamento e uso repetido, o que limita seu valor em sensores industriais e kits clínicos.
Transformando enzimas em ferramentas magnéticas
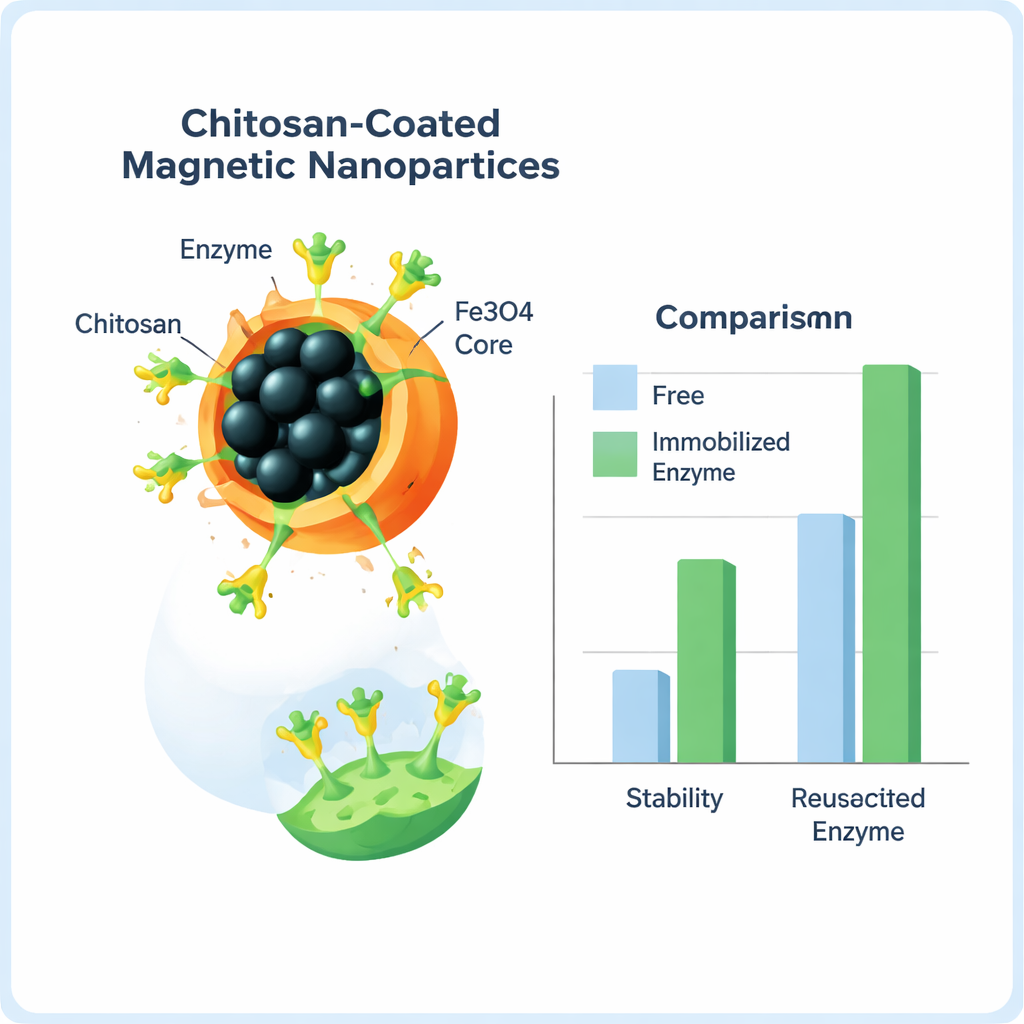
Para proteger e reutilizar a enzima, a equipe a fixou em nanopartículas de óxido de ferro — grânulos minúsculos de material magnético — revestidos com um polímero natural chamado quitosana, derivado de cascas de crustáceos. A quitosana fornece uma camada macia e biocompatível repleta de “alças” químicas que podem prender enzimas. Usando uma pequena molécula entrecruzante, glutaraldeído, formaram ligações covalentes fortes entre a enzima e as partículas revestidas. Os cientistas então ajustaram a quantidade de entrecruzante, o tempo da reação e a quantidade de suporte, optando por condições que proporcionaram o melhor equilíbrio entre quanto de enzima aderiu e quanta atividade ela manteve.
Verificando estrutura, resistência e durabilidade
Após a imobilização, a equipe confirmou que a enzima realmente estava sobre as partículas usando várias ferramentas estruturais que leem vibrações de ligação, padrões cristalinos e morfologia da superfície. Mais importante para uso prático, a enzima imobilizada teve desempenho superior à sua forma livre. Ela se ligou mais prontamente ao substrato corante e o converteu em produto colorido com muito mais eficiência — em alguns testes, até 11 vezes maior eficiência catalítica. A enzima ligada também tolerou uma faixa mais ampla de acidez, manteve maior atividade em temperaturas úteis e resistiu ao aquecimento a 50 °C por muito mais tempo. Sua meia‑vida nessa temperatura mais que dobrou e, após dois meses na geladeira, reteve aproximadamente o dobro da atividade da enzima livre. Como as partículas são magnéticas, poderiam ser retiradas da solução com um ímã e reutilizadas; mesmo após 11 ciclos de reação, cerca de 40% da atividade inicial permanecia.
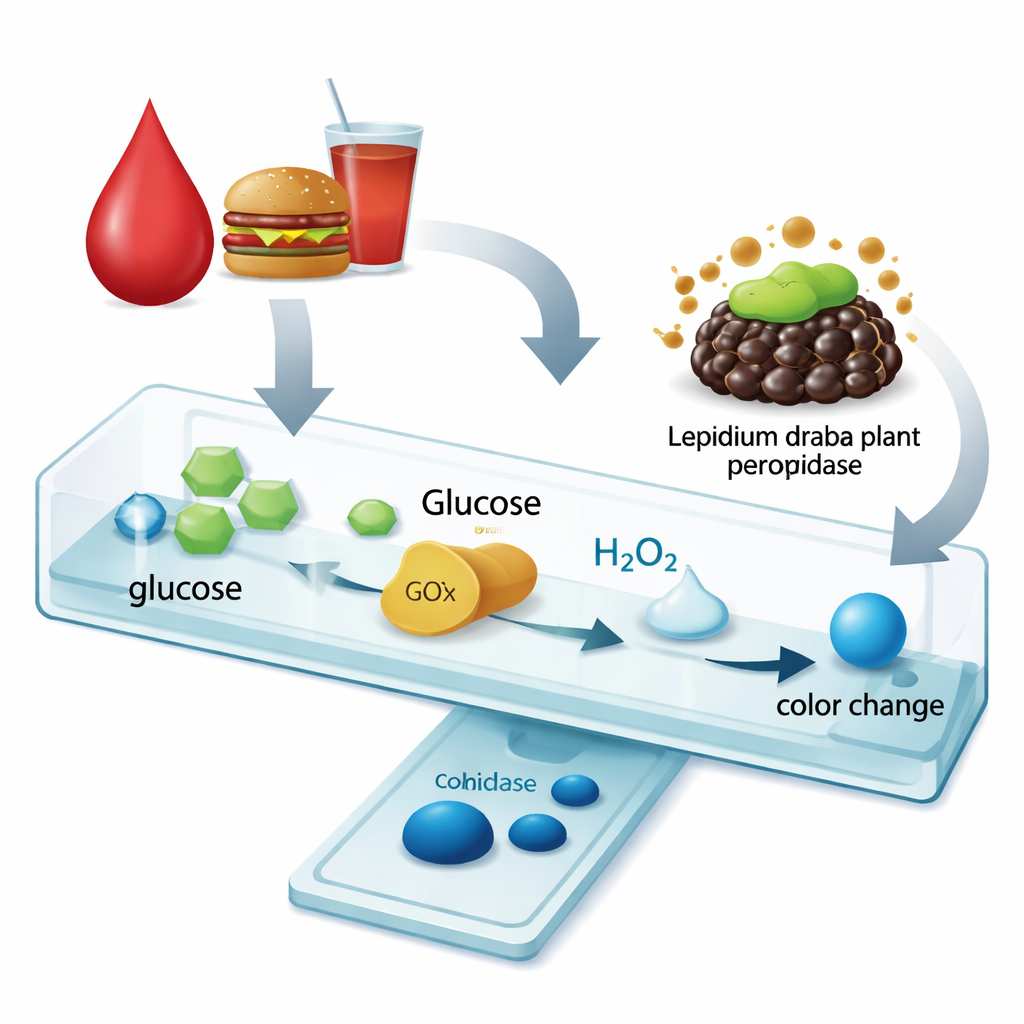
Mudança de cor mais nítida para testes de glicose
Para verificar se essa enzima mais resistente realmente melhora um teste prático, os pesquisadores montaram um ensaio simples de glicose baseado em cor. Primeiro, a enzima glicose oxidase padrão converte a glicose em peróxido de hidrogênio. Em seguida, a peroxidase de Lepidium draba, livre ou imobilizada nas esferas magnéticas de quitosana, usa esse peróxido para transformar um corante incolor em azul intenso. Com a forma imobilizada, a faixa útil de medição da glicose se expandiu dramaticamente — passando de apenas 0,1 a 1 milimol por litro com a enzima livre para 0,1 a 10 milimoles por litro quando imobilizada. Ao mesmo tempo, o tempo de reação necessário para o ensaio caiu para cerca de um terço, enquanto o nível mínimo detectável de glicose permaneceu muito baixo e clinicamente relevante.
O que isso significa para a saúde do dia a dia
Ancorando uma enzima vegetal em nanopartículas magnéticas revestidas com quitosana, os autores criaram um componente de sensor de glicose colorimétrico robusto, reutilizável e altamente sensível. Para o público em geral, isso significa que futuras tiras de teste, kits de laboratório ou mesmo embalagens inteligentes para alimentos podem se tornar mais estáveis, mais precisas em uma faixa maior de açúcares e potencialmente mais baratas porque a enzima ativa pode ser recuperada e reutilizada. Embora sejam necessários trabalhos adicionais para aumentar quanto de enzima as partículas podem suportar e para estender a abordagem a outros marcadores sanguíneos como colesterol ou ureia, este estudo mostra como nanomateriais e polímeros naturais podem trabalhar juntos para aprimorar ferramentas bioquímicas familiares, tornando‑as mais resistentes, limpas e versáteis para diagnósticos.
Citação: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Palavras-chave: biossensor de glicose, imobilização de enzimas, nanopartículas magnéticas, detecção colorimétrica, peroxidase