Clear Sky Science · pt
Validação de um novo biomarcador genômico de escalabilidade de células-tronco mesenquimais e implicações do status genotípico nos fenótipos de senescência celular
Por que cultivar células-tronco fica mais difícil com o tempo
Células-tronco da medula óssea adulta são um pilar de muitas terapias experimentais, desde reparar ossos danificados até reduzir inflamação. Mas há um problema: para tratar um paciente, os laboratórios precisam expandir essas células fora do corpo, e quanto mais elas são cultivadas, mais desaceleram e passam a se comportar como células “envelhecidas”. Este estudo investiga por que as células-tronco de algumas pessoas envelhecem mais devagar em placa de cultura e se uma pequena ausência de DNA pode ajudar cientistas a selecionar as células mais robustas para tratamentos futuros.
Um gene ausente que muda as regras
Os pesquisadores focaram em um gene chamado GSTT1, que ajuda as células a desintoxicar moléculas nocivas produzidas durante o metabolismo normal e sob estresse. Surpreendentemente, uma fração considerável de pessoas não possui esse gene — são “GSTT1 nulos”. Trabalhos anteriores sugeriam que células-tronco da medula óssea desses indivíduos poderiam crescer mais rápido e manter suas tampas cromossômicas protetoras, chamadas telômeros, mais longas. Neste projeto, a equipe examinou células-tronco de seis doadores saudáveis, agrupou-as em GSTT1-positivas e GSTT1-nulas e acompanhou como as células se comportavam ao longo de muitas rodadas de expansão e após exposição a radiação X, um forte indutor de envelhecimento celular.
Células que crescem rápido e resistem a sinais de envelhecimento
Quando os cientistas acompanharam o número de células ao longo de vários dias, as células-tronco GSTT1-nulas se multiplicaram mais rapidamente em passagens iniciais do que as células que carregavam o gene. Em expansões muito longas, as taxas de crescimento entre os grupos tornaram-se mais semelhantes, mas a vantagem inicial foi clara. Para sondar o envelhecimento diretamente, a equipe usou uma coloração clássica que torna as células senescentes, ou “envelhecidas”, azuis. Após muitas rodadas de divisão, e novamente após irradiação, os cultivos GSTT1-nulos consistentemente continham menos células azuis senescentes do que os cultivos GSTT1-positivos. Importante: essa diferença não veio de um encurtamento mais lento dos telômeros nem de maior atividade da enzima que mantém telômeros (hTERT); ambas as medidas eram semelhantes independentemente do status GSTT1, sugerindo que outro mecanismo estava em ação.
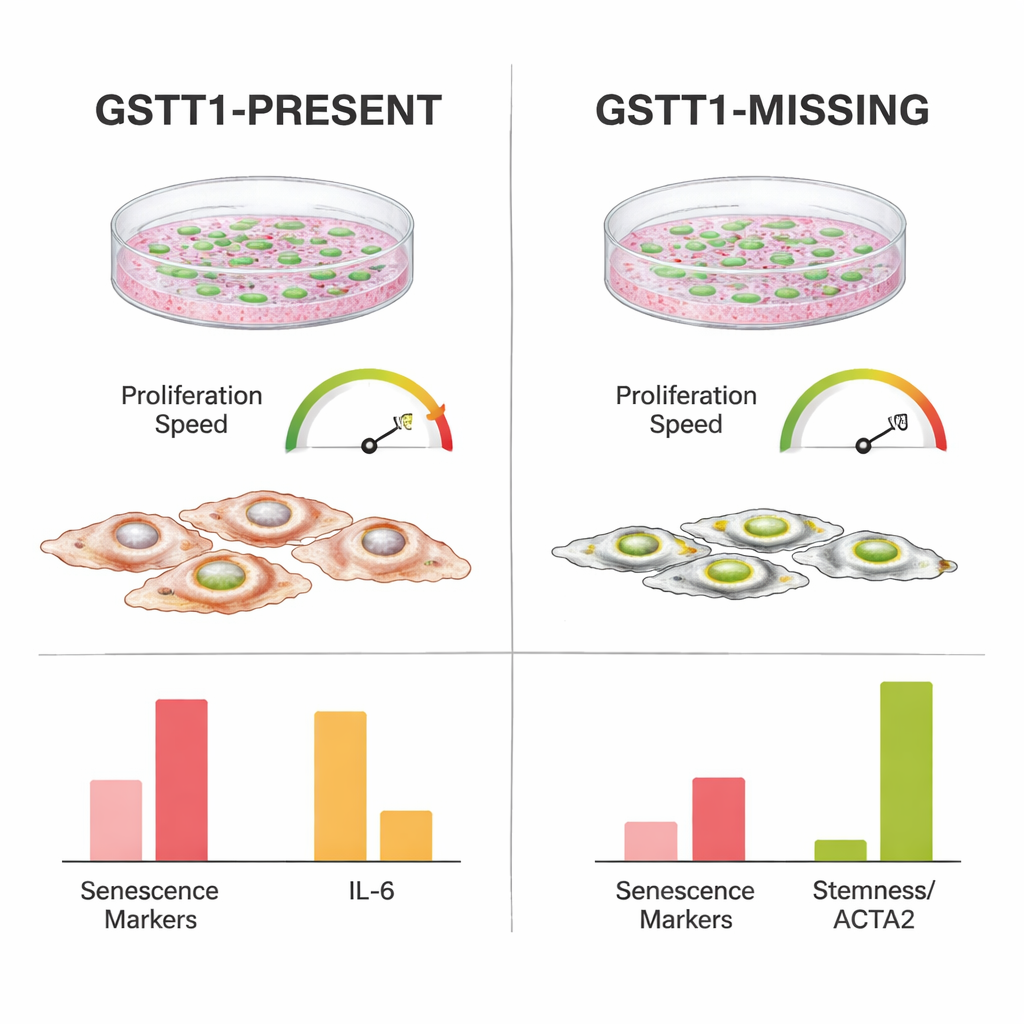
Menos estresse e inflamação na placa de cultura
Para entender o que tornava as células GSTT1-nulas mais resilientes, os pesquisadores mediram a atividade de genes ligados à parada do ciclo celular, dano ao DNA e ao chamado fenótipo secretor associado à senescência — um coquetel de sinais inflamatórios e de estresse liberados por células envelhecidas. Células com GSTT1 presente mostraram níveis mais altos de sinais-chave de “pare”, como p21 e p14, especialmente em passagens tardias e após irradiação. Elas também aumentaram IL‑6, uma molécula inflamatória potente, e outros genes relacionados ao estresse mais fortemente do que as células GSTT1-nulas. Em contraste, células-tronco GSTT1-nulas mantiveram níveis mais baixos desses marcadores de envelhecimento e inflamação, enquanto preservavam níveis mais altos de ACTA2 e TWIST1, genes associados à integridade estrutural e comportamento semelhante a células-tronco. Notavelmente, ambos os genótipos conservaram habilidade semelhante para se especializar em células ósseas e adiposas, o que significa que o efeito protetor não se devia simplesmente à perda da função normal de célula-tronco.
O que isso pode significar para futuras terapias celulares
Em conjunto, os achados sugerem que células-tronco da medula óssea que não possuem GSTT1 estão parcialmente protegidas do desgaste habitual da expansão em laboratório e da radiação. Elas crescem mais rápido no início, acumulam menos células claramente envelhecidas e mantêm um perfil menos inflamatório, embora seus cromossomos encurtem em taxas semelhantes. Para empresas e clínicas que fabricam grandes quantidades de células-tronco, o status GSTT1-nulo poderia servir como um marcador genético prático para identificar doadores cujas células toleram melhor a expansão, potencialmente resultando em terapias mais consistentes e potentes. Claro, o estudo usou um número pequeno de doadores e condições de cultura não clínicas, portanto são necessários estudos maiores e controlados. Ainda assim, o trabalho destaca como uma única diferença herdada pode inclinar a balança entre comportamento juvenil e envelhecido em células-tronco cultivadas para medicina regenerativa.
Citação: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Palavras-chave: células-tronco mesenquimais, senescência celular, biomarcadores, fabricação de terapia celular, polimorfismo GSTT1