Clear Sky Science · pt
Aprisionamento de sensor de voltagem excepcionalmente seletivo dos canais NaV1.5 pelo Mg-protoporfirina prejudica a migração de células cancerosas
Pigmento vegetal aponta para nova estratégia contra o câncer
Nossos corações e nossos tumores podem compartilhar uma vulnerabilidade inesperada: um tipo especial de portão elétrico na membrana celular chamado NaV1.5. Este estudo mostra que um parente natural dos blocos de construção da clorofila nas plantas, a magnézio‑protoporfirina IX (MgPpIX), pode fechar esse portão com precisão extraordinária. Ao fazê-lo, ela reduz drasticamente o movimento de certas células cancerosas — sugerindo que uma molécula inspirada na química da fotossíntese poderia ajudar a conter a metástase sem perturbar fortemente o cérebro ou os músculos.
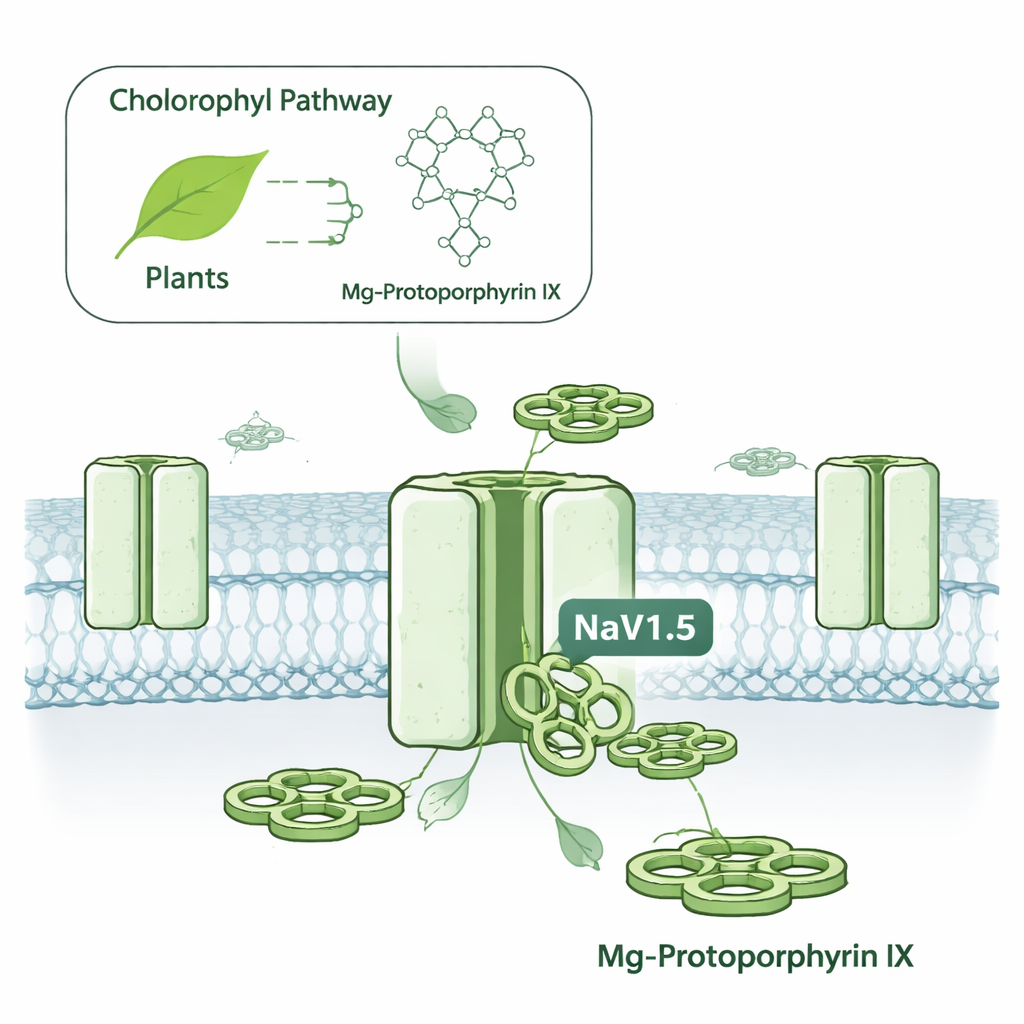
Um interruptor elétrico oculto em células cancerosas
As células usam canais de sódio dependentes de voltagem como pequenas portas que se abrem e fecham para permitir a passagem de partículas carregadas, gerando sinais elétricos. A NaV1.5 é mais conhecida por seu papel nos batimentos cardíacos, onde ajuda a desencadear cada contração. Mas o mesmo canal também é encontrado em vários cânceres, incluindo tumores de mama e cólon, onde sua atividade tem sido associada ao aumento da mobilidade e da invasividade celular. Alvejar a NaV1.5 tem sido difícil porque a maioria dos fármacos para canais de sódio também atinge canais relacionados em nervos e músculo esquelético, arriscando efeitos colaterais como convulsões, dormência ou fraqueza muscular. Os autores procuraram descobrir se pequenas moléculas poderiam distinguir a NaV1.5 de suas parentes com seletividade muito maior.
Um bloqueador inspirado em plantas com precisão recorde
A equipe examinou uma família de moléculas em forma de anel chamadas metal protoporfirinas, que se assemelham aos núcleos do heme no sangue e da clorofila nas plantas, mas contêm diferentes átomos metálicos centrais. Quando aplicaram várias versões a canais humanos NaV1.5 produzidos em células cultivadas, um composto se destacou: MgPpIX. Ele reduziu a corrente elétrica através da NaV1.5 em cerca de 99% em concentrações nanomolares, aproximadamente 100 vezes mais potente do que um análogo à base de ferro (hemina). Outras versões metálicas, como as contendo níquel ou cobre, foram essencialmente inativas. Notavelmente, o MgPpIX deixou vários outros tipos de canais de sódio humanos (usados pelo cérebro, nervos periféricos e músculo esquelético) completamente intocados nas mesmas doses, tornando sua seletividade uma das mais agudas já relatadas para essa família de canais.
Como a molécula trava uma pequena alavanca de voltagem
Para entender essa precisão incomum, os pesquisadores combinaram manipulação genética com simulações computacionais. Os canais de sódio têm quatro partes repetidas, cada uma contendo um “sensor de voltagem” que muda de posição quando o potencial de membrana varia. Ao trocar aminoácidos individuais entre a NaV1.5 e suas parentes insensíveis, a equipe rastreou a ação do MgPpIX até o sensor de voltagem no segundo domínio, especialmente dois resíduos expostos ao exterior da célula. Simulações de dinâmica molecular em um ambiente de membrana realista sugeriram que o MgPpIX se acomoda junto a esse sensor quando ele está em sua posição de repouso, a “para baixo”. O centro metálico positivamente carregado do MgPpIX é atraído por uma cadeia lateral carregada negativamente no canal, enquanto o anel plano interage com os lipídios circundantes. Essa ligação parece travar o sensor de voltagem no lugar, impedindo-o de se mover para o estado ativo “para cima” e, assim, mantendo o canal fechado. Curiosamente, despolarizações fortes — como as que ocorrem durante um batimento cardíaco — podem desalojar temporariamente a molécula, um comportamento que os autores descrevem como “dependência de uso reversa”.
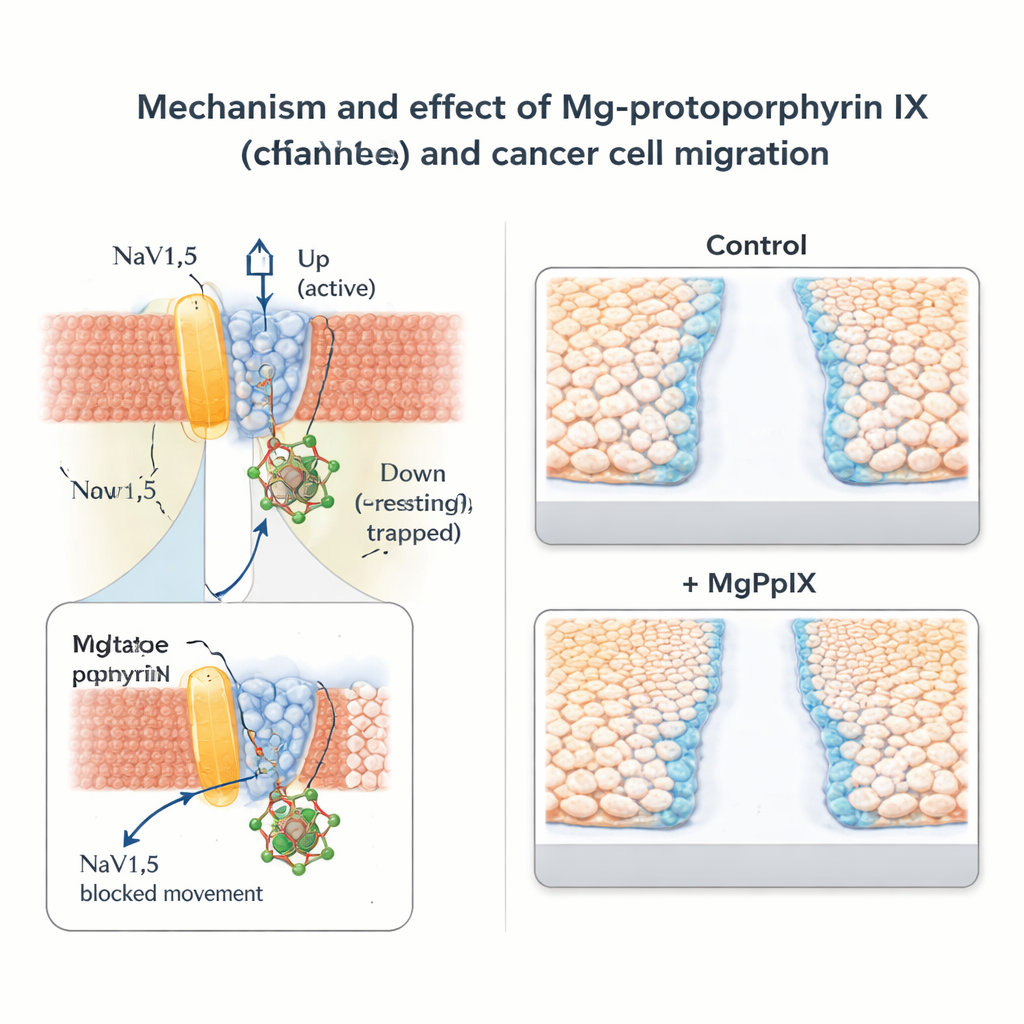
Retardando o movimento de células cancerosas sem bloqueio amplo de nervos
A equipe então explorou o que esse freio molecular significa para o comportamento do câncer. Em linhagens de câncer de mama (MDA-MB-231) e de cólon (SW-480) que expressam naturalmente NaV1.5, o MgPpIX reduziu dramaticamente as correntes de sódio e desacelerou a migração celular em ensaios padronizados de “riscar” e transwell. Quanto mais um dado metal protoporfirina bloqueava a NaV1.5, mais ele dificultava o movimento celular, fortalecendo a ligação entre a atividade do canal e a motilidade. Em contraste, linhagens de células cancerosas sem NaV1.5 não mostraram resposta ao MgPpIX nem eletricamente nem nos testes de migração, apoiando a ideia de que o efeito é altamente específico e não simplesmente tóxico. Em comparação com a toxina clássica de canais de sódio tetrodotoxina, o MgPpIX alcançou supressão mais forte da migração em concentrações muito mais baixas.
Promessa e cautela para futuros fármacos anti‑metastáticos
Para um leitor não especialista, a mensagem central é que os pesquisadores encontraram uma molécula relacionada a plantas que age como uma braçadeira de precisão em um portão elétrico do tipo cardíaco usurpado por alguns cânceres. Ao aprisionar a pequena alavanca de voltagem do portão em sua posição de repouso, o MgPpIX pode conter fortemente a mobilidade de células cancerosas em laboratório, poupando outros canais de sódio cruciais para sensação e movimento. Como a rápida atividade elétrica do coração pode aliviar parcialmente esse bloqueio, pode haver até uma janela de segurança na qual as células tumorais sejam inibidas mais do que as células cardíacas. Embora o MgPpIX em si possa não estar pronto como medicamento, seu sítio de ligação único e seu mecanismo fornecem um roteiro poderoso para projetar futuros fármacos destinados a interromper a disseminação do câncer ao alvejar a NaV1.5 com seletividade sem precedentes.
Citação: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Palavras-chave: canais de sódio, NaV1.5, migração de células cancerosas, moléculas derivadas de clorofila, fármacos direcionados para canais iônicos