Clear Sky Science · pt
MiniPromoters Ple384 (TH) e Ple388 (PITX3) para direcionamento de neurônios dopaminérgicos do mesencéfalo em camundongos e macacos
Por que esta pesquisa importa para a saúde do cérebro
As células produtoras de dopamina do cérebro nos ajudam a mover‑nos, aprender com recompensas e manter a motivação. São também as células que morrem na doença de Parkinson. Cientistas e médicos gostariam de entregar genes benéficos ou ferramentas moleculares especificamente a esses neurônios vulneráveis, tanto em animais de laboratório quanto, um dia, em pessoas. Mas fazer com que a terapia gênica seja ativada apenas nas células corretas — e não por todo o cérebro — tem sido um grande obstáculo. Este estudo descreve dois novos “interruptores” de DNA compactos que podem ativar genes de forma confiável quase exclusivamente nos neurônios dopaminérgicos do mesencéfalo de camundongos e macacos, abrindo caminho para tratamentos mais precisos e potencialmente mais seguros.
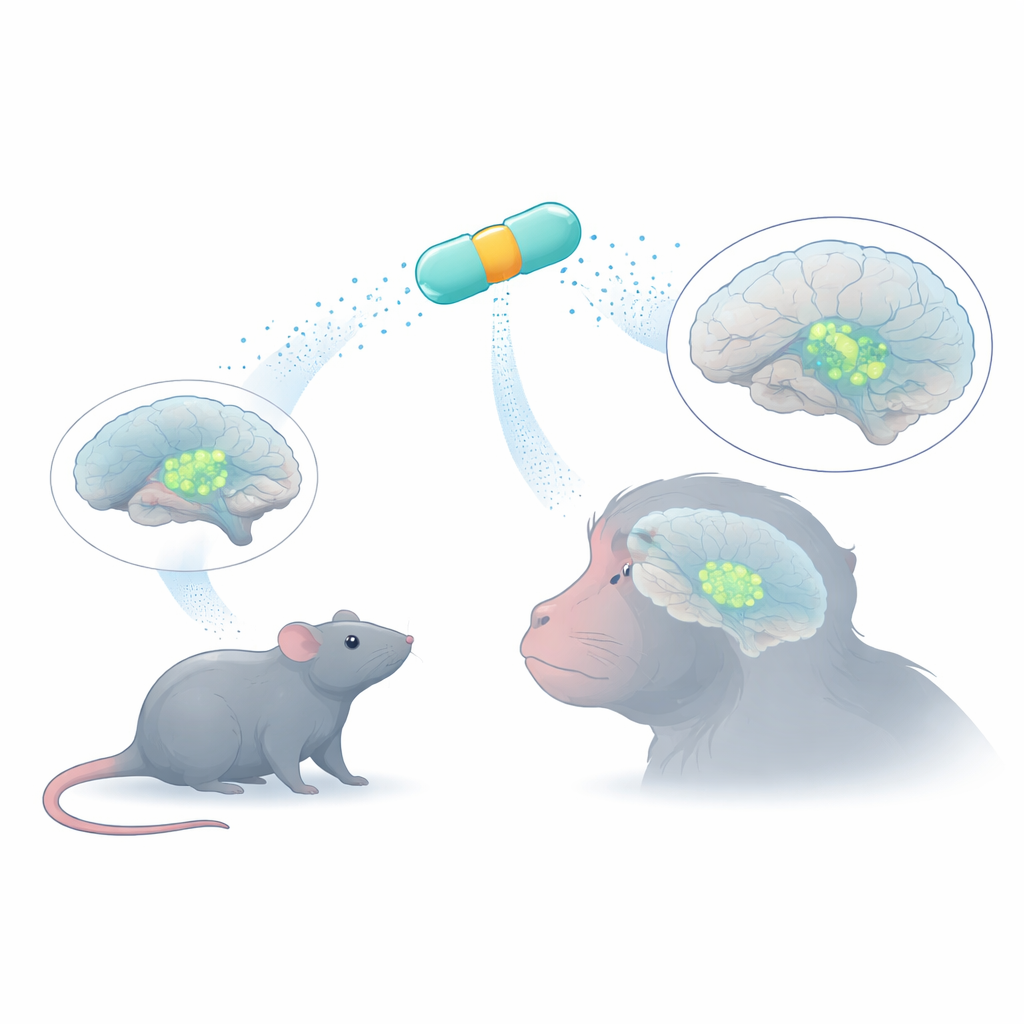
Pequenos interruptores genéticos com grande tarefa
Para levar um gene terapêutico às células do cérebro, os pesquisadores frequentemente usam vírus adeno‑associados (AAVs), vetores inofensivos capazes de transportar apenas uma quantidade limitada de DNA. Dentro de cada vírus, uma sequência promotora curta atua como um interruptor liga‑desliga, decidindo onde esse gene ficará ativo. Muitos promotores naturais são grandes demais ou pouco específicos, ativando genes em muitos tipos celulares. A equipe usou bioinformática para projetar oito “MiniPromoters” muito compactos a partir de DNA humano — combinações curtas de elementos de controle extraídos de genes conhecidos por marcar neurônios produtores de dopamina. O objetivo foi obter conjuntos de interruptores que caibam dentro de AAVs e ainda assim promovam expressão forte e focada por tipo celular.
Encontrando os alvos certos no cérebro do camundongo
Os oito MiniPromoters candidatos foram primeiro testados em camundongos. Cada promotor foi inserido em um AAV contendo uma proteína fluorescente verde, permitindo aos cientistas ver onde o interruptor estava ativo. Eles administraram os vírus tanto na corrente sanguínea quanto diretamente nos espaços preenchidos por fluido do cérebro. A maioria dos MiniPromoters não foi seletiva: alguns acenderam muitos tipos celulares não dopaminérgicos, outros mal funcionaram. Dois se destacaram. Um, chamado Ple384, foi construído a partir de regiões de controle do gene da tirosina hidroxilase, a enzima-chave usada por todos os neurônios produtores de catecolaminas. O outro, Ple388, veio do PITX3, um gene crítico para um subconjunto de neurônios dopaminérgicos do mesencéfalo. Tanto Ple384 quanto Ple388 produziram sinais intensos e bem confinados na substância negra compacta e na área tegmental ventral — os núcleos mesencefálicos de neurônios dopaminérgicos — com mais de 90% das células marcadas também apresentando a molécula característica da dopamina.
De camundongos a macacos sem perfurar profundamente o cérebro
Qualquer terapia gênica dirigida a doenças humanas deve, eventualmente, funcionar em primatas, cujos cérebros são maiores e mais complexos. Injetar diretamente na substância negra é tecnicamente exigente e pode danificar essa estrutura pequena e profunda. Em vez disso, os pesquisadores testaram se os mesmos MiniPromoters poderiam ser entregues no líquido cefalorraquidiano de macacos rhesus por meio de uma única injeção em um ventrículo lateral. Usando uma variante de cápside AAV conhecida por se espalhar amplamente a partir dos espaços fluídicos, eles observaram que tanto Ple384 quanto Ple388 promoveram expressão robusta em neurônios dopaminérgicos do mesencéfalo na substância negra e na área tegmental ventral, enquanto pouparam em grande parte outras regiões ricas em dopamina, como hipotálamo e locus coeruleus. A maioria das células marcadas na região‑alvo eram neurônios dopaminérgicos, confirmando que os interruptores mantiveram sua seletividade entre espécies.
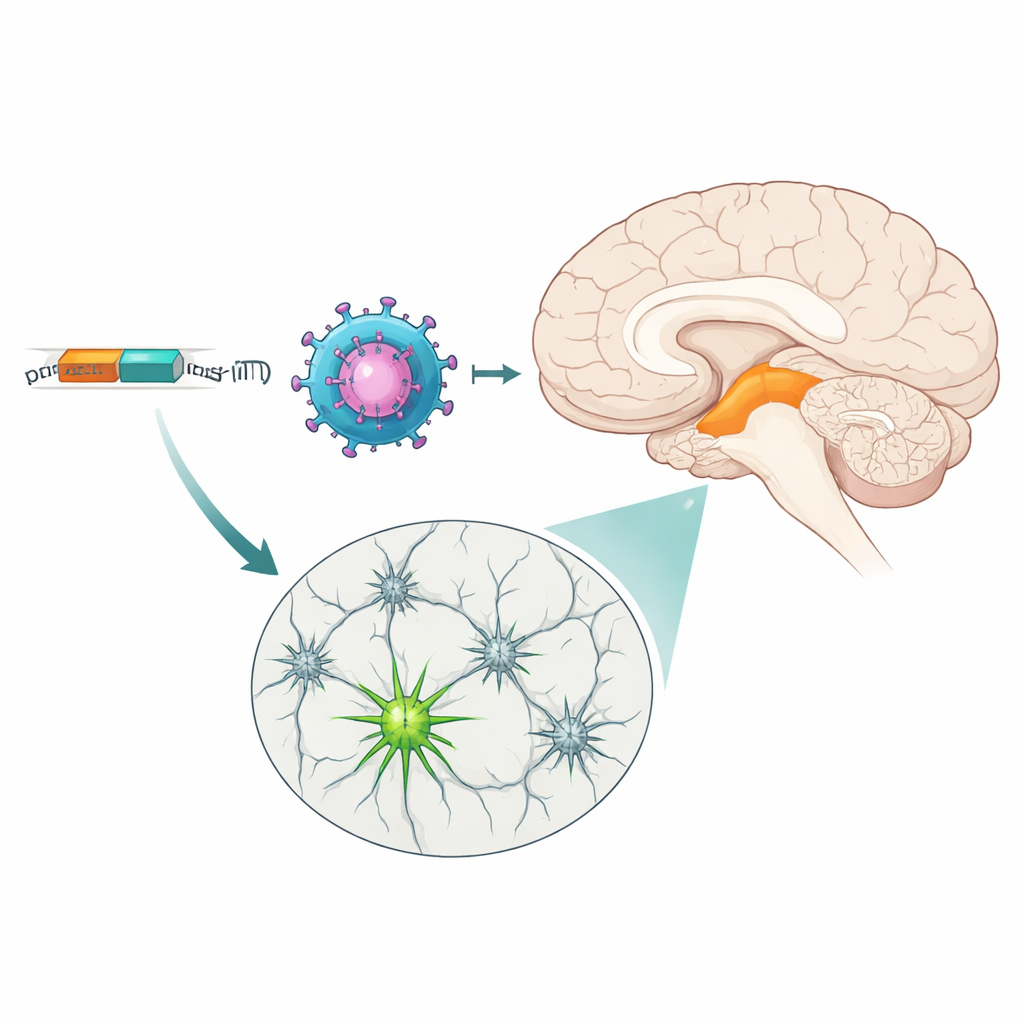
Duasherramentas com forças diferentes
Embora ambos os MiniPromoters atingissem seus alvos, fizeram‑no com padrões distintos. Ple384, baseado no mais amplo gene da tirosina hidroxilase, marcou mais neurônios no total e cobriu tanto as camadas ventral quanto dorsal da substância negra, além de uma porção maior da área tegmental ventral. Ple388, refletindo o gene PITX3 mais restrito, rotulou principalmente um subconjunto de neurônios do nível ventral e produziu fluorescência mais fraca. A expressão fora do alvo foi observada principalmente perto dos locais de injeção e em alguns órgãos periféricos após administração na corrente sanguínea, mas controles cuidadosos mostraram que os vetores virais eram capazes de alcançar muitas regiões cerebrais; foram os próprios MiniPromoters que limitaram a expressão majoritariamente aos neurônios dopaminérgicos do mesencéfalo. Essa força ajustável — um mais potente e abrangente, outro mais seletivo e moderado — permite que os pesquisadores escolham o interruptor que melhor corresponda às suas necessidades, desde modulação suave até intervenção em larga escala.
O que isso significa para terapias futuras
Para um não especialista, a mensagem principal é que os autores criaram dois interruptores genéticos compactos que funcionam como chaves de luz precisas e programáveis para neurônios de dopamina em camundongos e macacos. Ple384 oferece acesso forte e disseminado a essas células, enquanto Ple388 focaliza um subconjunto mais estreito e particularmente vulnerável. Como os interruptores são pequenos o bastante para caber confortavelmente em vetores virais comumente usados, eles deixam espaço para genes terapêuticos e podem ajudar a reduzir efeitos colaterais ao evitar regiões cerebrais indesejadas. À medida que a terapia gênica para a doença de Parkinson e condições relacionadas avança, elementos de controle direcionados como esses serão ingredientes essenciais para tratamentos poderosos e, ao mesmo tempo, precisos.
Citação: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Palavras-chave: neurônios de dopamina, terapia gênica, doença de Parkinson, vetores AAV, promotores específicos de células