Clear Sky Science · pt
Efeitos terapêuticos do IGF-2 na NMOSD ao inibir a apoptose de astrócitos por meio da modulação da via de sinalização IGF-1R/PI3K/AKT
Protegendo o cérebro em uma doença autoimune pouco conhecida
O transtorno do espectro da neuromielite óptica, ou NMOSD, é uma doença autoimune rara, mas devastadora, que ataca os nervos ópticos e a medula espinhal, frequentemente deixando os pacientes com cegueira, paralisia ou sérios problemas cognitivos. Os medicamentos atuais atuam principalmente suprimindo o sistema imunológico, são caros e não protegem diretamente as células cerebrais contra danos. Este estudo investiga se uma molécula natural relacionada ao crescimento presente no sangue, chamada IGF‑2, pode ajudar a proteger as células cerebrais de lesões na NMOSD e oferecer uma nova abordagem terapêutica para a doença.
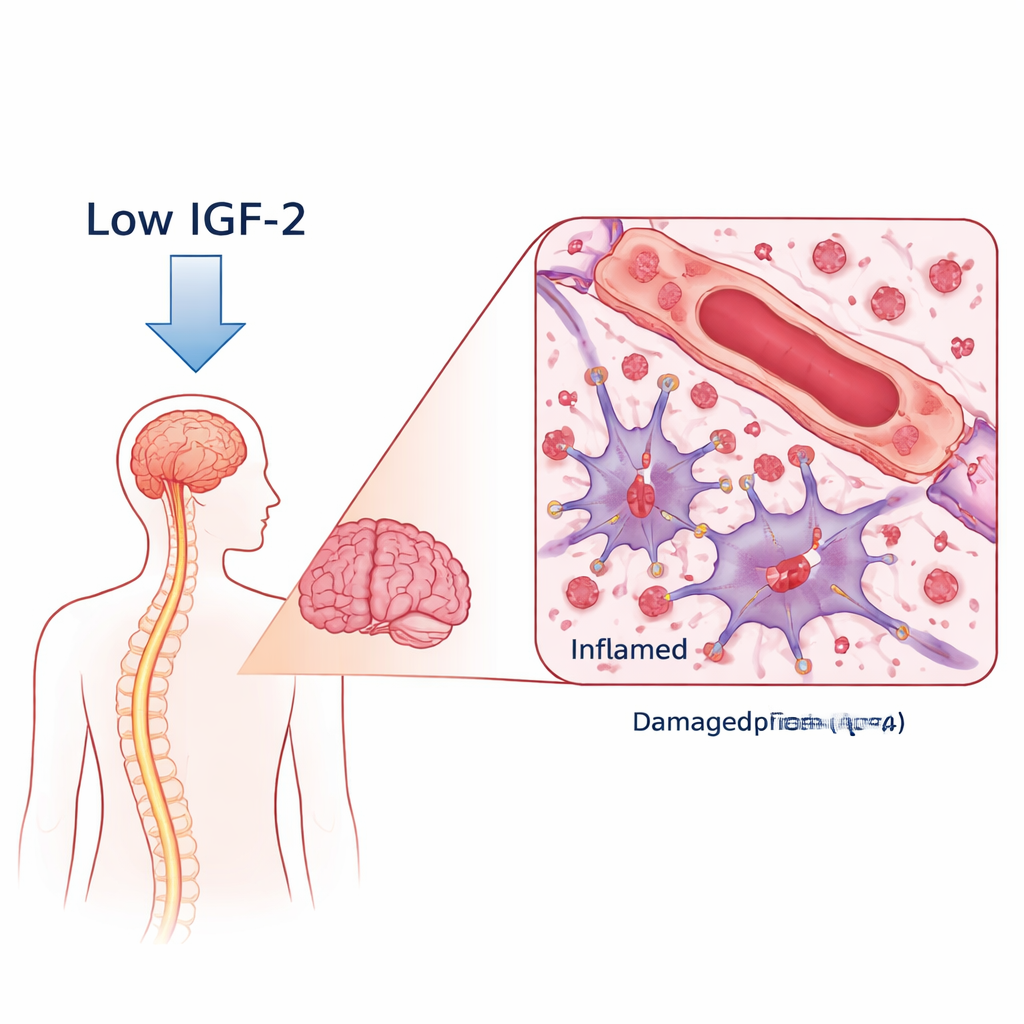
Um anticorpo prejudicial e um protetor ausente
Na NMOSD, o organismo produz anticorpos contra uma proteína canalizadora de água chamada AQP4, que se localiza em células de suporte em forma de estrela no cérebro chamadas astrócitos. Quando esses anticorpos se ligam, eles desencadeiam ataques imunes que danificam os astrócitos, removem a mielina (o revestimento isolante dos nervos) e podem prejudicar os neurônios. Os pesquisadores compararam o sangue de mulheres com NMOSD positivo para anticorpo anti‑AQP4 com o de voluntárias saudáveis. Usando um levantamento proteico amplo, encontraram níveis de IGF‑2 marcadamente mais baixos em pacientes com NMOSD, enquanto duas proteínas de ligação ao IGF que podem aprisionar o IGF‑2 estavam aumentadas. Importante, pacientes com os níveis mais baixos de IGF‑2 tendiam a ter maior incapacidade e piores resultados em testes de pensamento e memória, ligando essa molécula à gravidade da doença e à saúde cognitiva.
Tratamento padrão ajuda o IGF-2 a se recuperar
Muitos pacientes com NMOSD recebem rituximabe, um fármaco que elimina células B produtoras de anticorpos. A equipe mediu proteínas no sangue antes e depois do tratamento com rituximabe. Após a terapia, os níveis de IGF‑2 aumentaram e as proteínas de ligação diminuíram, aproximando‑se do padrão observado em pessoas saudáveis. Isso sugere que domar o sistema imune pode permitir ao corpo restaurar alguns de seus próprios fatores protetores. Embora o rituximabe não seja projetado para agir diretamente sobre o IGF‑2, a mudança nesta molécula indica que ela pode fazer parte da resposta de recuperação do organismo, e que monitorar o IGF‑2 poderia ajudar a acompanhar a evolução dos pacientes ao longo do tempo.
Testando o IGF-2 em uma versão murina da doença
Para verificar se o IGF‑2 pode fazer mais do que sinalizar a gravidade da doença, os cientistas recorreram a um modelo murino. Injetaram anticorpos humanos anti‑AQP4 e complemento humano nos cérebros de camundongos, o que reproduziu características-chave da NMOSD: perda de AQP4 nos astrócitos, inflamação, dano à mielina e fraqueza dos membros. Outro grupo de camundongos recebeu previamente um vírus inofensivo que fez com que suas células cerebrais produzissem IGF‑2 extra. Esses camundongos com aumento de IGF‑2 perderam menos peso, apresentaram problemas motores mais leves e mostraram menor perda de mielina e inflamação no tecido cerebral e na medula espinhal. O tratamento padrão com rituximabe também ajudou, mas a superexpressão de IGF‑2 pareceu proteger o tecido cerebral de forma mais direta, sugerindo um papel neuroprotetor além da ação apenas imunossupressora.
Como o IGF-2 acalma a morte celular e a inflamação
A equipe então examinou astrócitos em placas de cultura expostos a anticorpos de NMOSD. Normalmente, esses anticorpos reduziram os níveis de um receptor chave chamado IGF‑1R e suprimiram uma via protetora downstream conhecida como PI3K/AKT, ao mesmo tempo em que ativavam proteínas de “autodestruição” e sinais inflamatórios. Quando os pesquisadores forçaram os astrócitos a produzir mais IGF‑2, essa via protetora voltou a ser ativada, os marcadores de morte celular diminuíram, e as células liberaram menos moléculas inflamatórias como IL‑1β, IL‑6 e TNF‑α. Bloquear o receptor IGF‑1R apagou em parte esses benefícios, mostrando que o IGF‑2 atua principalmente ativando a cadeia IGF‑1R/PI3K/AKT dentro dos astrócitos. Em camundongos vivos, o aumento de IGF‑2 também reduziu a ativação das microglias, os sentinelas imunológicos do cérebro, e diminuiu sinais inflamatórios na corrente sanguínea.
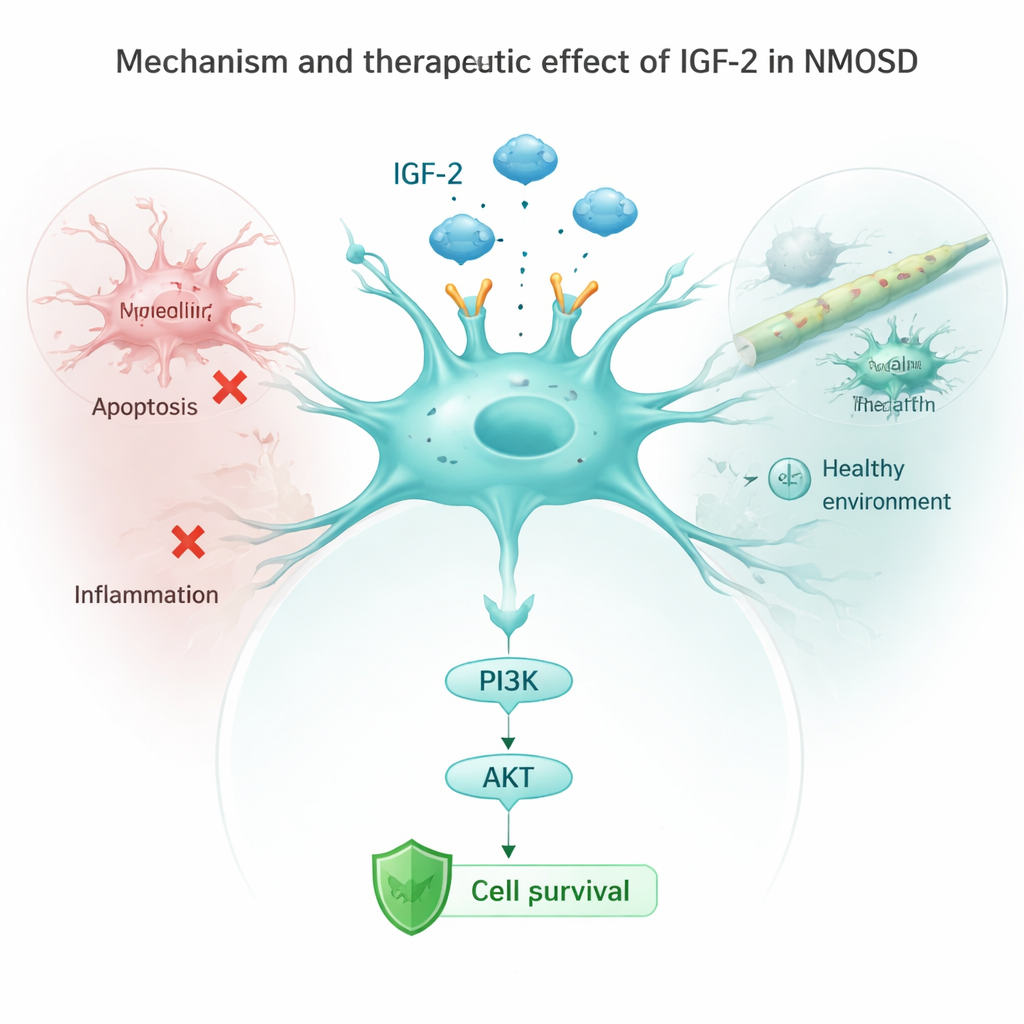
O que isso pode significar para os pacientes
Em conjunto, esses achados sugerem que baixos níveis de IGF‑2 são tanto um sinal de alerta quanto uma oportunidade perdida na NMOSD. Pacientes com menos IGF‑2 tendem a estar mais incapacitados e com função cognitiva reduzida, enquanto restaurar ou aumentar o IGF‑2 em modelos experimentais ajuda os astrócitos a sobreviver, reduz a inflamação cerebral e atenua o dano neural. Embora este trabalho seja inicial e baseado em um número pequeno de pacientes e em estudos animais, ele aponta o IGF‑2 como um alvo promissor para tratamentos futuros que não apenas reduziríam o ataque imune, mas também protegeriam diretamente as células cerebrais vulneráveis.
Citação: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Palavras-chave: neuromielite óptica, astrócitos, IGF-2, neuroinflamação, neuroproteção