Clear Sky Science · pt
Análise da função cardíaca sistólica em camundongos com nocaute de PERM1 usando grandes coortes de animais
Por que corações minúsculos de camundongo importam para a saúde humana
A insuficiência cardíaca costuma ser descrita como uma bomba cansada, mas o que realmente enfraquece um coração é surpreendentemente complexo. Neste estudo, cientistas usaram um grupo incomumente grande de camundongos para fazer uma pergunta focada: desligar um único gene chamado PERM1, conhecido por ajudar as células cardíacas a produzir energia, também altera a força com que o coração se contrai? Ao escanear cuidadosamente os corações de mais de 170 camundongos, eles mostram que esse gene remodela sutilmente o coração e reduz sua força de ejeção, ao mesmo tempo em que os animais, em grande parte, permanecem externamente saudáveis. As descobertas ajudam a resolver um debate na área e oferecem um roteiro para projetar melhores experimentos cardíacos no futuro.
Um gene que conecta uso de combustível à força de ejeção
PERM1 foi identificado inicialmente como um interruptor que aumenta a produção de energia em células musculares, incluindo as do coração. Trabalhos anteriores mostraram que os níveis de PERM1 caem em corações em falha tanto em camundongos quanto em humanos, levantando a possibilidade de que PERM1 baixo possa realmente contribuir para batimentos cardíacos mais fracos. Mas estudos usando camundongos com nocaute de PERM1 — animais geneticamente modificados para não ter o gene — produziram respostas conflitantes sobre se seus corações realmente bombeiam com menos eficácia. Como o PERM1 é visto como um possível alvo para novas terapias contra insuficiência cardíaca, os autores propuseram testar seu impacto na função cardíaca com número suficiente de animais e estatística rigorosa para fornecer uma resposta clara de sim ou não.
Um olhar em grande escala sobre corações pequenos
A equipe reuniu dados de ecocardiograma — a mesma técnica de ultrassom usada em clínicas de cardiologia — de todo camundongo com nocaute de PERM1 e de seu irmao saudável usado no laboratório ao longo de um período de 18 meses. Essa varredura retrospectiva produziu 84 animais normais (tipo selvagem) e 88 nocaute, um tamanho amostral muito maior do que o típico em estudos cardíacos com camundongos. A partir das imagens de ultrassom, eles mediram indicadores padrão de quão bem o ventrículo esquerdo, a principal câmara de bombeamento, funciona. O número-chave foi a fração de ejeção, a porcentagem de sangue expelida a cada batimento, junto com medidas relacionadas, como quanto o diâmetro do ventrículo se reduz quando contrai, quão espessas são as paredes e a quantidade total de sangue bombeada por minuto.
Ejeção mais fraca, câmara maior, débito similar
Os resultados mostram um padrão consistente. Em média, a fração de ejeção caiu de cerca de 65% nos camundongos normais para 54% nos nocaute de PERM1, uma diferença grande o suficiente para ter relevância clínica em pacientes humanos e respaldada por estatísticas extremamente robustas. Outras medidas de contração, como encurtamento fracional e espessamento das paredes, também declinaram. Ao mesmo tempo, os ventrículos esquerdos dos nocaute eram visivelmente maiores, especialmente no final da contração, indicando que mais sangue ficou retido na câmara. Apesar dessa contração mais fraca, a quantidade total de sangue bombeada por minuto caiu apenas ligeiramente — cerca de 6% — porque as câmaras aumentadas podiam conter mais sangue inicialmente. Em outras palavras, o coração compensou parcialmente a contração ruim pela dilatação de sua câmara principal.
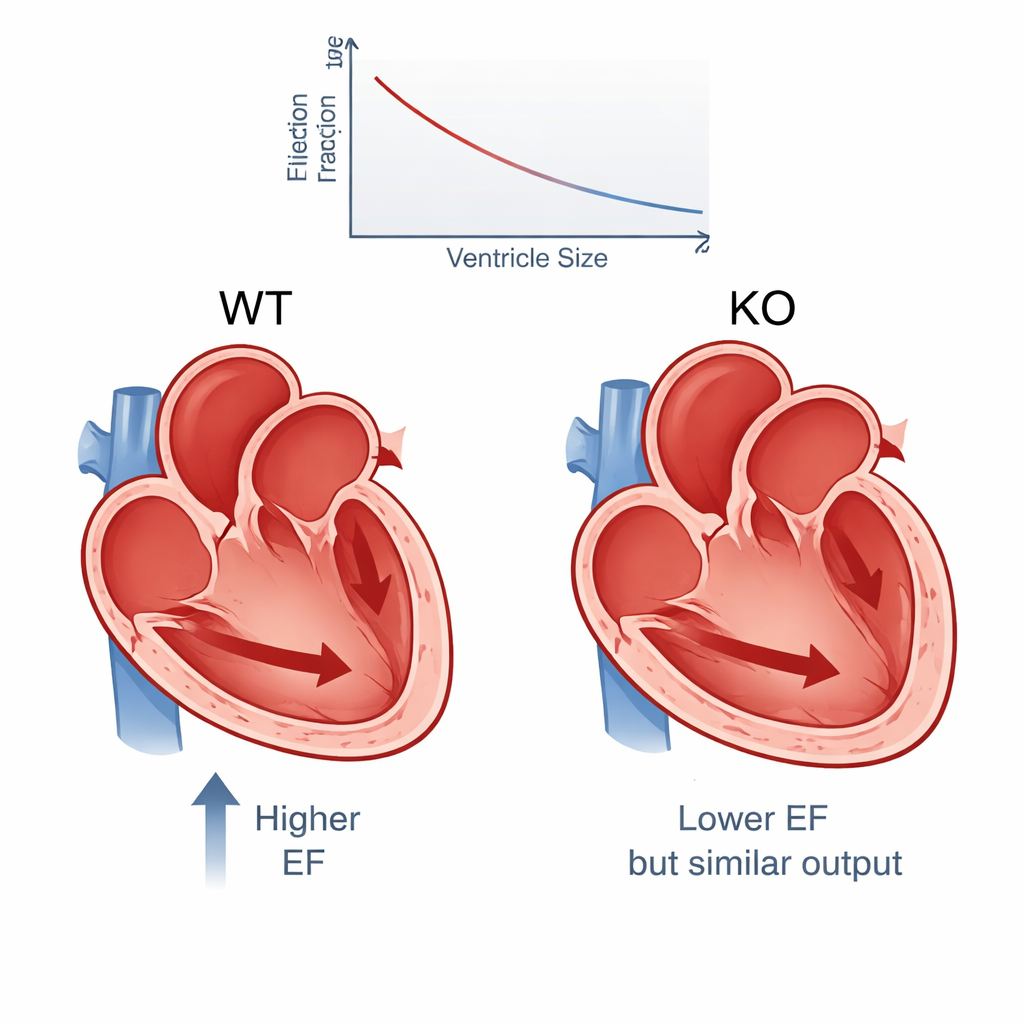
Diversidade oculta em corações “idênticos”
Como o estudo incluiu tantos animais, os pesquisadores puderam olhar além das médias e estudar como corações individuais variavam. Mesmo entre camundongos saudáveis e geneticamente idênticos, eles observaram uma dispersão surpreendentemente ampla na fração de ejeção. O nocaute de PERM1 deslocou toda a distribuição para baixo — mais corações com menor força de bombeamento —, mas não aumentou a largura dessa dispersão. Cerca de 7% dos camundongos nocaute tinham frações de ejeção abaixo de 40%, um nível que qualifica como insuficiência cardíaca com fração de ejeção reduzida em pessoas, no entanto esses camundongos ainda mantinham um débito sanguíneo quase normal. Análises estatísticas mostraram que sexo, idade e peso corporal explicavam apenas uma pequena porção da variabilidade; a maioria das diferenças provavelmente decorre de fatores biológicos mais difíceis de medir, como influências ambientais sutis ou alterações epigenéticas.
O que isso significa para pesquisas cardíacas futuras
Para ajudar outros cientistas a projetar melhores experimentos, os autores usaram seu grande conjunto de dados para calcular quantos animais são tipicamente necessários para detectar mudanças significativas em cada parâmetro cardíaco. Eles descobriram que os tamanhos de grupo modestos frequentemente usados na área podem facilmente deixar passar efeitos reais, mas moderados, especialmente para medidas sutis como volume sistólico ou débito cardíaco. No geral, o estudo apresenta um forte argumento de que a perda de PERM1 causa um remodelamento específico do coração — câmaras maiores, contração mais fraca — em vez de falha completa, e que esse remodelamento é parcialmente equilibrado por mudanças estruturais que ajudam a preservar o fluxo sanguíneo. Para não especialistas, a conclusão é que um único gene regulador de energia pode empurrar o coração para um novo modo de funcionamento, que parece saudável por fora, mas carrega mudanças mais silenciosas na construção da bomba e na sua força de trabalho.
Citação: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Palavras-chave: insuficiência cardíaca, contratilidade cardíaca, energetia mitocondrial, modelos de camundongo, ecocardiografia