Clear Sky Science · pt
Modelos generalizados de vasos sanguíneos para oncologia baseada em nanopartículas magnéticas: propriedades geométricas e microfluídicas
Guiando pequenos ímãs pelo corpo
Imagine poder atrair medicamentos contra o câncer diretamente para um tumor usando um ímã, poupando o resto do corpo dos efeitos colaterais mais severos. Este estudo explora como pequenas partículas magnéticas se deslocam por redes semelhantes a vasos sanguíneos e faz uma pergunta aparentemente simples: em condições de fluxo realistas, ímãs podem realmente direcionar essas partículas para onde os médicos desejam?
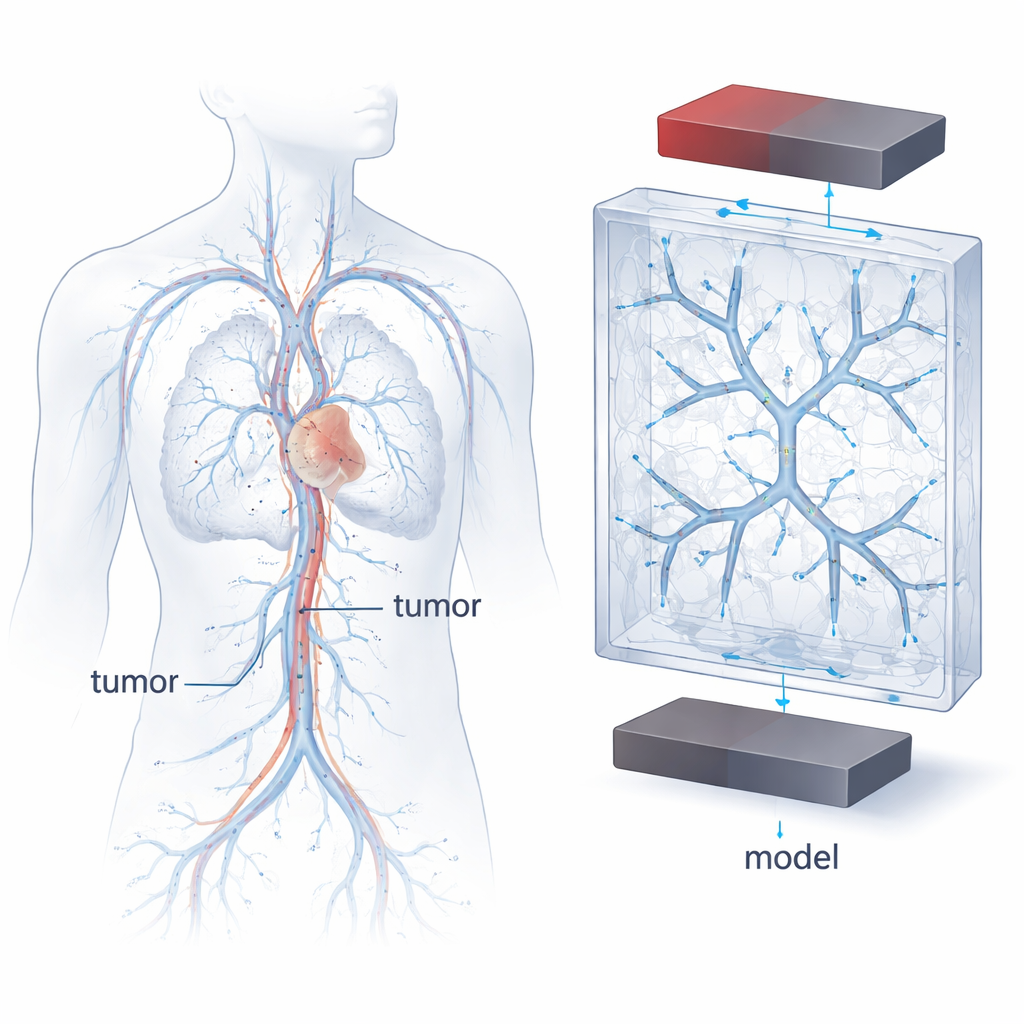
Por que a geometria dos vasos e o fluxo importam
Terapias magnéticas contra o câncer dependem de nanopartículas de óxido de ferro superparamagnéticas — SPIONs — que podem ser atraídas por um campo magnético enquanto transportam fármacos pela corrente sanguínea. Mas os vasos sanguíneos não são tubos retos e simples: ramificam-se, estreitam-se, curvam-se e se dividem, e o sangue acelera ou desacelera em resposta. Essas mudanças de forma e velocidade afetam como as partículas se movem, onde se concentram e se têm tempo suficiente para tocar as paredes dos vasos e aderir. Os vasos sanguíneos reais dos pacientes são extremamente variáveis, o que dificulta comparar experimentos ou prever o comportamento de uma nova terapia. Os autores, portanto, propuseram construir uma “vasculatura modelo” altamente controlada e reprodutível que ainda capture as características essenciais dos vasos que alimentam tumores.
Construindo redes ideais de vasos tumorais
Para projetar esses vasos modelo, a equipe recorreu a regras clássicas que descrevem como artérias reais se ramificam. Uma dessas regras, a lei de Murray, relaciona os diâmetros dos vasos pai e das ramificações filhas em uma rede energeticamente eficiente. Usando medidas clínicas de tumores de mama e essas leis de escala, os pesquisadores geraram matematicamente árvores ramificadas que imitam como os vasos que alimentam tumores diminuem até a rede capilar. Em seguida, usaram impressão 3D de alta resolução para embutir redes de canais ocos com dois, três ou quatro níveis de ramificação dentro de blocos plásticos transparentes. Os canais seguiram um padrão de ramificação simétrico e se estenderam em três dimensões, oferecendo um cenário simplificado, porém fisiologicamente inspirado, para estudar o movimento das partículas.
Observando partículas magnéticas em ação
Através dessas redes impressas, a equipe bombeou água como substituto do sangue, injetou então um fluido contendo SPIONs a montante e aplicou um campo magnético estático ao redor do modelo. Imagens de alta velocidade forneceram um registro em filme de como as nuvens escuras de partículas passaram por diferentes ramos, enquanto a análise computacional converteu mudanças de brilho em sinais temporais que refletem a presença local de partículas. Variando a vazão de fundo, a concentração de partículas, a complexidade das ramificações e a presença ou ausência do ímã, os pesquisadores puderam separar como cada fator moldou a distribuição de partículas, o tempo de residência e a deposição final nas paredes dos canais.
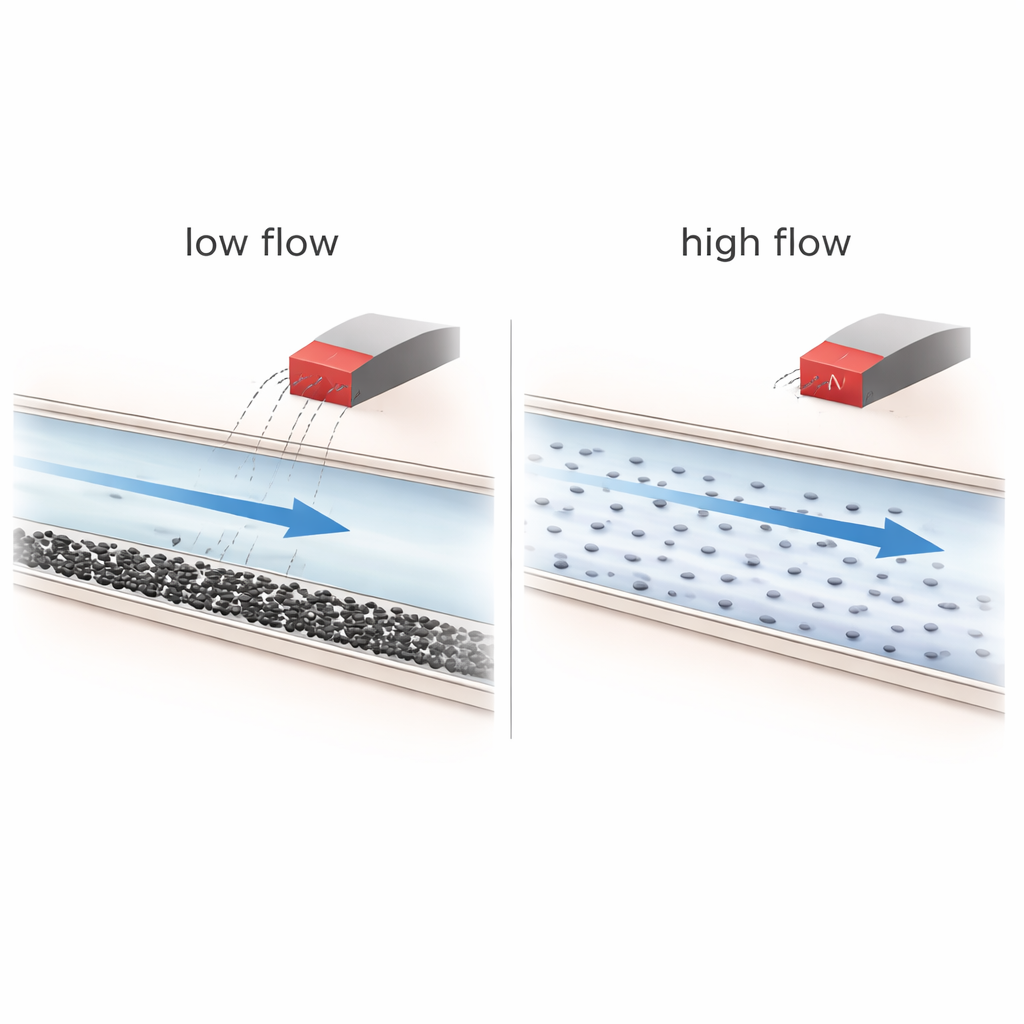
Quando os ímãs ajudam — e quando não ajudam
Os experimentos revelam que as condições de fluxo dominam a história. Em taxas de fluxo mais altas, o fluido se mistura bem e as nanopartículas viajam rapidamente; nessas condições, o campo magnético tem quase nenhuma influência, e as partículas simplesmente seguem as linhas de corrente pela rede. Em taxas de fluxo baixas, contudo, a gravidade e efeitos de concentração fazem com que as partículas se depositem na parte inferior dos canais, formando camadas estratificadas e, às vezes, aglomerados frouxos. Nesta situação já desigual, o ímã pode empurrar mais partículas para certos ramos e prolongar ligeiramente seu tempo de residência, particularmente em redes mais complexas e altamente ramificadas. Ainda assim, cálculos mostram que a força magnética sobre uma única partícula de 40 nanômetros é muitas ordens de magnitude mais fraca que o arrasto viscoso do líquido em fluxo, tornando o verdadeiro “controle de partícula isolada” fisicamente irrealista nas condições testadas.
O que isso significa para futuras terapias contra o câncer
Para um não-especialista, a principal conclusão é que ímãs isoladamente não podem, de forma confiável, retirar nanopartículas livres de uma corrente sanguínea em rápido movimento. Em vez disso, efeitos magnéticos perceptíveis surgem apenas quando as partículas já reduziram a velocidade, assentaram ou se agregaram — situações que efetivamente amplificam sua resposta magnética. Os modelos de vasos generalizados e impressos em 3D apresentados aqui fornecem uma maneira padronizada de explorar esses efeitos em diferentes geometrias de rede e regimes de fluxo. Para o futuro do direcionamento magnético de fármacos, este trabalho sugere que estratégias bem-sucedidas provavelmente precisarão explorar comportamentos coletivos — como agregação controlada ou sistemas transportadores — em vez de confiar no direcionamento de nanopartículas isoladas por grandes vasos rapidamente perfundidos.
Citação: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Palavras-chave: direcionamento magnético de fármacos, nanopartículas, vasculatura tumoral, modelos microfluídicos, administração de fármacos