Clear Sky Science · pt
Mirando o eixo Akt–EphA2 e a adesão célula–célula aumenta a sensibilidade à anóikis em células cancerosas
Por que as células cancerosas livres importam
Quando células cancerosas se desprendem de um tumor e viajam pela corrente sanguínea, normalmente deveriam morrer porque perdem sua aderência ao tecido ao redor. Esse programa de segurança embutido, chamado morte celular induzida por desprendimento, ajuda a impedir que tecidos saudáveis cresçam onde não deveriam. Células cancerosas metastáticas, porém, frequentemente aprendem a ignorar esse sinal e permanecem vivas enquanto flutuam, facilitando que semeiem novos tumores. Este estudo faz uma pergunta aparentemente simples: se restaurarmos um importante “sentido do toque” mecânico em células agressivas de câncer de mama, podemos forçar essas células errantes a morrer e, se não, quais artifícios de reserva elas usam para sobreviver?
Reacendendo um sentido do toque perdido
As células testam constantemente quão rígido é o ambiente, puxando as estruturas que as ancoram. Em tecido saudável, perder o contato ou pousar em uma superfície muito macia tende a disparar a autodestruição. A proteína Tropomyosin 2.1 (Tpm2.1) é uma parte importante dessa maquinaria de tensão interna e frequentemente está ausente ou reduzida em células cancerosas. Os pesquisadores usaram uma linhagem de células de câncer de mama metastático amplamente estudada e a modificaram para produzir mais Tpm2.1, restaurando grande parte desse sensoriamento de rigidez. Quando essas células modificadas foram forçadas a crescer em placas especiais antiaderentes que as impediam de se fixar, elas de fato apresentaram mais morte celular, cresceram mais lentamente e se moveram menos do que as células cancerosas não modificadas. Ainda assim, mesmo após vários dias em suspensão, cerca de 70% das células que expressavam Tpm2.1 ainda estavam vivas, sugerindo que reviver o sentido do toque por si só não resolve completamente o problema.
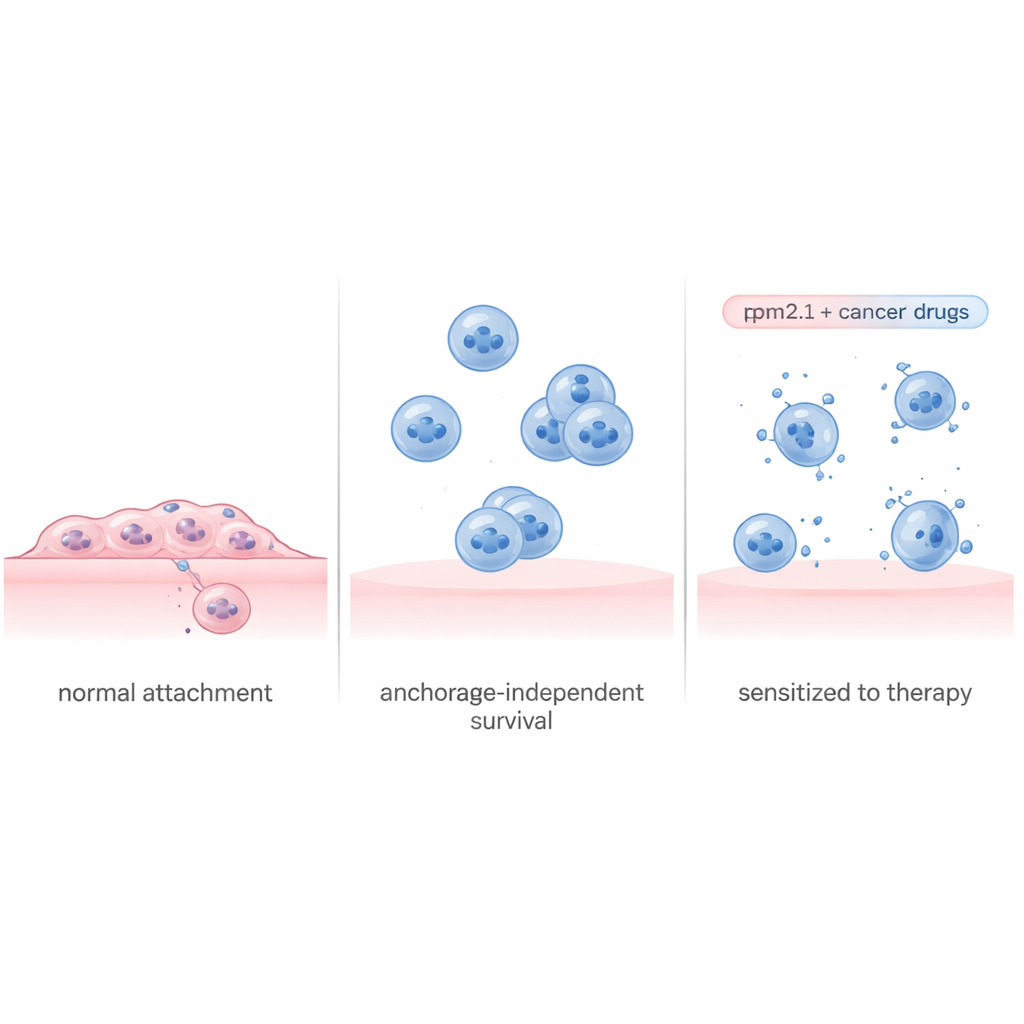
Lendo o manual de sobrevivência das células cancerosas
Para entender por que algumas células morriam enquanto outras sobreviviam, a equipe separou as células em suspensão que expressavam Tpm2.1 em dois grupos: aquelas que mostravam sinais iniciais de morte celular e as que pareciam saudáveis. Em seguida, mediram quais genes estavam ativados ou desativados em cada grupo ao longo de quatro dias. As células em processo de morte exibiram um amplo desligamento de programas envolvidos na divisão celular, reparo de DNA e adesão, juntamente com sinais de estresse que pareciam um caminho sem volta para a autodestruição. Em contraste, as células sobreviventes ativaram um plano de sobrevivência coordenado. Logo após o desprendimento, elas ligaram vias inflamatórias e relacionadas ao sistema imune e, mais tarde, aumentaram grandes circuitos de crescimento e sobrevivência, incluindo uma conhecida via centrada na proteína Akt. Ao mesmo tempo, reforçaram fortemente genes que ajudam as células a aderir umas às outras, permitindo que formem aglomerados protetores mesmo sem se fixarem na matriz circundante.
Força no número: como aglomerados celulares resistem à morte
Porque os dados de expressão gênica apontaram para um aumento da adesão célula–célula, os pesquisadores testaram se o simples ajuntamento poderia ajudar as células a sobreviver em suspensão. Quando as células que expressavam Tpm2.1 foram cultivadas em alta densidade, onde o agrupamento era fácil, muito menos células morreram do que quando foram mantidas esparsas. Uma molécula de adesão, ICAM1, destacou‑se como especialmente elevada nas células sobreviventes e já é conhecida por ajudar aglomerados de células tumorais circulantes a se formarem e se alojarem em tecidos distantes. Bloquear ICAM1 com um inibidor de pequena molécula fez com que mais células que expressavam Tpm2.1 morressem em suspensão, enquanto teve pouco efeito em culturas normais aderidas. Essas descobertas sustentam a ideia de que, uma vez que sua mecânica interna está parcialmente restaurada, as células cancerosas ainda podem escapar da morte segurando‑se literalmente umas às outras em vez de ao ambiente.
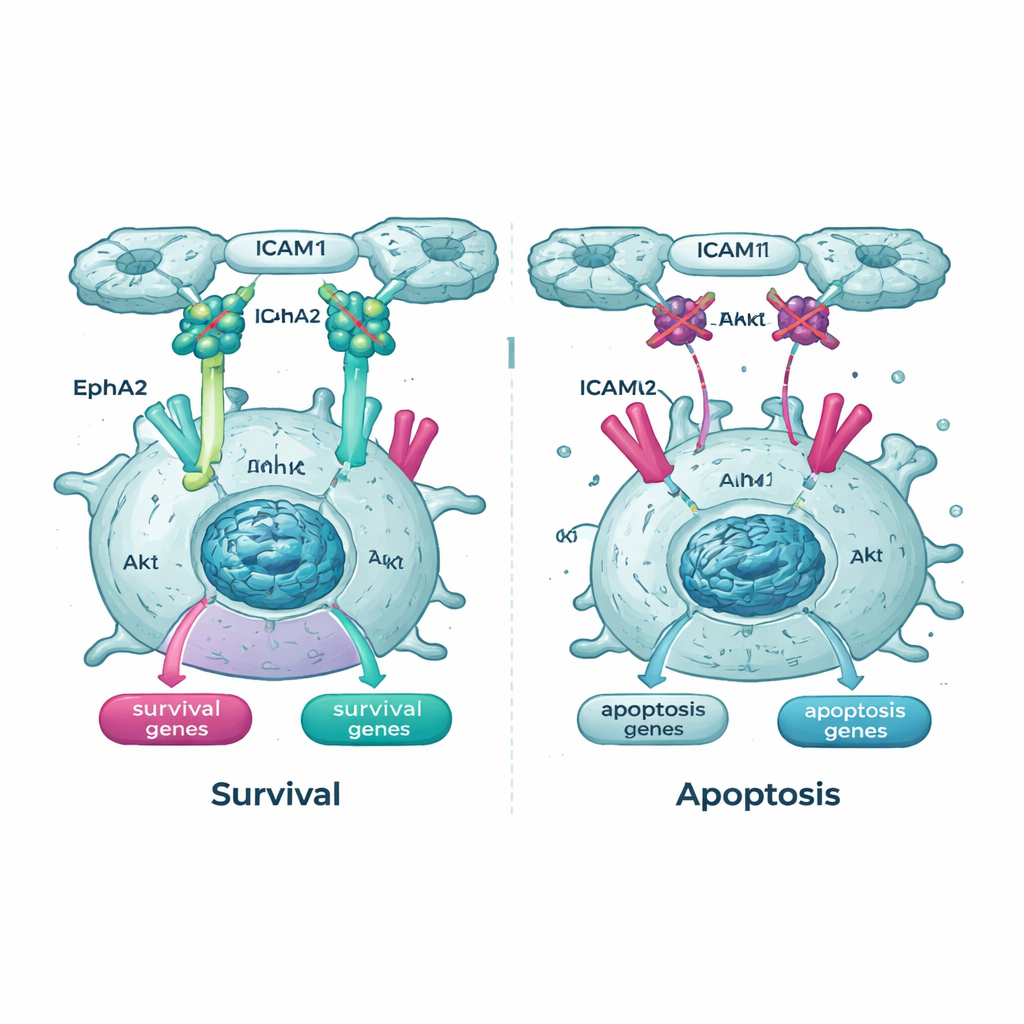
Cortando linhas de vida internas chave
As análises genéticas também destacaram a via Akt e um de seus parceiros, um receptor chamado EphA2, como linhas de vida importantes para células cancerosas em suspensão. Nas células que expressavam Tpm2.1, a forma ativa, fosforilada, de Akt estava mais baixa em suspensão do que nas células controle, e os níveis e a atividade de EphA2 também foram reduzidos. Quando a equipe tratou as células com fármacos que bloqueiam Akt ou EphA2, tanto as células cancerosas normais quanto as que expressavam Tpm2.1 tornaram‑se muito mais propensas a morrer em suspensão. Notavelmente, as células com sensoriamento de rigidez restaurado foram especialmente sensíveis a esses fármacos ao longo do tempo, o que sugere que, uma vez que suas checagens mecânicas de segurança estão parcialmente reativadas, elas dependem mais fortemente dos sinais de sobrevivência remanescentes.
Transformando um estado prontificado em uma fraqueza letal
Para um não especialista, a mensagem principal é que consertar um interruptor de segurança quebrado nas células cancerosas — sua capacidade de sentir e responder à perda de contato — é necessário, mas não suficiente para levá‑las à autodestruição. As células que sobrevivem o fazem unindo‑se e redirecionando sua fiação interna por vias alternativas de crescimento e sobrevivência. Este trabalho mostra que restaurar o sensoriamento de rigidez com Tpm2.1 coloca células de câncer de mama metastático em um estado “prontificado”, no qual estão mais próximas da morte, mas ainda não comprometidas. Ao então bloquear a via Akt–EphA2 e perturbar a adesão célula–célula via ICAM1, os pesquisadores podem empurrar essas células prontificadas além do limite e aumentar muito a morte celular induzida por desprendimento. Em termos práticos, o estudo delineia uma estratégia para futuras terapias combinadas destinadas a eliminar células tumorais em suspensão antes que possam semear novas metástases.
Citação: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Palavras-chave: metástase do câncer de mama, adesão celular, anóikis, sinalização Akt, sensoriamento de rigidez