Clear Sky Science · pt
Análise integrada de reguladores globais e genes de efluxo associados à reversão da resistência antimicrobiana em Klebsiella pneumoniae multirresistente
Por que esses germes hospitalares são tão difíceis de eliminar
Em hospitais ao redor do mundo, determinadas cepas da bactéria Klebsiella pneumoniae tornaram‑se notoriamente difíceis de tratar. Elas resistem a múltiplos antibióticos que antes funcionavam de forma confiável, transformando infecções rotineiras em emergências potencialmente fatais. Este estudo examina o interior microbiano para entender um truque importante que essas bactérias usam: bombas microscópicas que expulsam os antibióticos de volta para fora da célula, e os interruptores genéticos que parecem aumentar ou reduzir a atividade dessas bombas.
Superbactérias e suas rotas moleculares de escape
Klebsiella pneumoniae multirresistente agora é encontrada em muitos hospitais, inclusive no centro médico iraquiano onde esta pesquisa foi realizada. Essas bactérias podem sobreviver a várias famílias importantes de antibióticos ao mesmo tempo, como fluoroquinolonas, aminoglicosídeos e cefalosporinas de terceira geração. Uma maneira de fazer isso é instalando poderosas “bombas de efluxo” em seu envelope celular. Entre as mais importantes está um sistema chamado AcrAB‑TolC, que atravessa as membranas bacterianas e funciona como uma pequena bomba de porão, capturando moléculas de antibiótico dentro da célula e empurrando‑as de volta para fora antes que os medicamentos possam causar dano sério. Quando essas bombas estão altamente ativas, a concentração do antibiótico dentro da bactéria jamais sobe o suficiente para ser letal.
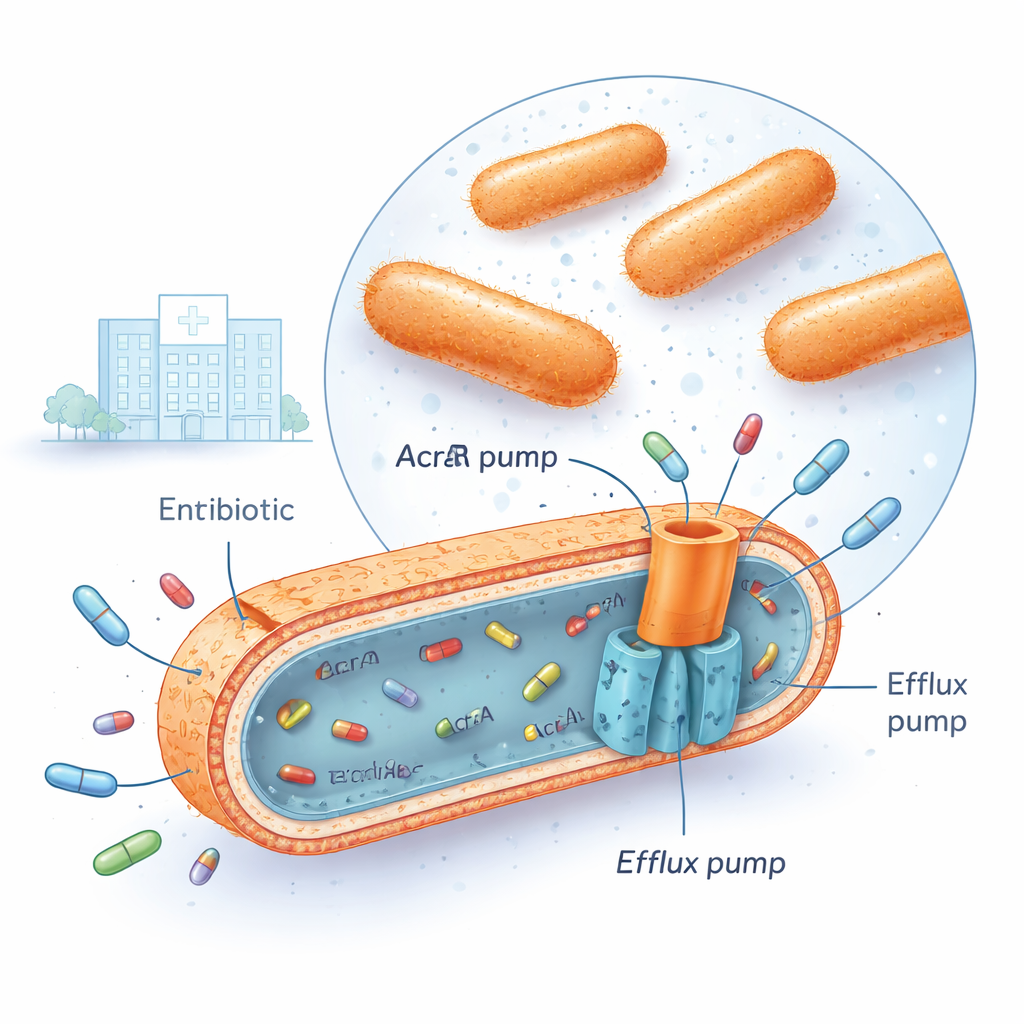
Interruptores genéticos que acompanham a aceleração das bombas
Os pesquisadores coletaram 30 isolados clínicos multirresistentes de Klebsiella pneumoniae e os compararam com 10 isolados sensíveis a antibióticos e uma estirpe de referência padrão. Usando uma técnica chamada PCR quantitativa em tempo real, mediram quanto certos genes estavam ativados. Eles se concentraram em três “reguladores globais” — genes chamados marA, soxS e rob — juntamente com as três partes da bomba AcrAB‑TolC (acrA, acrB e tolC). Nas cepas resistentes, dois reguladores, marA e soxS, normalmente estavam aumentados cerca de quatro a cinco vezes em comparação com as bactérias sensíveis, enquanto acrB, um componente central da bomba, estava elevado em quase oito vezes. Análises estatísticas mostraram que quando os níveis de marA e soxS eram altos, os níveis de acrB geralmente também eram altos, e essas cepas tendiam a suportar doses muito mais elevadas de fluoroquinolonas como ciprofloxacino. Um terceiro regulador, rob, mudou pouco e não se correlacionou com a atividade da bomba, sugerindo que ele desempenha um papel menor nas condições testadas.
Desligando as bombas para enfraquecer a resistência
Encontrar genes de bomba e regulador ativos em conjunto é sugestivo, mas não é suficiente para provar que eles realmente dirigem a resistência. Para testar se as bombas eram funcionalmente importantes, a equipe recorreu a uma ferramenta química chamada PAβN. Este composto não é usado como medicamento em pacientes, mas no laboratório pode bloquear bombas do tipo AcrAB‑TolC e impedi‑las de expulsar antibióticos. Os cientistas escolheram dez isolados resistentes que apresentavam níveis especialmente altos do gene acrB e mediram quanta ciprofloxacino era necessária para interromper seu crescimento, com e sem PAβN. Em oito dessas dez cepas, bloquear a bomba reduziu a dose necessária de ciprofloxacino em pelo menos quatro vezes, e às vezes em até dezesseis vezes. Essa queda demonstra que, em muitas dessas superbactérias, bombas de efluxo ativas são de fato uma razão importante pela qual elas toleram doses altas de antibiótico.
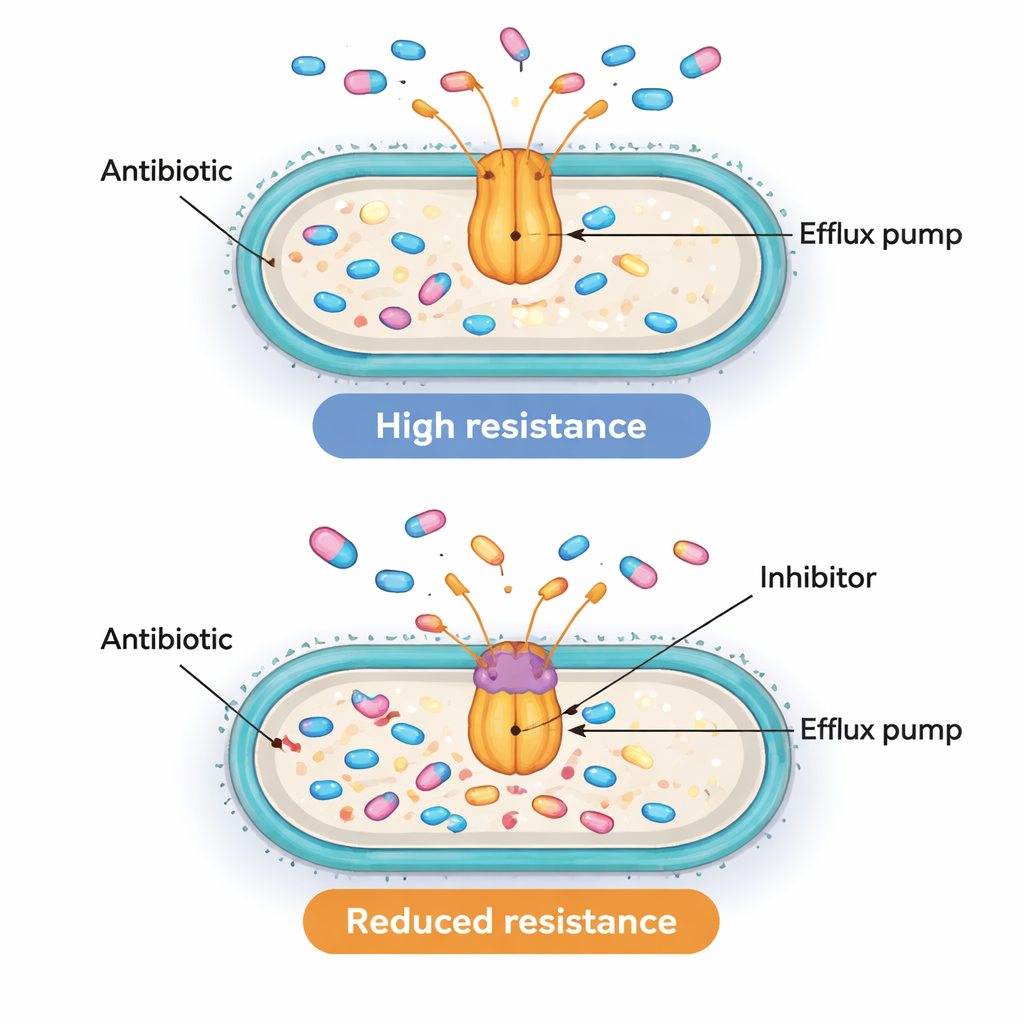
Um quebra‑cabeça complexo de resistência com alvos promissores
Nem toda cepa se comportou da mesma maneira. Algumas bactérias com expressão elevada dos genes de bomba recuperaram a sensibilidade apenas parcialmente quando as bombas foram bloqueadas, o que implica que outras vias de resistência — como alterações no alvo do antibiótico dentro da célula, produção de enzimas que inativam o fármaco ou bombas alternativas — também contribuem. A gentamicina, um antibiótico aminoglicosídeo, por exemplo, permaneceu em grande parte sem alteração pelos padrões observados em marA/soxS e nos genes AcrAB‑TolC, ressaltando que a multirresistência geralmente é construída a partir de várias defesas sobrepostas em vez de um único mecanismo.
O que isso significa para tratamentos futuros
Para não especialistas, a mensagem-chave é que algumas bactérias hospitalares podem sobreviver aos antibióticos não apenas bloqueando ou degradando os fármacos, mas ativamente os expulsando. Este estudo associa maior atividade de dois “interruptores” genéticos, MarA e SoxS, a bombas de efluxo mais ativas e a uma resistência mais forte a uma classe amplamente usada de antibióticos. Quando as bombas são experimentalmente bloqueadas, muitas dessas bactérias voltam a ficar pelo menos parcialmente sensíveis. Embora o trabalho ainda não prove exatamente como esses interruptores controlam as bombas, ele destaca tanto os reguladores quanto as bombas como alvos atraentes. A longo prazo, combinar antibióticos convencionais com bloqueadores de bombas seguros — ou fármacos que reduzam a atividade desses reguladores globais — poderia ajudar a restaurar a utilidade dos tratamentos existentes contra infecções multirresistentes antes intimidantes.
Citação: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Palavras-chave: resistência a antibióticos, bombas de efluxo, Klebsiella pneumoniae, fluoroquinolonas, reversão da resistência