Clear Sky Science · pt
Regulação negativa da enzima desubiquitinadora USP10 se correlaciona com apoptose neuronal na mielopatia associada ao HTLV-1
Por que isso importa para pessoas que vivem com doenças virais do sistema nervoso
Alguns vírus não causam apenas infecções de curta duração; eles podem danificar silenciosamente o sistema nervoso ao longo de muitos anos. O vírus linfotrópico de células T humano tipo 1 (HTLV-1) é um desses vírus e pode levar a um distúrbio crônico da medula espinhal chamado mielopatia associada ao HTLV-1 (HAM). Pessoas com HAM perdem gradualmente força e controle das pernas, além de apresentarem problemas urinários e sensoriais. Este estudo faz uma pergunta simples, porém crucial: por que as células nervosas da medula espinhal morrem nessa condição, e uma única molécula protetora poderia ajudar a explicar quem apresenta evolução pior ou melhor?
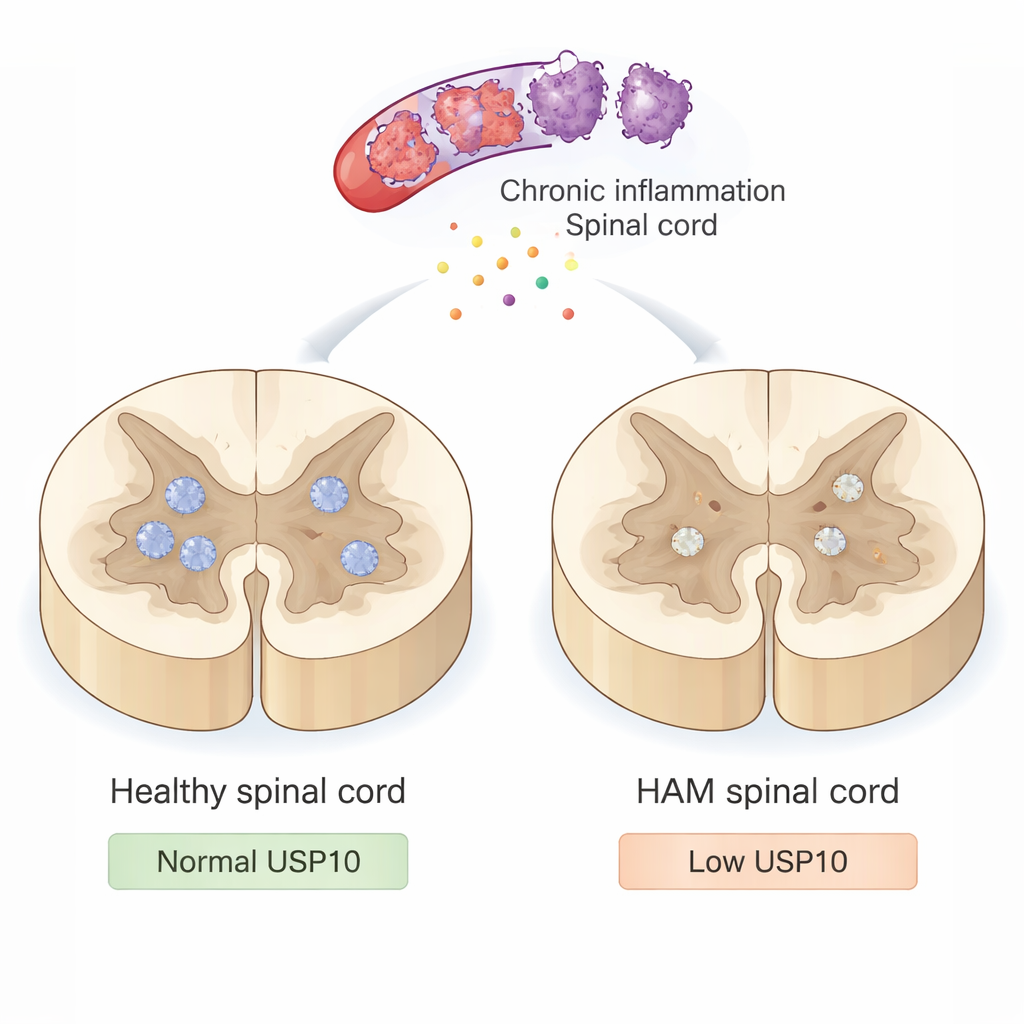
Um ataque lento à medula espinhal
A HAM não é causada pela infecção direta do vírus às células nervosas. Em vez disso, o HTLV-1 infecta células do sistema imune que invadem a medula espinhal e desencadeiam uma inflamação de longa duração. Essas células imunes hiperativas liberam substâncias tóxicas e sinais inflamatórios que, embora destinados a controlar a infecção, também lesionam neurônios próximos e sua bainha de mielina. Com o tempo, esse ataque persistente leva a pernas rígidas e fracas e dificuldade para caminhar. Ainda assim, os médicos não compreendem totalmente por que alguns neurônios sucumbem a esse ambiente inflamatório enquanto outros sobrevivem por décadas.
Uma enzima de “limpeza” celular sob suspeita
Os pesquisadores focaram em uma proteína chamada USP10, uma enzima que ajuda a gerir o sistema de controle de qualidade protéica da célula e é conhecida por limitar o estresse celular e a morte programada (apoptose). A USP10 é ativa em muitos tecidos, incluindo o cérebro e a medula espinhal, e trabalhos anteriores em doença de Parkinson, acidente vascular cerebral e outras condições sugerem que ela ajuda neurônios a resistirem a danos oxidativos e inflamatórios. Usando amostras de medula espinhal de oito pessoas que morreram com HAM e dois controles neurologicamente saudáveis, a equipe empregou técnicas de coloração para ver onde a USP10 estava presente e quão fortemente ela era expressa nas células nervosas.
Menos USP10, mais neurônios morrendo
Em medulas espinhais saudáveis, a USP10 era fortemente visível em muitos neurônios. Na maioria dos casos de HAM, no entanto, a coloração para USP10 nos neurônios estava claramente reduzida, e em um paciente estava quase ausente. Os cientistas então buscaram sinais característicos de apoptose usando dois métodos: um teste TUNEL que detecta DNA fragmentado e coloração para caspase-3 ativa, uma proteína envolvida nas fases iniciais da morte celular. Nos controles, praticamente nenhum neurônio mostrou esses sinais de morte. Em contraste, nos pacientes com HAM, uma grande fração de neurônios foi TUNEL-positiva e muitos mostraram caspase-3 ativa. Importante, amostras com menor expressão de USP10 tendiam a apresentar mais neurônios apoptóticos e menos neurônios sobreviventes marcados por NeuN, um marcador neuronal padrão. Um paciente notável com HAM que ainda andava apenas com uma bengala após 22 anos apresentou forte expressão de USP10 e números relativamente preservados de neurônios, sugerindo que níveis mais altos de USP10 podem ajudar a proteger contra incapacidade severa.
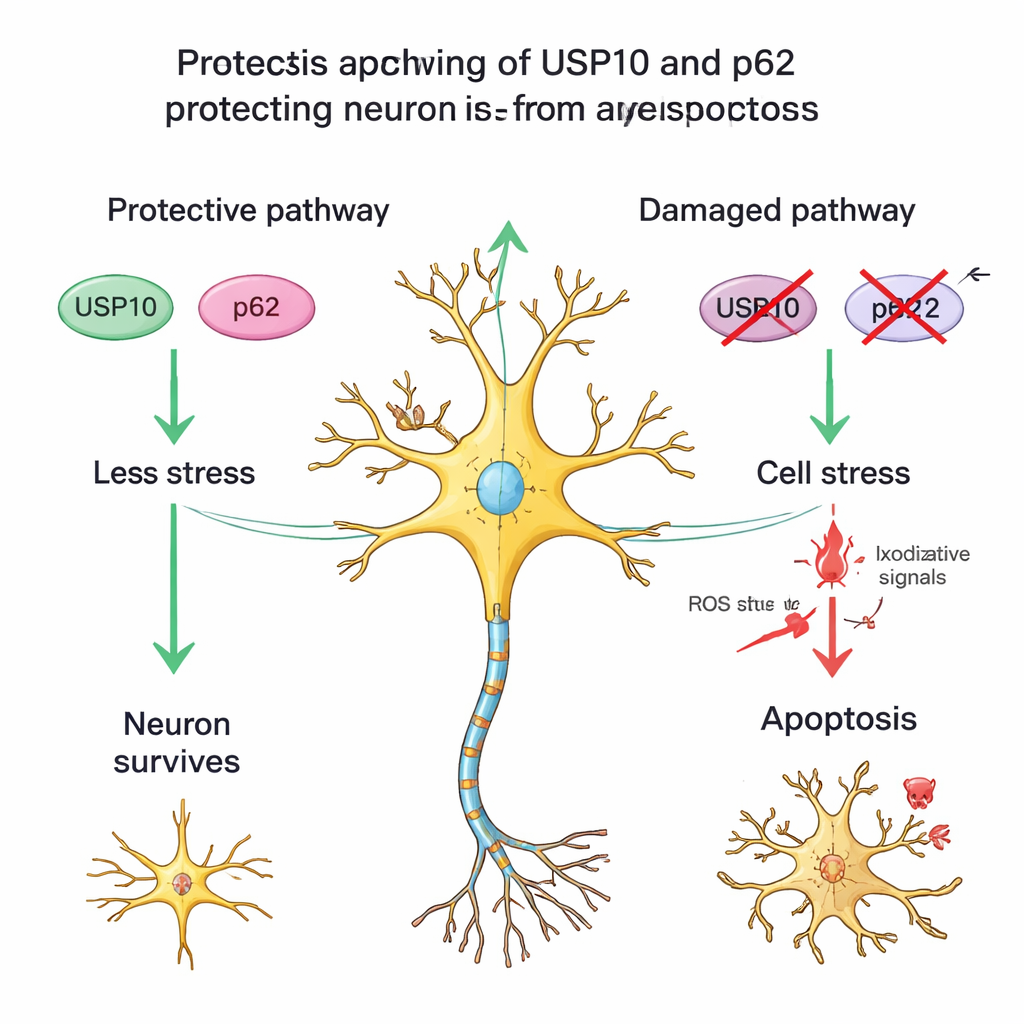
Uma proteína parceira e células estressadas, mas sobreviventes
A equipe também examinou outra proteína, p62, que atua com a USP10 no manejo de proteínas danificadas e na regulação de vias de estresse e sobrevivência. Em medulas espinhais saudáveis, a coloração para p62 era moderada; entre os pacientes com HAM, aqueles com baixa USP10 frequentemente também apresentavam coloração mais fraca para p62 e menos neurônios sobreviventes. Esse padrão apoia a ideia de uma parceria USP10–p62 que ajuda os neurônios a resistir à inflamação crônica. Os pesquisadores notaram ainda muitos neurônios no tecido de HAM que mantinham a típica morfologia de células nervosas, mas haviam perdido a coloração para NeuN, um sinal observado em outras lesões cerebrais quando neurônios estão sob estresse sério, porém não totalmente mortos. Isso sugere que, na HAM, alguns neurônios são perdidos de forma definitiva, enquanto outros permanecem em um estado danificado e vulnerável, possivelmente porque as defesas ligadas à USP10 estão enfraquecidas.
O que isso pode significar para diagnóstico e tratamento futuros
Este estudo não prova que a perda de USP10 causa diretamente a morte neuronal, pois é baseado em um pequeno número de amostras de autópsia e não pode acompanhar alterações ao longo do tempo. Ainda assim, as ligações consistentes entre baixa USP10, redução de p62, mais sinais de apoptose e menos neurônios sobreviventes apontam para uma via comum que pode conectar a inflamação crônica à degeneração neuronal lenta na HAM. Para pacientes, isso levanta uma possibilidade animadora: medir ou reforçar vias relacionadas à USP10 na medula espinhal — ou potencialmente em amostras mais acessíveis, como o líquido cefalorraquidiano — poderia um dia ajudar a identificar quem está em maior risco de progressão rápida, orientar o monitoramento ou inspirar novos tratamentos projetados para reforçar os próprios sistemas de proteção contra estresse das células em doenças neuroinflamatórias induzidas por vírus.
Citação: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Palavras-chave: mielopatia associada ao HTLV-1, neuroinflamação, apoptose neuronal, USP10, degeneração da medula espinhal