Clear Sky Science · pt
Atividade antibacteriana e citotoxicidade de cimentos à base de silicato tricálcico com diferentes aditivos antibacterianos
Por que isso importa para sua próxima obturação
Quando você tem uma cárie profunda, os dentistas hoje tentam salvar o máximo possível do dente natural em vez de perfurar tudo. Isso frequentemente significa que uma fina camada de dentina amolecida, contendo bactérias, é deixada sob a restauração. Este estudo faz uma pergunta simples, porém crucial: podemos aprimorar um cimento amplamente usado para reparar dentes de modo que ele elimine silenciosamente os germes remanescentes sem prejudicar as células vivas dentro do dente?
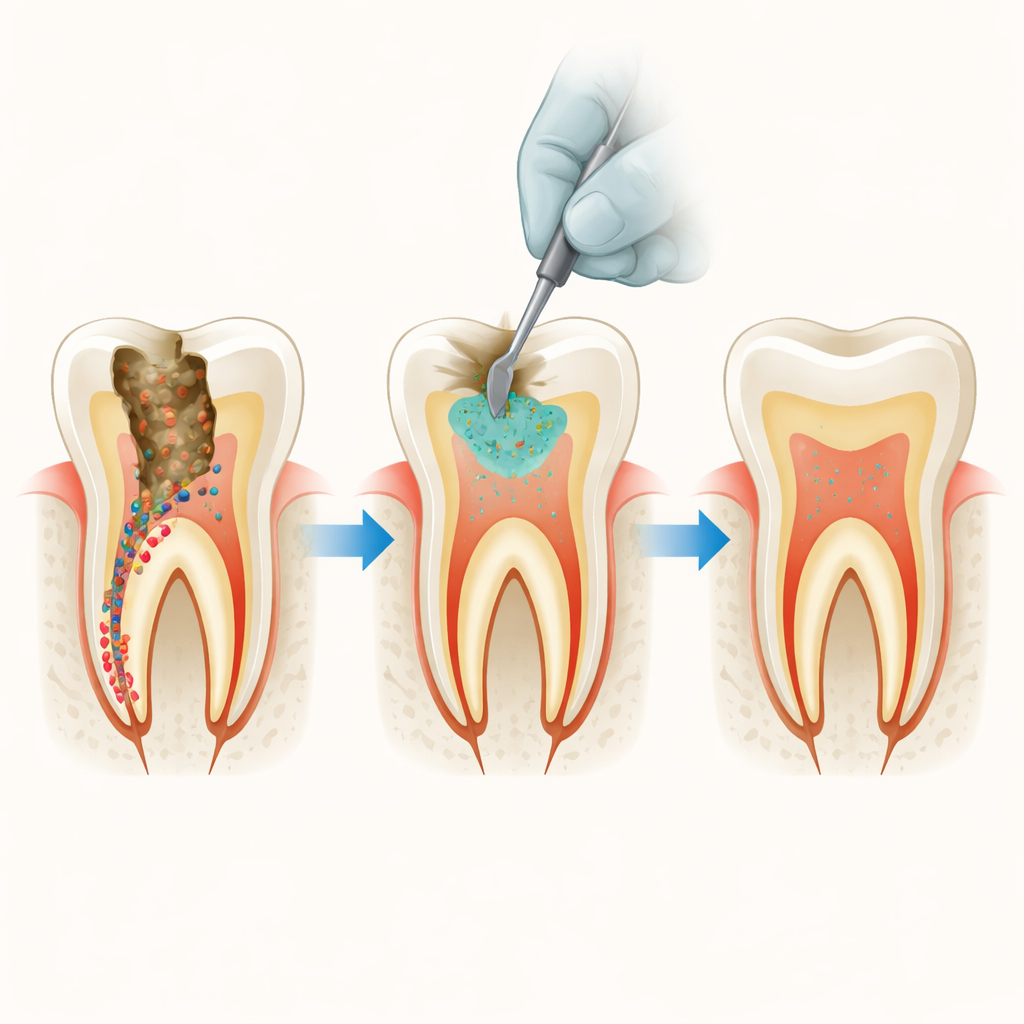
Cáries profundas e germes ocultos
As técnicas modernas de "perfuração mínima" visam evitar expor o núcleo mole do dente, ou polpa, deixando uma dentina que ainda pode se remineralizar. A desvantagem é que algumas bactérias causadoras de cárie, como Streptococcus mutans e espécies de Lactobacillus, podem permanecer nessa camada. Com o tempo, essas bactérias podem provocar nova deterioração sob uma restauração aparentemente saudável. Cimentos à base de silicato tricálcico são populares para selar cavidades profundas porque ajudam a reformar minerais e criam uma barreira estanque, mas isoladamente não são muito eficientes em deter bactérias.
Transformando um cimento comum em um combatente de germes
Os pesquisadores pegaram esse cimento conhecido e misturaram cinco diferentes aditivos antibacterianos em várias concentrações. Dois eram compostos orgânicos frequentemente encontrados em desinfetantes (cloreto de benzalcônio e cetrimida), e três eram substâncias inorgânicas usadas em produtos ou materiais dentais (óxido de titânio, óxido de zinco e fluoreto estanhoso). Eles prensaram essas misturas em pequenos discos e os colocaram em placas cobertas com cinco tipos de bactérias associadas à cárie dentária e infecções orais. Medindo os círculos de clareamento ao redor de cada disco onde as bactérias não conseguiam crescer, puderam avaliar o quanto cada receita inibia os germes.
Encontrando o ponto de equilíbrio entre matar germes e poupar células
Como um material que mata bactérias mas também envenena as células do dente seria inútil na boca, a equipe também testou como os aditivos mais promissores afetavam células vivas. Eles expuseram indiretamente dois tipos de células humanas — fibroblastos, que são células de suporte comuns, e células-tronco da polpa dentária, que ajudam a reparar o tecido dentário — aos cimentos. Um teste de mudança de cor mediu quantas células permaneceram ativas, e corantes fluorescentes especiais mostraram células vivas (verde) e mortas (vermelho) ao microscópio. Esse arranjo mimetizou a situação real em uma cárie profunda, onde o cimento fica separado da polpa por uma fina camada de dentina e libera substâncias que difundem em direção às células.
O que funcionou melhor e o que foi forte demais
Os resultados mostraram que o tipo e a quantidade do aditivo importavam muito. O cloreto de benzalcônio proporcionou o efeito antibacteriano mais forte e mais amplo, produzindo grandes zonas livres de germes contra todas as espécies testadas, especialmente as linhagens de Lactobacillus frequentemente encontradas em cáries profundas. A cetrimida também ajudou, mas geralmente exigiu concentrações maiores para igualar o desempenho do benzalcônio. Os três agentes inorgânicos só melhoraram o efeito antibacteriano do cimento nas doses mais altas testadas e, mesmo assim, principalmente contra bactérias específicas como S. mutans e Actinomyces. No aspecto de segurança, o cimento base sozinho foi bem tolerado por ambos os tipos celulares e até pareceu favorecer a saúde dos fibroblastos. A adição de cloreto de benzalcônio permaneceu inócua para fibroblastos até cerca de 1%, tornou-se ligeiramente prejudicial em 2–4% e claramente mais nociva em 7%. As células-tronco da polpa dentária foram mais sensíveis no geral: tanto o cloreto de benzalcônio quanto a cetrimida reduziram sua sobrevivência, com a cetrimida tornando-se moderadamente tóxica a partir de 2%.
O que isso pode significar para o futuro do cuidado dental
Juntando esses achados, o estudo aponta para uma receita especialmente promissora: cimento à base de silicato tricálcico contendo 1% de cloreto de benzalcônio. Nesse nível, o material suprimiu fortemente bactérias nocivas enquanto mantinha os fibroblastos totalmente vivos e as células-tronco da polpa dentária em sua maioria viáveis. Em termos práticos, isso sugere que futuras obturações profundas poderiam ser feitas com um cimento que combate discretamente os germes remanescentes sob a superfície ao mesmo tempo em que é suficientemente gentil com o tecido vivo dentro do dente. Mais trabalho é necessário — especialmente em condições bucais complexas e do mundo real —, mas essa fórmula equilibrada pode ajudar os dentistas a proteger melhor dentes tratados com técnicas minimamente invasivas.
Citação: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Palavras-chave: cárie dentária profunda, cimento dental antibacteriano, silicato tricálcico, cloreto de benzalcônio, biocompatibilidade de células da polpa